Dimethoxyethan - Dimethoxyethane
 | |
 | |
| Jména | |
|---|---|
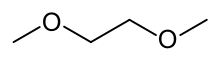
| Preferovaný název IUPAC 1,2-dimethoxyethan[1] | |
| Ostatní jména Ethan-1,2-diyldimethylether[1] DME Glyme Ethylenglykol dimethylether Monoglym Dimethyl glykol Dimethylcellosolve | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA | 100.003.451 |
PubChem CID | |
| Číslo RTECS |
|
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C4H10Ó2 | |
| Molární hmotnost | 90.122 g · mol−1 |
| Vzhled | Bezbarvá kapalina |
| Hustota | 0,8683 g / cm3 |
| Bod tání | -58 ° C (-72 ° F; 215 K) |
| Bod varu | 85 ° C (185 ° F; 358 K) |
| mísitelný | |
| Nebezpečí | |
Klasifikace EU (DSD) (zastaralý) | Hořlavý (F) Toxický (T) Repr. Kočka. 2 |
| R-věty (zastaralý) | R60, R61, R11, R19, R20 |
| S-věty (zastaralý) | S53, S45 |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | -2 ° C (28 ° F; 271 K) |
| Související sloučeniny | |
Příbuzný Etherové | Dimethoxymethan |
Související sloučeniny | Ethylenglykol 1,4-dioxan Diethylenglykol dimethylether |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Dimethoxyethan, také známý jako glyme, monoglym, dimethyl glykol, ethylenglykol dimethylether, dimethylcellosolve, a DME, je bezbarvý, aprotický a kapalina éter který se používá jako solventní, zejména v bateriích.[2] Dimethoxyethan je mísitelný s voda.
Výroba
Monoglym se průmyslově vyrábí reakcí dimethylether s ethylenoxid:[3][4]
- CH3OCH3 + CH2CH2O → CH3OCH2CH2OCH3
Aplikace jako rozpouštědlo a ligand

Spolu s vysokoupermitivita rozpouštědlo (např. propylenkarbonát ) se jako nízko-viskozita složka rozpouštědla pro elektrolyty z lithiové baterie. V laboratoři se DME používá jako koordinační rozpouštědlo.
Dimethoxyethan se často používá jako alternativa s vyšším bodem varu diethylether a THF. Dimethoxyethan působí jako dvojzubec ligand pro některé kovové kationty. Proto se často používá v organokovová chemie. Grignardovy reakce a hydridové redukce jsou typické aplikace. Je také vhodný pro reakce katalyzované palladiem počítaje v to Suzukiho reakce a Stille spojky. Dimethoxyethan je také dobrým rozpouštědlem pro oligo - a polysacharidy.
Reference
- ^ A b Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 704. doi:10.1039/9781849733069-00648. ISBN 978-0-85404-182-4.
- ^ D. Berndt, D. Spahrbier, „Baterie“ v Ullmann's Encyclopedia of Industrial Chemistry 2005, Wiley-VCH, Weinheim. doi:10.1002 / 14356007.a03_343
- ^ Siegfried Rebsdat a Dieter Mayer (2000). "Ethylenglykol". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a10_101. ISBN 3527306730.CS1 maint: používá parametr autoři (odkaz)
- ^ Dimethoxyethan
- ^ Arteaga-Müller, Rocío; Tsurugi, Hayato; Saito, Teruhiko; Yanagawa, Masao; Oda, Seiji; Mashima, Kazushi (2009). „Nový tantalový katalyzátor bez ligandu pro vysoce selektivní trimerizaci ethylenu poskytujícího 1-hexen: nový důkaz mechanismu metalocyklů“. Journal of the American Chemical Society. 131 (15): 5370–5371. doi:10.1021 / ja8100837. PMID 20560633.

