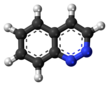
Cinnoline - Cinnoline
 | |||
| |||
| Jména | |||
|---|---|---|---|
| Preferovaný název IUPAC Cinnoline | |||
| Ostatní jména Benzopyridazin | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Informační karta ECHA | 100.005.423 | ||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C8H6N2 | |||
| Molární hmotnost | 130.150 g · mol−1 | ||
| Bod tání | 39 ° C (102 ° F; 312 K) | ||
| Kyselost (strK.A) | 2.64[1] | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Cinnoline je aromatický heterocyklická sloučenina se vzorcem C.8H6N2. to je izomerní s ostatními naftyridiny počítaje v to chinoxalin, ftalazin a chinazolin.
Vlastnosti
Volnou bázi lze získat jako olej zpracováním hydrochlorid se základnou. Po ochlazení éterických roztoků kokrystaluje s jednou molekulou etheru jako bílé hedvábné jehly (t.t. 24–25 ° C). Volný základna taje při 39 ° C. Má chuť podobnou chuti chloralhydrát a po určitou dobu zanechává ostré podráždění. Deriváty cinolinu se získávají z oxycinnolinkarboxylové kyseliny, která se tvoří štěpením diazochloridu kyseliny orthofenylpropiolové vodou. Oxycinnolinkarboxylová kyselina zahříváním poskytne oxycinnolin tající při 225 ° C, který s chlorid fosforečný dává chlorcinnolin. Tato látka je snížena o Železné piliny a kyselina sírová na dihydrocinnolin.
Objev a syntéza
Sloučenina byla nejprve získána v nečisté formě cyklizací alkyn Ó-C6H4(NH2) C≡CCO2H ve vodě, čímž se získá kyselina 4-hydroxycinolin-3-karboxylová. Tento materiál by mohl být dekarboxylovaný a hydroxylová skupina se redukčně odstraní za vzniku mateřského heterocyklu. Tato reakce se nazývá Bohatší syntéza cinolinu.[2] Pro jeho syntézu existují vylepšené metody. Může být připraven dehydrogenace z dihydrocinnolin s čerstvě vysráženým oxid rtuťnatý. Může být izolován jako hydrochlorid.[3]
Cinnolines jsou deriváty cinolinu. Klasika organická reakce pro syntézu cinnolinů je Widman – Stoermerova syntéza,[4] A reakce uzavření kruhu α-vinyl- anilin s kyselina chlorovodíková a dusitan sodný:

Dusitan sodný se nejprve převede na kyselina dusitá který pak tvoří elektrofilní středně pokročilí oxid dusný. Další meziprodukt je stáj nitrosamin s ztrácí vodu tvořící diazoniová sůl který pak reaguje s vinylovou skupinou v kroku uzavření kruhu. Koncepčně související reakcí je Bambergerova syntéza triazinu směrem k triazinům.
Další metodou cinnoline je Syntéza cinolinu Borsche.
Bezpečnost
Cinnoline je toxický.[Citace je zapotřebí ]
Viz také
Reference
- ^ Brown, H.C. a kol., Baude, E.A. a Náchod, F.C., Stanovení organických struktur fyzikálními metodami, Academic Press, New York, 1955.
- ^ Victor von Richter (1883). „Über Cinnolinderivate“. Chemische Berichte. 16: 677–683. doi:10,1002 / cber.188301601154.
- ^ Parrick, J .; Shaw, C. J. G .; Mehta, L. K. (2000). "Pyridaziny, cinnoliny, benzocinnoliny a ftalaziny". Roddova chemie uhlíkových sloučenin. 4 (2. vyd.). s. 1–69.
- ^ Bradford P. Mundy; Michael G. Ellerd; Frank G. Jr. Favaloro (2005). Pojmenujte reakce a činidla v organické syntéze. ISBN 0-471-22854-0.