Pikolinát chromitý - Chromium(III) picolinate
 | |||
| |||
| Jména | |||
|---|---|---|---|
| Název IUPAC Tris (pikolinát) chrom (III) | |||
| Identifikátory | |||
3D model (JSmol ) |
| ||
| ChEBI | |||
| ChemSpider | |||
| Informační karta ECHA | 100.131.423 | ||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| Cr (C.6H4NE2)3 | |||
| Molární hmotnost | 418,33 g / mol | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Pikolinát chromitý (CrPic3) je chemická sloučenina prodáván jako doplněk výživy k léčbě typu 2 cukrovka a podporovat hubnutí.[1] Tento jasně červený koordinační sloučenina je odvozen z chrom (III) a kyselina pikolinová. Je zapotřebí velkého množství chromu glukóza využití do inzulín v normálním zdraví, ale nedostatek je extrémně běžný a byl pozorován u lidí, kteří dostávají 100% svých potřeb živin intravenózně, tj. celkem parenterální výživa diety.[2] Chrom byl identifikován jako regulující inzulín zvýšením citlivosti inzulinový receptor.[3] Proto byl jako léčba typu 2 navržen pikolinát chromitý cukrovka, ačkoli jeho účinnost zůstává kontroverzní kvůli protichůdným důkazům z pokusů na lidech.[4]
Dějiny
Studie z roku 1989 naznačuje, že pikolinát chromitý může pomáhat při hubnutí a zvyšování svalové hmoty, což vedlo ke zvýšení používání pikolinátu chromitého doplňky, což má za následek, že je na chvíli druhým nejčastěji používaným doplňkem vápníku.[4] 2013 Cochrane recenze nebyl schopen najít „spolehlivé důkazy pro rozhodování o pevných rozhodnutích“ na podporu těchto tvrzení.[5] Výzkum obecně ukázal, že zlepšuje citlivost na inzulín buď prodloužením jeho aktivity, nebo zvýšením regulace produkce mRNA vyrábět více receptory inzulínu.[Citace je zapotřebí ]
Mezi přechodné kovy, Cr3+ je nejkontroverznější z hlediska nutriční hodnoty a toxicity.[6] Tato diskuse se soustředí na to, zda Cr3+ poskytuje jakékoli výživové výhody.[6][7] Kromě toho je tato kontroverze umocněna skutečností, že u žádných biomolekul obsahujících Cr nebyla charakterizována jejich struktura ani nebyl stanoven způsob účinku. První experiment, který vedl k objevení Cr3+ hraje roli v metabolismu glukózy navrhl, že biologicky aktivní forma kovu existovala v proteinu zvaném faktor tolerance glukózy, nicméně, nové důkazy naznačují, že se jedná pouze o artefakt získaný z izolačních postupů.[4][6][8][9] Jediný přijatý indikátor nedostatek chromu je zvrácení příznaků, ke kterému dochází při podávání suplementace chromu (III) lidem na celková parenterální výživa.[10]
Fyzikálně-chemické vlastnosti


Pikolinát chromitý je růžovočervená sloučenina a poprvé byla uvedena v roce 1917.[4][11] Je špatně rozpustný ve vodě, má a rozpustnost 600 μM ve vodě téměř neutrální pH.[7] Podobně jako u jiných sloučenin chromu je to relativně inertní a nereaktivní, což znamená, že tento komplex je stabilní za podmínek okolí a k rozkladu jsou nutné vysoké teploty sloučenina.[12] Při nižších úrovních pH komplex hydrolyzuje uvolnit kyselina pikolinová a zdarma Cr3+.[7]
Struktura
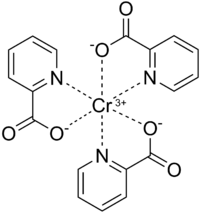
Pikolinát chromitý (III) je zkreslený oktaedrická geometrie a je izostrukturální na kobalt (III) a mangan (III) protějšky.[13][14] Chrom (III) je a tvrdá kyselina lewisová a jako takový má vysoká afinita do karboxylát kyslík a střední afinita k pyridin dusík z pikolinát.[13][15] Každý pikolinátový ligand působí jako a bidentate chelátování agent a neutralizuje náboj +3 Cr3+. Důkazy, že Cr3+ souřadnice středu pyridinového dusíku pochází z posunu v IR spektra C = N vibrace na 1602,4 cm−1 pro volnou kyselinu pikolinovou na 1565,9 cm−1 pro pikolinát chromitý.[13] The délka vazby mezi Cr3+ a atom dusíku pyridinového kruhu na pikoliantu se pohybuje v rozmezí od 2,047 do 2,048 A.[14] Pikolinátový ligand se koordinuje s Cr3+ pouze když deprotonovaný a je to patrné ze zmizení IR pásem v rozmezí od 2400 do 2800 cm−1 (se středem na 2500 cm−1) a 1443 cm−1, což odpovídá roztahování a ohýbání O-H na karboxylové funkční skupině.[12][13] Dále tento IR posun také naznačuje, že pouze jeden atom kyslíku z karboxylátu pikolinátových souřadnic na Cr3+ centrum.[12][13][15] Délka vazby Cr-O se pohybuje od 1,949 do 1,957 A.[14] The Krystalická struktura byl popsán teprve nedávno v roce 2013.[15] Voda nekoordinuje s Cr3+ centrum a místo toho se o něm uvažuje vodíková vazba mezi ostatními Cr (obr)3 komplexy k vytvoření sítě Cr (Pic)3 komplexy.[15]
Biochemie pikolinátu chromitého
Chrom byl identifikován jako základní živina při udržování normální hladiny glukózy v krvi a jako takové se navrhuje interakce se dvěma přirozeně se vyskytujícími molekulami nacházejícími se v těle.[8] Tyto interakce se s největší pravděpodobností vyskytují prostřednictvím koordinace s tvrdými ligandy, jako je aspartát a glutamát, protože samotný Cr (III) je tvrdý kov.
Absorpce a vylučování pikolinátu chromitého
Jakmile je pikolinát chromitý požit a vstoupí do žaludek, kyselé hydrolýza komplexu dochází při kontaktu s sliznice žaludku.[16] Hydrolyzovaný Cr3+ je přítomna ve formě hexaaqua a polymerizuje za vzniku nerozpustného hydroxidu chromitého (III) olace ) jakmile dosáhne zásaditý pH tenké střevo.[17] Přibližně 2% Cr3+ se vstřebává střevem jako pikolinát chromitý přes nenasycené pasivní doprava.[11] Ačkoli je absorpce nízká, CrPic3 absorbuje účinněji než jiné organické a anorganické zdroje (tj. CrCl3 a nikotinát chromitý) a tak se hromadí ve vyšších koncentracích v tkáních.[9][18] To byl jeden hlavní prodejní bod pro pikolinát chromitý (III) oproti jiným doplňkům chromu (III). Organické zdroje mají tendenci lépe absorbovat, protože mají více ligandů lipofilní a obvykle neutralizují náboj kovu, což umožňuje snadnější průchod střevní membránou.[18]
Bylo také prokázáno, že dietní faktory ovlivňují Cr3+ vstřebávání. Škrob, jednoduché cukry, kyselina šťavelová, a nějaký aminokyseliny mají tendenci zvyšovat rychlost absorpce chromu (III). To je výsledek chelatace ligandu, přeměny hexaaqua Cr3+ do lipofilnějších forem.[18] Naproti tomu vápník, hořčík, titan, zinek, vanad a železo snižují rychlost absorpce.[18] Pravděpodobně tyto ionty zavádějí nové rovnováhy kov-ligand, čímž snižují zásobu lipofilního ligandu dostupnou pro Cr3+. Jakmile je absorbováno do krevního řečiště, 80% Cr3+ od CrPic3 se předává transferinu.[16][18][19] The přesný mechanismus uvolňování není v současné době známo, předpokládá se však, že k němu nedochází jedinou elektronovou redukcí, jako v případě Fe3+, kvůli vysoké nestabilitě Cr2+.[17] Spravováno Cr3+ lze nalézt ve všech tkáních v rozmezí 10–100 μg / kg tělesné hmotnosti.[18] Vylučuje se primárně močí (80%), zbytek se vylučuje potem a výkaly.[18]
Vazba chromu (III) na transferin

Transferrin, navíc chromodulin byl identifikován jako hlavní fyziologický transport chromu,[19][21] ačkoli nedávná studie zjistila, že Cr3+ ve skutečnosti zakazuje transferinu působit jako prostředek přenosu kovových iontů.[22] Zatímco transferin je vysoce specifický pro železité ionty, za normálních podmínek je pouze 30% molekul transferinu nasyceno železitými ionty, což umožňuje také vazbu dalších kovů, zejména těch s velkým poměrem náboje k velikosti.[7][11][20] Vazebná místa se skládají z C-laloku a N-laloku, které mají téměř identickou strukturu.[20] Každý lalok obsahuje kyselina asparagová, histidin, 2 tyrosin zbytky a hydrogenuhličitan iont, který působí jako a bidentate ligand, aby se železo nebo jiné kovy mohly zkresleně vázat na transferin oktaedrická geometrie.[19][20][21] Důkazy podporující závazek Cr3+ k transferinu pochází z rozsáhlých klinických studií, které prokázaly pozitivní korelaci mezi hladinami feritin a půstu glukóza, inzulín, a glykosylovaný hemoglobin (Hb1Ac) úrovně.[7] Dále an in vivo studie na potkanech ukázala, že 80% izotopově značeného Cr3+ skončil na transferinu, zatímco ostatní byli vázáni albumin. An in vitro studie ukázala, že když byl k izolovanému transferinu přidán chlorid chromitý, Cr3+ snadno vázaný transferrin v důsledku změn ve UV-Vis spektru.[11][19][23] The konstanta formace pro Cr3+ v C-laloku je 1,41 x 1010 M−1 a 2,04 x 105 M−1 v N-laloku, což naznačuje, že Cr3+ přednostně váže C-lalok.[7][19][20] Celkově je konstanta tvorby chromu (III) nižší než u železitého iontu.[19] Bikarbonátový ligand je rozhodující pro vazbu Cr3+ jako když jsou koncentrace hydrogenuhličitanu velmi nízké, vazebná afinita je také významně nižší.[19] Elektronová paramagnetická rezonance Studie (EPR) ukázaly, že pod pH 6 se chrom (III) váže pouze na N-lalok a že při téměř neutrálním pH se chrom (III) váže také na C-lalok.[7] Chrom (III) může soutěžit s železitým iontem o vazbu na C-lalok, když nasycení výrazně přesahuje 30%.[20] Tyto účinky jsou tedy patrné pouze u pacientů trpících hemochromatóza, onemocnění akumulace železa charakterizované nadměrnou saturací železa v transferinu.[23]
Mechanismus účinku

Nízkomolekulární látka vázající chrom (LMWCr; také známý jako chromodulin) je oligopeptid, který, jak se zdá, váže v těle chrom (III).[24] Skládá se ze čtyř aminokyselinových zbytků; aspartát, cystein, glutamát, a glycin, spojený čtyřmi (Cr3+) centra.[7][10][25] Interaguje s inzulinovým receptorem prodloužením aktivity kinázy stimulací dráhy tyrosinkinázy, což vede ke zlepšení absorpce glukózy.[19][26] To bylo zaměňováno s faktor tolerance glukózy. Přes nedávné snahy charakterizovat chromodulin je přesná struktura stále relativně neznámá.[27]
Přesný mechanismus působení chromodulinu na inzulinový receptor je v současné době neznámý, jeden obecně popsaný mechanismus je uveden níže. Tento navrhovaný mechanismus má nejvyšší míru shody s různými experimenty zahrnujícími chromodulin.[6][11][17][23]
Chromodulin obvykle existuje ve formě apochromodulinu, který neobsahuje ionty Cr (III) a má minimální aktivitu na inzulínové receptory.[23] Apochromodulin je uložen v buňkách citlivých na inzulín v jádře. Když stoupne hladina glukózy v krvi, inzulín se uvolňuje do krevního řečiště a váže se na vnější α-podjednotku inzulínového receptoru, a transmembránový protein.[25] Inzulínový receptor se skládá ze 2 extracelulárních α-podjednotek a 2 transmembránových p-podjednotek.[23] Jakmile se inzulín váže na inzulínový receptor, dojde ke konformační změně v receptoru, což způsobí všechny 3 tyrosin zbytky (umístěné v p-podjednotkách), které mají být fosforylovány. To aktivuje receptor a umožňuje mu přenášet signál z inzulínu do buňky.[10][23][25]Jak bylo uvedeno výše, absorbovaný pikolinát chromitý se nakonec vzdá Cr3+ k transferinu. Na druhé straně transferin transportuje Cr3+ na buňky citlivé na inzulín (tj. adipocyty ) kde se váže na apochromodulin za vzniku holochromodulinu.[23] Holochromodulin se váže na inzulínový receptor, což pomáhá udržovat aktivní konformaci inzulínového receptoru prodloužením kinázové aktivity kinázy nebo up-regulující množství inzulínového receptoru mRNA hladiny, čímž se snižují hladiny glukózy v krvi.[10]
Experimenty dokázaly, že chrom (III) byl schopen regulovat inzulínem stimulovanou signální transdukci inzulínu prostřednictvím ovlivnění molekul IR po proudu, jak dokazuje zvýšená hladina fosforylace tyrosinu IRS-1, zvýšené Thr308 a Ser473 fosforylace z Akt a zvýšil se PI3-K aktivita v různých buněčných a zvířecích modelech.[28] Zvýšená fosforylace IRS-1 vedla ke zvýšené citlivosti na inzulínové receptory, zatímco Akt a PI3-K vedly ke zvýšení GLUT4 translokace na povrch buněk, což způsobuje větší absorpci glukózy.[28]
Bylo také prokázáno, že chrom (III) může zmírnit rezistence na inzulín redukcí endoplazmatické retikulum (ER) stres.[28] ER stres je definován jako akumulace špatně poskládaných a rozložených proteinů v lumenu ER.[28] ER stres vede ke stimulaci terminální kinázy c-Jun (JNK ), který zase fosforyluje serinový zbytek IRS, což vede k potlačení kaskády signalizace inzulínu a menšímu příjmu glukózy.[29] Experimentální nálezy naznačují, že chrom inhibuje ER stres, a proto je potlačena potlačení inzulínové signalizace.[29] Přesný mechanismus není znám.[29]
Dalším způsobem, že Cr (III) může prodloužit kinázovou aktivitu inzulínového receptoru, je oxidace kritického Aktivní stránky cysteinový zbytek na protein-tyrosin fosfatáze 1B (PTP1B ). Za normálních okolností PTP1B defosforyluje fosfotyrosinové zbytky prováděním nukleofilního útoku na fosfátovou skupinu prostřednictvím svého cysteinového zbytku, čímž inaktivuje inzulinový receptor.[30] Tento proces odstraňuje fosfátovou skupinu z tyrosinového zbytku za vzniku Cys-S-PO32− skupina, která je následně hydrolyzována vodou k regeneraci cysteinového zbytku, což umožňuje další kolo působení.[30] Výzkum ukázal, že chrom (III) může ve skutečnosti způsobit nevratnou inhibici PTP1B. Předpokládá se, že Cr (III) se převádí na Cr (VI) nebo Cr (V) (působením oxidoreduktázy ), které poté oxidují thiol cysteinového zbytku na PTP1B až kyselina sulfenová, v důsledku čehož není schopen zaútočit na fosfátovou skupinu na fosfotyrosinu.[31] Jedná se však pouze o věrohodný mechanismus a nebyl prokázán žádný přímý důkaz podporující tuto hypotézu.[30]Když je signální kaskáda vypnutá, holochromodulin je vylučován močí od konstanta formace je příliš velký na to, aby přímo odstranil Cr (III).[7] Experimentální důkazy ukázaly, že ztráta chromodulinu z buněk koreluje se zvýšením koncentrací chrómu v moči po požití potravy bohaté na sacharidy (tj. Glukózy).[25]
Zdravotní tvrzení a debaty
Tělesná hmotnost
Pikolinát chromitý (III) byl uveden na trh ve Spojených státech jako pomoc při vývoji těla pro sportovci a jako prostředek hubnout. Recenze uvádějí buď žádný vliv na růst svalů nebo ztrátu tuku,[32] nebo také mírný, ale statisticky významný úbytek hmotnosti o 1,1 kg (2,4 lb) ve studiích delších než 12 týdnů.[5] The Evropský úřad pro bezpečnost potravin přezkoumal literaturu a dospěl k závěru, že neexistují dostatečné důkazy na podporu tvrzení.[33]
Cukrovka
Existují tvrzení, že pikolinátová forma suplementace chrómu pomáhá při redukci rezistence na inzulín a zlepšování metabolismus glukózy, zejména u typu 2 diabetici, ale recenze neprokázaly žádnou souvislost mezi koncentrací chrómu a glukózy nebo inzulínu u nediabetiků a neprůkazné výsledky u diabetiků.[34][35] Autoři druhého přehledu zmínili, že pikolinát chromitý se snížil HbA1c hladiny o 0,7% u pacientů s diabetem typu 2, zjistili, že nekvalitní studie přinesly větší pozitivní výsledky než kvalitnější studie.[35][36] Dvě hodnocení dospěla k závěru, že pikolinát chromitý může být účinnější při snižování glukóza v krvi úrovně ve srovnání s jinými doplňky stravy obsahujícími chrom.[35][37]
V roce 2005 USA Úřad pro kontrolu potravin a léčiv (FDA) schválila kvalifikované zdravotní tvrzení pro pikolinát chromitý jako doplněk stravy týkající se inzulínové rezistence a rizika cukrovky 2. typu. Každá společnost, která si přeje učinit takové tvrzení, musí použít přesné znění: „Jedna malá studie naznačuje, že pikolinát chromitý může snížit riziko inzulínové rezistence, a proto možná může snížit riziko cukrovky typu 2. FDA však dochází k závěru, že existence vztah mezi pikolinátem chromitým a buď inzulínovou rezistencí, nebo diabetem typu 2, je velmi nejistý. “ V rámci procesu přezkoumání petice FDA zamítla další tvrzení týkající se snížení abnormálně zvýšené hladiny cukru v krvi, rizika kardiovaskulárních onemocnění, rizika retinopatie nebo rizika onemocnění ledvin.[38] V roce 2006 FDA dodal, že „vztah mezi příjmem pikolinátu chromitého a inzulínovou rezistencí je velmi nejistý“.[39]
Variabilita studií
V klinických výsledcích týkajících se pikolinátu chromitého s adekvátní léčbou diabetu 2. typu nebyla pozorována konzistence. To je způsobeno stupněm intolerance glukózy u pacientů, kteří se účastní klinických studií.[9] Intolerance glukózy je gradient a její intenzitu ovlivňuje etnická příslušnost, stupeň obezity, věk, distribuce tělesného tuku a mnoho dalších faktorů.[9] V některých studiích byly podávány nízké dávky doplňku, avšak musí být člověku podáno vhodné množství pikolinátu chromitého, než bude pozorován jakýkoli znatelný pokles hladiny glukózy v důsledku různých úrovní inzulínové rezistence. Dalším důležitým bodem, který je třeba zmínit, je, že cukrovka není vždy způsobena intolerancí glukózy.[9] Jak již bylo zmíněno dříve, bylo prokázáno, že Cr (III) ovlivňuje pouze intoleranci glukózy, nikoli hladinu inzulínu. Prostředí, ve kterých byly studie prováděny, navíc nebyla konzistentní. Úrovně stresu, strava konzumovaná pacienty a genetika pacientů se u studovaných subjektů lišily.[9] To platí také o kontrolách mezi různými studiemi, ve kterých byli jedinci s cukrovkou již léčeni širokou škálou antidiabetických léků, které mohou snížit účinky chrómu na ovlivnění inzulínové aktivity.[29] To by mohlo vysvětlit, proč studie na zvířatech mají tendenci přinášet pozitivnější výsledky vzhledem k tomu, že tato diabetická zvířata nebyla pro kontrolní skupinu léčena antidiabetiky.[29] Jak je uvedeno v části o absorpci a vylučování, strava ovlivňuje absorpci / biologickou dostupnost pikolinátu chromitého. Dohromady tyto různé faktory přispěly k variabilitě studií.
Bezpečnost a toxicita
Byly vzneseny počáteční obavy, že je pravděpodobnější, že je způsobí pikolinát chromitý Poškození DNA a mutace než jiné formy trojmocný chrom,[40] ale tyto výsledky jsou také diskutovány.[41] Tyto obavy byly částečně založeny na studiích na ovocných muškách, kde suplementace pikolinátu chromitého vytváří chromozomální aberace, brání vývoji potomků,[42] a způsobuje sterilitu a smrtící mutace.[43]
Byla publikována studie hodnotící toxicitu pikolinátu Cr (III) na lidech.[44] Vědci, kteří provedli tuto studii, použili předchozí znalosti, že Cr (III) je redukován na Cr (II) buněčnými reduktanty, jako je NADH nebo cystein.[44] Ukázalo se, že tato redukovaná forma Cr (II) reaguje s H2Ó2 vygenerovat radikální druhy což zase okysličovat Páry bází DNA.[45][46] S ohledem na tyto znalosti vědci podávali deseti ženám 400 μg pikolinátu chromitého denně po dobu osmi týdnů.[44] Měřením množství oxidovaného páru bází DNA pomocí 5-hydroxymethyluracilu titry protilátek mohla skupina odvodit množství oxidace párů bází DNA, ke kterému dochází v přímé souvislosti s pikolinátem chromitým.[44] Výsledky studie naznačují, že samotný pikolinát chromitý nezpůsobuje významné poškození chromozomů in vivo.[44]
Obecně lze říci, že se ukázalo, že pikolinát chromitý není pro člověka toxický. U většiny dospělých může být užíván perorálně v dávkách až 1000 μg denně.[47] Tato nízká toxicita byla obecně spojena s nízkou absorpcí Cr (III) v těle prostřednictvím plíce, kůže a gastrointestinální trakt,[48] spolu s vysokým vylučováním. Normálně lze 99% odebraného chrómu (III) obnovit ve stolici uživatele. Existují ojedinělé případy doplňování chrómu (III) vedoucí k selhání ledvin, avšak tento vztah je nejasný a musí být ještě testován.[49]
Regulace pikolinátu chromitého
V roce 2004 agentura UK Food Standards Agency doporučila spotřebitelům, aby přednostně před pikolinátem chromitým (III) používali jiné formy trojmocného chromu, dokud nedostane odbornou radu od Výboru pro mutagenitu. Důvodem byly obavy vyvolané skupinou odborníků pro vitamíny a minerály, že pikolinát chromitý může být genotoxický (způsobit rakovinu). Výbor také vzal na vědomí dvě případové zprávy z selhání ledvin který by mohl být způsoben tímto doplňkem a vyžadoval další výzkum jeho bezpečnosti.[50][51] V prosinci 2004 zveřejnil Výbor pro mutagenitu svá zjištění, která dospěla k závěru, že „celkově lze dospět k závěru, že bilance údajů naznačuje, že pikolinát chromitý by měl být považován za mutagenní in vitro“ a že „dostupné v -vivo testy na savcích s pikolinátem chromitým jsou negativní “.[52] Na základě těchto zjištění UK Food Standards Agency stáhla své doporučení, aby se zabránilo pikolinátu chrómu (III), i když plánuje své rady týkající se doplňků chrómu přezkoumávat.[53]
V roce 2010 byl společností Health Canada schválen pikolinát chromitý pro použití v doplňcích stravy. Mezi schválená prohlášení na etiketě patří: faktor udržující dobré zdraví, poskytuje podporu zdravému metabolismu glukózy, pomáhá tělu metabolizovat sacharidy a pomáhá tělu metabolizovat tuky.[54]
Reference
- ^ Preuss, H. G .; Echard, B .; Perricone, N. V .; Bagchi, D .; Yasmin, T .; Stohs, S. J. (2008). "Srovnání metabolických účinků šesti různých komerčních sloučenin trojmocného chrómu". Journal of Anorganic Biochemistry. 102 (11): 1986–1990. doi:10.1016 / j.jinorgbio.2008.07.012. PMID 18774175.
- ^ Recenze Chromium Archivováno 7. února 2012 na adrese Wayback Machine Expertní skupina pro přezkum chromu na vitamíny a minerály, 12. srpna 2002
- ^ Stearns DM (2000). „Je chrom stopový esenciální kov?“. Biofaktory. 11 (3): 149–62. doi:10.1002 / biof.5520110301. PMID 10875302. S2CID 19417496.
- ^ A b C d Vincent, John (2010). „Chrom: slaví 50 let jako zásadní prvek?“. Daltonské transakce. 39 (16): 3787–3794. doi:10.1039 / B920480F. PMID 20372701.
- ^ A b Tian, H; Guo, X; Wang, X; On, Z; Sun, R; Ge, S; Zhang, Z (2013). „Doplněk pikolinátu chromitého pro dospělé s nadváhou nebo obezitou“. Cochrane Database of Systematic Reviews. 11 (11): CD010063. doi:10.1002 / 14651858.CD010063.pub2. PMC 7433292. PMID 24293292. CD010063.
- ^ A b C d Levina, Aviva; Lay, Peter (2008). "Chemické vlastnosti a toxicita doplňků výživy pro chrom (III)". Chemický výzkum v toxikologii. 21 (3): 563–571. doi:10.1021 / tx700385t. PMID 18237145.
- ^ A b C d E F G h i Feng, Weiyue (2007). „Kapitola 6 - Transport chromu (III) v těle: důsledky pro funkci“ (PDF). V Vincent, John (ed.). Nutriční biochemie chromu (III). Amsterdam: Elsevier B.V. s. 121–137. ISBN 978-0-444-53071-4. Citováno 20. března 2015.
- ^ A b Cefalu, William; Hu, Frank (2004). „Role chromu v lidském zdraví a při cukrovce“. Péče o cukrovku. 27 (11): 2741–2751. doi:10.2337 / diacare.27.11.2741. PMID 15505017. Citováno 20. března 2015.
- ^ A b C d E F Anderson, Richard (1998). „Chrom, intolerance glukózy a cukrovka“. Journal of the American College of Nutrition. 17 (6): 548–555. doi:10.1080/07315724.1998.10718802. PMID 9853533.
- ^ A b C d Vincent, John (2004). „Nedávný pokrok v nutriční biochemii trojmocného chromu“. Sborník Výživové společnosti. 63 (1): 41–47. doi:10.1079 / PNS2003315. PMID 15070438.
- ^ A b C d E Vincent, John (2001). „The Bioinorganic Chemistry of Chromium (III)“. Mnohostěn. 20 (1–2): 1–26. doi:10.1016 / S0277-5387 (00) 00624-0.
- ^ A b C Abou – Gamra, Zeinab; Abdel – Messih, Michel (2014). "Korelace tepelných a spektrálních vlastností komplexu pikolinátu chromitého a kinetická studie jeho tepelné degradace". Journal of Thermal Analysis and Calorimetry. 117 (2): 993–1000. doi:10.1007 / s10973-014-3768-5. S2CID 93050541.
- ^ A b C d E Parajón – Costa, Beatriz; Wagner, Claudia; Baran, Enrique (2003). "Voltametrická a spektroskopická studie komplexů chrom (III) / pikolinát". Zeitschrift für Anorganische und Allgemeine Chemie. 629 (6): 1085–1090. doi:10.1002 / zaac.200300050.
- ^ A b C Stearns, Diane; Armstrong, William (1992). "Mononukleární a dvoujaderné komplexy chrómu (III) pikolinátu". Anorganická chemie. 31 (25): 5178–5184. doi:10.1021 / ic00051a007.
- ^ A b C d Hakimi, Mohammad (2013). „Strukturální a spektrální charakterizace komplexu pikolinátu chromitého (III): Představujeme novou redoxní reakci“. Journal of the Korean Chemical Society. 57 (6): 721–725. doi:10,5012 / jkcs.2013.57.6.721. Citováno 1. dubna 2015.
- ^ A b Lukaski, Henry (2007). „Kapitola 4 - Účinky chromu (III) jako doplňku výživy“ (PDF). V Vincent, John (ed.). Nutriční biochemie chromu (III). Amsterdam: Elsevier B.V. s. 57–70. ISBN 978-0-444-53071-4. Citováno 20. března 2015.
- ^ A b C Laschinsky, Niels; Kottwitz, Karin; Freund, Barbara; Dresow, bernd; Fischer, Roland; Nielsen, Peter (2012). "Biologická dostupnost doplňků chrómu u potkanů a lidí". BioMetals. 25 (5): 1051–1060. doi:10.1007 / s10534-012-9571-5. PMID 22814636. S2CID 1533593.
- ^ A b C d E F G Debski, B .; Goniewicz, M .; Krzyzowskal, M .; Lewicka, A .; Lewickil, S .; Niemcewiz, M .; Zdanowskil, R. (2014). „Úloha chromu III v organismu a jeho možné využití při léčbě cukrovky a obezity“. Annals of Agricultural and Environmental Medicine. 21 (2): 331–335. doi:10.5604/1232-1966.1108599. PMID 24959784.
- ^ A b C d E F G h Vincent, John (2015). „Je farmakologický způsob působení chromu (III) jako sekundárního posla?“. Výzkum biologických stopových prvků. 166 (1): 7–12. doi:10.1007 / s12011-015-0231-9. PMID 25595680. S2CID 16895342.
- ^ A b C d E F Quarles, C .; Marcus, R .; Brumaghim, Julia (2011). „Konkurenční vazba Fe3+, Cr3+a Ni2+ převést ". Journal of Biological Anorganic Chemistry. 16 (6): 913–921. doi:10.1007 / s00775-011-0792-9. PMID 21678080. S2CID 24302252.
- ^ A b Vincent, John (2012). "Vazba a transport alternativních kovů transferinem". Biochimica et Biophysica Acta (BBA) - Obecné předměty. 1820 (3): 362–378. doi:10.1016 / j.bbagen.2011.07.003. PMID 21782896.
- ^ Levina, Aviva; Pham, T. H. Nguyen; Lay, Peter A. (2016-05-01). „Vazba chromu (III) na transferin může být součástí detoxikace dietního chromu (III) spíše než transportu esenciálního stopového prvku“. Angewandte Chemie International Edition. 55 (28): 8104–8107. doi:10,1002 / anie.201602996. ISSN 1521-3773. PMID 27197571.
- ^ A b C d E F G Vincent, John (2012). "Biochemické mechanismy". V Vincent, John (ed.). Bioanorganická chemie chromu. Chichester, Velká Británie: John Wiley & Sons. 125–167. doi:10.1002 / 9781118458891.ch6. ISBN 9780470664827.
- ^ Viera M, Davis-McGibony CM (2008). „Izolace a charakterizace nízkomolekulární látky vázající chrom (LMWCr) z kuřecích jater“. Protein J.. 27 (6): 371–5. doi:10.1007 / s10930-008-9146-z. PMID 18769887. S2CID 32564084.
- ^ A b C d Vincent, John (2000). „The Biochemistry of Chromium“. The Journal of Nutrition. 130 (4): 715–718. doi:10.1093 / jn / 130.4.715. PMID 10736319.
- ^ Clodfelder BJ, Emamaullee J, Hepburn DD, Chakov NE, Nettles HS, Vincent JB (2001). „Stezka chrómu (III) in vivo z krve do moči: role transferinu a chromodulinu“. J. Biol. Inorg. Chem. 6 (5–6): 608–17. doi:10,1007 / s007750100238. PMID 11472024. S2CID 8956685.
- ^ Vincent JB (1994). „Vztah mezi faktorem tolerance glukózy a látkou vázající chrom s nízkou molekulovou hmotností“ (PDF). J. Nutr. 124 (1): 117–9. doi:10.1093 / jn / 124.1.117. PMID 8283288.
- ^ A b C d Kitamura, Masanori (2008). „Stres endoplazmatického retikula a rozvinutá proteinová odpověď v renální patofyziologii: Janusovy tváře“. American Journal of Physiology. 295 (2): 323–334. doi:10.1152 / ajprenal.00050.2008. PMID 18367660.
- ^ A b C d E Hua, Yinan; Clark, Suzanne; Ren, červen; Sreejayan, Nair (2012). "Molekulární mechanismy chromu při snižování inzulínové rezistence". Journal of Nutritional Biochemistry. 23 (4): 313–319. doi:10.1016 / j.jnutbio.2011.11.001. PMC 3308119. PMID 22423897.
- ^ A b C Tonksová, Nicholas (2003). "PTP1B: Od okraje k přední linii!". FEBS Dopisy. 546 (1): 140–148. doi:10.1016 / S0014-5793 (03) 00603-3. PMID 12829250. S2CID 21205538.
- ^ Levina, Aviva (2011). „Antidiabetické léky na bázi kovů: pokroky a výzvy“. Daltonské transakce. 40 (44): 11675–1686. doi:10.1039 / C1DT10380F. PMID 21750828.
- ^ Vincent J.B .; Pytel, DA; Roffman, M; Finch, M; Komorowski, JR (2003). „Potenciální hodnota a toxicita pikolinátu chromitého jako doplňku výživy, látky pro hubnutí a látky pro vývoj svalů“. Sportovní medicína. 33 (3): 213–230. doi:10.2165/00007256-200333030-00004. PMID 12656641. S2CID 9981172.
- ^ „Vědecké stanovisko k odůvodnění zdravotních tvrzení týkajících se chrómu a příspěvku k normálnímu metabolismu makroživin (ID 260, 401, 4665, 4666, 4667), udržování normální koncentrace glukózy v krvi (ID 262, 4667), příspěvek k udržení nebo dosažení výsledků normální tělesné hmotnosti (ID 339, 4665, 4666) a snížení únavy a únavy (ID 261) podle čl. 13 odst. 1 nařízení (ES) č. 1924/2006 ". Deník EFSA. 8 (10). 2010. doi:10.2903 / j.efsa.2010.1732.
- ^ Althuis MD, Jordan NE, Ludington EA, Wittes JT (1. července 2002). „Reakce glukózy a inzulínu na doplňky chrómu: metaanalýza“. American Journal of Clinical Nutrition. 76 (1): 148–155. doi:10.1093 / ajcn / 76.1.148. PMID 12081828.
- ^ A b C Balk EM, Tatsioni A, Lichtenstein AH, Lau J, Pittas AG (2007). „Vliv suplementace chrómu na metabolismus glukózy a lipidů: systematický přehled randomizovaných kontrolovaných studií“. Péče o cukrovku. 30 (8): 2154–2163. doi:10.2337 / dc06-0996. PMID 17519436.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Suksomboon, N .; Poolsup, N .; Yuwanakom, A. (2014). „Systematický přehled a metaanalýza účinnosti a bezpečnosti doplňování chrómu při cukrovce“. Journal of Clinical Pharmacy and Therapeutics. 39 (3): 292–306. doi:10.1111 / jcpt.12147. PMID 24635480.
- ^ Broadhurst CL, Domenico P (prosinec 2006). „Klinické studie o doplňování chrom pikolinátu u diabetes mellitus - přehled“. Diabetes Technol. Ther. 8 (6): 677–87. doi:10.1089 / dia.2006.8.677. PMID 17109600.
- ^ Kvalifikovaná zdravotní tvrzení: Rozhodnutí o prosazování - pikolinát chromitý a inzulínová rezistence (dok. Č. 2004Q-0144) (2005) U.S. Food and Drug Administration.
- ^ Trumbo PR, Ellwood KC (srpen 2006). „Příjem pikolinátu chromitého a riziko diabetu 2. typu: důkazní zpráva Spojených států pro kontrolu potravin a léčiv“. Nutr. Rev. 64 (8): 357–63. doi:10.1111 / j.1753-4887.2006.tb00220.x. PMID 16958312.
- ^ Chaudhary S, Pinkston J, Rabile MM, Van Horn JD (2005). „Neobvyklá reaktivita v komerčním doplňku chrómu ve srovnání se základním štěpením DNA syntetickými komplexy chrómu“. Journal of Anorganic Biochemistry. 99 (3): 787–794. doi:10.1016 / j.jinorgbio.2004.12.009. PMID 15708800.
- ^ Hininger I, Benaraba R, Osman M, Faure H, Marie Roussel A, Anderson RA (2007). „Bezpečnost komplexů trojmocného chrómu: žádné důkazy o poškození DNA v lidských HaCaT keratinocytech“. Volný radikál. Biol. Med. 42 (12): 1759–65. doi:10.1016 / j.freeradbiomed.2007.02.034. PMID 17512455.
- ^ Stallings DM, Hepburn DD, Hannah M, Vincent JB, O'Donnell J (2006). „Doplněk výživy pikolinát chromitý generuje chromozomální aberace a brání vývoji potomstva v Drosophila melanogaster“. Mutat. Res. 610 (1–2): 101–13. doi:10.1016 / j.mrgentox.2006.06.019. PMID 16887379.
- ^ Hepburn DD, Xiao J, Bindom S, Vincent JB, O'Donnell J (2003). „Doplněk výživy pikolinát chromitý způsobuje sterilitu a smrtící mutace v Drosophila melanogaster“. Proc. Natl. Acad. Sci. USA. 100 (7): 3766–71. doi:10.1073 / pnas.0636646100. PMC 152996. PMID 12649323.
- ^ A b C d E Kato, Ikuko; Vogelman, Joseph; Dilman, Vladimir; Karkoszka, Jerzy; Frenkel, Krystyna; Durr, Nancy; Orentreich, Norman; Toniolo, Paolo (1998). "Účinek suplementace pikolinátem chromitým na titry protilátek proti 5-hydroxymethyluracilu". European Journal of Epidemiology. 14 (6): 621–626. doi:10.1023 / A: 1007442203258. PMID 9794131. S2CID 19071972.
- ^ Tsou, Tsui - Chun; Chen, Chiu-lan; Liu, Tsung - Yun; Yang, Jia-Ling (1996). „Indukce 8-hydroxydeoxyguanosinu v DNA chromem (III) plus peroxid vodíku a jeho prevence pomocí lapačů“ (PDF). Karcinogeneze. 17 (1): 103–108. doi:10.1093 / carcin / 17.1.103. PMID 8565117. Citováno 20. března 2015.
- ^ Ozawa, T .; Hanaki, A. (1990). „Studie zachycující odstřeďování reakcí Cr (III) s peroxidem vodíku v přítomnosti biologických redukčních látek: je Cr (III) netoxický?“. Biochemistry International. 22 (2): 343–352. PMID 1965278.
- ^ Jeejeebhoy, Khursheed (2009). „Role chromu ve výživě a terapii a jako potenciální toxin“. Recenze výživy. 57 (11): 329–335. doi:10.1111 / j.1753-4887.1999.tb06909.x. PMID 10628183.
- ^ Fairhurst, S .; Minty, C. (1989). Toxicita chrómu a anorganických sloučenin chrómu. Přehled toxicity; 21. Londýn: H.M.S.O. s. 1–243. ISBN 9780118855211.
- ^ Wasser, Walter; Feldman, Nathaniel; D'Agati, Vivette (1997). „Chronické selhání ledvin po požití pikolinátu chromitého na přepážku“. Annals of Internal Medicine. 126 (5): 410. doi:10.7326/0003-4819-126-5-199703010-00019. PMID 9054292. S2CID 27418296.
- ^ Bezpečné horní úrovně pro vitamíny a minerály Archivováno 2008-07-04 na Wayback Machine Food Standards Agency - květen 2003
- ^ Hodnocení rizika: Chrom Expertní skupina pro vitamíny a minerály, 2003
- ^ PROHLÁŠENÍ O MUTAGENICI TRIVALENTNÍHO CHROMU A PICOLINÁTU CHROMU Archivováno 16. května 2008 v Wayback Machine KOM / 04 / S3 - prosinec 2004
- ^ Agentura reviduje doporučení pikolinátu chromitého Agentura pro potravinové normy - 13. prosince 2004
- ^ „Monografie: Chrom (z chrom pikolinátu)“. Health Canada. 9. prosince 2009. Citováno 24. března 2015.
externí odkazy
 Média související s Pikolinát chromitý na Wikimedia Commons
Média související s Pikolinát chromitý na Wikimedia Commons- Příručka společnosti Merck


