Benzil - Benzil
 | |
 | |
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC Difenylethanedion | |
| Systematický název IUPAC 1,2-difenylethan-1,2-dion | |
| Ostatní jména Difenylethan-1,2-dion Benzil Dibenzoyl Bibenzoyl Difenylglyoxal | |
| Identifikátory | |
3D model (JSmol ) | |
| 608047 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.004.689 |
| Číslo ES |
|
PubChem CID | |
| Číslo RTECS |
|
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C14H10Ó2 | |
| Molární hmotnost | 210.232 g · mol−1 |
| Vzhled | žlutý krystalický prášek |
| Hustota | 1,23 g / cm3, pevná látka (1,255 g / cm3, rentgen) |
| Bod tání | 94,0 až 96,0 ° C; 201,2 až 204,8 ° F; 367,1 až 369,2 K. |
| Bod varu | 346,0 až 348,0 ° C; 654,8 až 658,4 ° F; 619,1 až 621,1 K. |
| nerozpustný | |
| Rozpustnost v ethanol | rozpustný |
| Rozpustnost v diethylether | rozpustný |
| Rozpustnost v benzen | rozpustný |
| -118.6·10−6 cm3/ mol | |
| Struktura | |
| P31,221[1] | |
| 3.8 D[2] | |
| Nebezpečí | |
| Hlavní nebezpečí | Dráždivý |
| Piktogramy GHS |  |
| Signální slovo GHS | Varování |
| H315, H319, H335 | |
| P261, P264, P271, P280, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P403 + 233, P405, P501 | |
| NFPA 704 (ohnivý diamant) | |
| Související sloučeniny | |
Příbuzný diketony | biacetyl |
Související sloučeniny | benzofenon glyoxal bibenzil |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
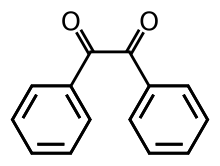
Benzil (systematicky známý jako 1,2-difenylethan-1,2-dion) je organická sloučenina se vzorcem (C6H5CO )2, obecně zkráceně (Ph CO)2. Tato žlutá pevná látka je jednou z nejběžnějších diketony. Jeho hlavní použití je jako fotoiniciátor v polymerní chemie.[3]
Struktura
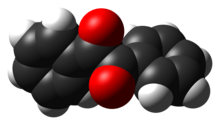
Nejpozoruhodnějším strukturálním rysem sloučeniny je dlouhá vazba uhlík-uhlík 1,54 A, což naznačuje absenci vazby pí mezi dvěma karbonylovými centry. Centra PhCO jsou planární, ale dvojice benzoylových skupin je zkroucená vzhledem k druhé s a vzepětí úhel 117 °.[4] Méně bráněno analogy (glyoxal, biacetyl, kyselina šťavelová deriváty), (RCO)2 skupina přijímá rovinnou antikonformaci.
Aplikace
Většina benzilu se používá ve volných radikálech vytvrzování z polymer sítí. Ultrafialový záření rozkládá benzil a vytváří v materiálu radikály, které podporují tvorbu křížové odkazy. Benzil je silný lidský inhibitor karboxylesterázy, enzymy podílející se na hydrolýze karboxylesterů a mnoho klinicky používaných léků.[5]
Benzil je relativně špatný fotoiniciátor a používá se zřídka. Absorbuje při vlnové délce 260 nm. Prochází fotobělení, což umožňuje vytvrzujícímu světlu dosáhnout při delší expozici hlubších vrstev materiálu.[6]
Reakce
Benzil je standardní stavební blok v organická syntéza. Kondenzuje s aminy diketimin ligandy. Klasika organická reakce benzilu je přesmyk kyseliny benzolové, ve kterém báze katalyzuje přeměnu benzilu na kyselinu benzilovou. Tato reaktivita se využívá při přípravě léčiva fenytoin. Benzil také reaguje s 1,3-difenylaceton v kondenzace aldolu dát tetrafenylcyklopentadienon.
Příprava
Benzil se připravuje z benzoin, například s octan měďnatý:[7]
- PhC (O) CH (OH) Ph + 2 Cu2+ → PhC (O) C (O) Ph + 2 H+ + 2 Cu+
Další vhodná oxidační činidla, jako např kyselina dusičná (HNO3) se běžně používají.
Chlorid železitý (FeCl3) lze použít jako levný katalyzátor pro tuto chemickou konverzi.[8]
Reference
- ^ Acta Crystallogr. B43 398 (1987)
- ^ Spectrochim. Acta A60 (8-9) 1805 (2004)
- ^ Hardo Siegel, Manfred Eggersdorfer „Ketones“ v Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, 2002, Wiley-VCH, Weinheim. doi:10.1002 / 14356007.a15_077
- ^ Quang. Shen, Kolbjoern. Hagen „Molekulární struktura a konformace benzilu v plynné fázi, jak je stanoveno elektronovou difrakcí“ J. Phys. Chem., 1987, 91 (6), str. 1357–1360. doi:10.1021 / j100290a017.
- ^ Wadkins. R. M. a kol. "Identifikace a charakterizace nových benzil (difenylethan-1,2-dionu) analog jako inhibitorů savčích karboxylesteráz. J. Med. Chem., 2005 48 str. 2906–15.
- ^ Arthur Green, W. (2010-04-22). Průmyslové fotoiniciátory: Technický průvodce. ISBN 9781439827468.
- ^ Depreux, P .; Bethegnies, G .; Marcincal-Lefebvre, A. (1988). "Syntéza benzilu z benzoinu s octanem měďnatým". Journal of Chemical Education. 65 (6): 553. Bibcode:1988JChEd..65..553D. doi:10.1021 / ed065p553.
- ^ Bi, Xiaoxin; Wu, Lintao; Yan, Chaoguo; Jing, Xiaobi; Zhu, Hongxiang (2011). „One-Pot Synthesis Benzils from Aldehydes via Nhc-Catalyzed Benzoin Dimerization Under-Metal-Free Conditions in Water“. Journal of the Chilean Chemical Society. 56 (2): 663. doi:10.4067 / S0717-97072011000200008.

