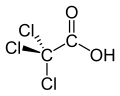
Kyselina trichloroctová - Trichloroacetic acid
| |||
 | |||
| Jména | |||
|---|---|---|---|
| Název IUPAC Kyselina trichloroctová | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChEMBL | |||
| ChemSpider | |||
| Informační karta ECHA | 100.000.844 | ||
| KEGG | |||
PubChem CID | |||
| Číslo RTECS |
| ||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C2HCl3Ó2 | |||
| Molární hmotnost | 163.38 g · mol−1 | ||
| Vzhled | Bezbarvá až bílá krystalická pevná látka | ||
| Zápach | ostrý, štiplavý [1] | ||
| Hustota | 1,63 g / cm3 | ||
| Bod tání | 57 až 58 ° C (135 až 136 ° F; 330 až 331 K)[2] | ||
| Bod varu | 196 až 197 ° C (385 až 387 ° F; 469 až 470 K)[2] | ||
| 1000 g / 100 ml[2] | |||
| Tlak páry | 1 mmHg (51,1 ° C)[1] | ||
| Kyselost (strK.A) | 0.66[3] | ||
| -73.0·10−6 cm3/ mol | |||
| Struktura | |||
| 3.23 D | |||
| Nebezpečí | |||
Klasifikace EU (DSD) (zastaralý) | Žíravý (C) Nebezpečný pro prostředí (N) | ||
| R-věty (zastaralý) | R35, R50 / 53 | ||
| S-věty (zastaralý) | (S1 / 2), S26, S36 / 37/39, S45, S60, S61 | ||
| NFPA 704 (ohnivý diamant) | |||
| Smrtelná dávka nebo koncentrace (LD, LC): | |||
LD50 (střední dávka ) | 5000 mg / kg orálně u potkanů[2] | ||
| NIOSH (Limity expozice USA pro zdraví): | |||
PEL (Dovolený) | žádný[1] | ||
REL (Doporučeno) | TWA 1 ppm (7 mg / m3)[1] | ||
IDLH (Okamžité nebezpečí) | N.D.[1] | ||
| Související sloučeniny | |||
Příbuzný kyseliny chloroctové | Kyselina chloroctová Kyselina dichloroctová | ||
Související sloučeniny | Octová kyselina Kyselina trifluoroctová Kyselina tribromoctová | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Kyselina trichloroctová (TCA; TCAA; také známý jako kyselina trichlorethanová) je obdobou octová kyselina ve kterém tři vodík atomy methyl všechny skupiny byly nahrazeny chlór atomy. Solí a estery kyseliny trichloroctové trichloracetáty.
Syntéza
Připravuje se reakcí chloru s octová kyselina v přítomnosti vhodného katalyzátor.
- CH
3COOH + 3Cl
2 → CCl
3COOH +3HCl
Další cestou k kyselině trichloroctové je oxidace trichloracetaldehydu.
Použití
Je široce používán v biochemie pro srážení makromolekul, jako je bílkoviny, DNA, a RNA. TCA a DCA se oba používají při kosmetických ošetřeních (např chemický peeling a odstranění tetování ) a jako lokální léky pro chemoablaci bradavice, počítaje v to genitální bradavice. Může také zabít normální buňky. Používání k tomuto účelu během těhotenství se považuje za bezpečné.[4][5]
Své sodík sůl byl použit jako herbicid počínaje padesátými lety, ale regulační orgány ji stáhly z trhu na konci 80. a na začátku 90. let.[6][7][8][9]
Dějiny
Objev kyseliny trichloroctové v Jean-Baptiste Dumas v roce 1839 poskytl pozoruhodný příklad pomalu se rozvíjející teorii organických radikálů a valencí.[10] Tato teorie byla v rozporu s vírou Jöns Jakob Berzelius, který zahájil dlouhý spor mezi Dumasem a Berzeliusem.[11]
Viz také
Reference
- ^ A b C d E NIOSH Kapesní průvodce chemickými nebezpečími # 0626Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH)
- ^ A b C d Budavari, Susan, ed. (1996), Merck Index: Encyclopedia of Chemicals, Drugs, and Biologicals (12. vydání), Merck, ISBN 0911910123
- ^ Databog fysik kemi, F&K Forlaget 11. udgave 2009
- ^ "Kyselina trichloroctová nebo kyselina bichloroctová pro genitální bradavice (lidský papilomavirus)". WebMD.
- ^ Wiley DJ, Douglas J, Beutner K, Cox T, Fife K, Moscicki AB, Fukumoto L (2002). „Vnější genitální bradavice: diagnostika, léčba a prevence“. Klinické infekční nemoci. 35 (Suppl 2): S210 – S224. doi:10.1086/342109. PMID 12353208.
- ^ TCA-sodík v Pesticide Properties DataBase (PPDB), accessed June 20, 2014
- ^ G. S. Rai a C. L. Hamner Perzistence trichloracetátu sodného v různých typech půdy Weeds 2 (4) Oct.1953: 271-279
- ^ OECD Kyselina trichloroctová CAS č.: 76-03-9 Zpřístupněno 20. června 2014
- ^ EPA prosinec 1991. Kyselina trichloroctová (TCA) EPA Zrušení 12/91 Zpřístupněno 20. června 2014
- ^ Dumas (1839). "Kyselina trichloroctová". Annalen der Pharmacie. 32: 101–119. doi:10,1002 / jlac.18390320109.
- ^ William Albert Noyes (1927). "Mocenství". Sborník americké filozofické společnosti. 66: 287–308. JSTOR 3301070.