Indene - Indene
 | |
 | |
| Jména | |
|---|---|
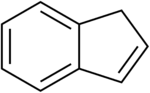
| Preferovaný název IUPAC 1H-Indene | |
| Systematický název IUPAC Bicyklo [4.3.0] nona-l, 3,5,7-tetraen | |
| Ostatní jména Benzocyklopentadien Indonaphthene | |
| Identifikátory | |
3D model (JSmol ) | |
| 635873 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Informační karta ECHA | 100.002.176 |
| 27265 | |
| KEGG | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C9H8 | |
| Molární hmotnost | 116.16 |
| Vzhled | Bezbarvá kapalina[1] |
| Hustota | 0,997 g / ml |
| Bod tání | -1,8 ° C (28,8 ° F; 271,3 K) |
| Bod varu | 181,6 ° C (358,9 ° F; 454,8 K) |
| Nerozpustný | |
| Kyselost (strK.A) | 20,1 (v DMSO)[2] |
| −80.89×10−6 cm3/ mol | |
| Nebezpečí | |
| Hlavní nebezpečí | Hořlavý |
| Bod vzplanutí | 78,3 ° C (172,9 ° F; 351,4 K) |
| NIOSH (Limity expozice USA zdraví): | |
PEL (Dovolený) | žádný[1] |
REL (Doporučeno) | TWA 10 ppm (45 mg / m3)[1] |
IDLH (Okamžité nebezpečí) | N.D.[1] |
| Související sloučeniny | |
Související sloučeniny | Benzofuran, Benzothiofen, Indole |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Indene je hořlavý polycyklický uhlovodík s chemický vzorec C9H8. Skládá se z a benzen prsten fúzovaný s a cyklopenten prsten. Tato aromatická kapalina je bezbarvá, i když vzorky jsou často světle žluté. Hlavní průmyslové využití indenu je ve výrobě indenu /kumaron termoplastické pryskyřice. Substituované indeny a jejich úzce související indane deriváty jsou důležité strukturální motivy nalezené v mnoha přírodní produkty a biologicky aktivní molekuly, jako např sulindac.[3]
Izolace
Inden se přirozeně vyskytuje v uhelný dehet zlomky vroucí kolem 175–185 ° C. Lze jej získat zahřátím této frakce s sodík k vysrážení pevného "sodno-indenu". Tento krok využívá slabou kyselost indenu, o čemž svědčí jeho deprotonace sodíkem, čímž se získá indenylový derivát. Sodio-inden se parou převede zpět na inden destilace.[4]
Reaktivita
Indene snadno polymerizuje. Oxidace indenu kyselinou dichroman výnosy kyselina homoftalová (Ó-karboxylfenyloctová kyselina). Kondenzuje se diethylem šťavelan v přítomnosti ethoxid sodný za vzniku inden-oxalového esteru a s aldehydy nebo ketony v přítomnosti alkálie tvořit benzofulvenes, které jsou vysoce barevné. Léčba indenu pomocí organolithium činidla dávají lithium indenyl sloučeniny:
- C9H8 + RLi → LiC9H7 + RH
Indenyl je a ligand v organokovová chemie, což vede k mnoha indenylové komplexy přechodových kovů.[5]
Viz také
Reference
- ^ A b C d NIOSH Kapesní průvodce chemickými nebezpečími. "#0340". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ Bordwell FG (1988). "Rovnovážné kyselosti v roztoku dimethylsulfoxidu". Účty chemického výzkumu. 21 (12): 456–463. doi:10.1021 / ar00156a004.Tabulka Bordwell pKa v DMSO Archivováno 2008-10-09 na Wayback Machine
- ^ Wu, Jie; Qiu, Guanyinsheng (2014). "Generování indenových derivátů tandemovými reakcemi". Synlett. 25 (19): 2703–2713. doi:10.1055 / s-0034-1379318.
- ^ Collin, Gerd; Mildenberg, Rolf; Zander, Mechthild; Höke, Hartmut; McKillip, William; Freitag, Werner; Imöhl, Wolfgang. "Pryskyřice, syntetické". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH.
- ^ O'Connor, Joseph M .; Casey, Charles P. (1987). "Ring-Slippage Chemistry of Transition Metal Cyclopentadienyl and Indenyl Complexes". Chemické recenze. 87 (2): 307–318. doi:10.1021 / cr00078a002.
externí odkazy
- Miller, Rohde (1890). „Zur Synthese von Indenderivaten“. Berichte der Deutschen Chemischen Gesellschaft. 23 (2): 1881–1886. doi:10.1002 / cber.18900230227.
- Miller, Rohde (1890). „Zur Synthese von Indenderivaten“. Berichte der Deutschen Chemischen Gesellschaft. 23 (2): 1887–1902. doi:10.1002 / cber.18900230228.
- Finar, I.L. (1985). Organická chemie. Longman Scientific & Technical. ISBN 0-582-44257-5.
