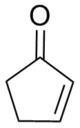
Cyklopentenon - Cyclopentenone
| |||
| Jména | |||
|---|---|---|---|
| Název IUPAC 2-cyklopenten-1-on | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Informační karta ECHA | 100.012.012 | ||
PubChem CID | |||
| UNII | |||
| |||
| |||
| Vlastnosti | |||
| C5H6Ó | |||
| Molární hmotnost | 82,04 g · mol−1 | ||
| Hustota | 0,98 g · ml−1 | ||
| Bod varu | 150 ° C (302 ° F; 423 K) | ||
| téměř nerozpustný v voda | |||
| Nebezpečí | |||
| Hlavní nebezpečí | Škodlivý | ||
| Bod vzplanutí | 42 ° C (108 ° F; 315 K) | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
2-cyklopentenon je keton s chemický vzorec C5H6Ó a Číslo CAS 930-30-3. Je strukturálně podobný cyklopentanon, s další funkcí nenasycení α-β v kruhovém systému. 2-Cyklopentenon obsahuje dvě funkční skupiny, keton a alken. Je to bezbarvá kapalina.
Termín cyklopentenon může také označovat a strukturální motiv kde cyklopentenon skupina je podjednotka větší molekuly. Cyklopentenony se nacházejí ve velkém počtu přírodní produkty, počítaje v to jasmón, aflatoxiny a několik prostaglandiny.
Syntéza
2-Cyklopentenony lze syntetizovat mnoha způsoby. Jedna z cest zahrnuje eliminaci α-brom -cyklopentanon použitím uhličitan lithný[1] a Claisenova kondenzace -dekarboxylace -izomerizace kaskády nenasycených diestery Jak je ukázáno níže.[2]

Kyselinou katalyzovaná dehydratace cyklopentandiolů poskytuje cyklopentenon.[3]
Jako funkční skupina se syntéza 2-cyklopentenonů provádí řadou dalších způsobů, včetně Nazarovova cyklizační reakce z divinylketonů, Oxidace Saegusa – Ito z cyklopentanony, metatéza zavírání prstenů z odpovídajících dienes, oxidace odpovídající cyklické allylalkoholy a Pauson-Khandova reakce z alkeny, alkyny, a kysličník uhelnatý.[4]
Reakce
Jako enone 2-cyklopentenon prochází typickými reakcemi α-β nenasycených ketonů, včetně přidání nukleofilního konjugátu, Baylis-Hillmanova reakce a Michaelova reakce. Cyklopentenon také funguje jako vynikající dienophile v Diels-Alderova reakce, reagující s širokou paletou dienes. V jednom příkladu a Dien typu Danishefsky reaguje s cyklopentenonem za vzniku kondenzovaného tricyklického systému na cestě k syntéze koriolinu.[5]

Výskyt
Byl izolován z vepřového masa vařeného v tlaku játra současnou párou destilace a kontinuální extrakce rozpouštědlem.[6]
Reference
- ^ US EP1418166 „Daisuke, Fukushima & Hirata Norihiko,„ Proces výroby 2-bromcyklopentanonu “, zveřejněno 12. 5. 2004
- ^ US EP1422212, Liang, Shelue; Andrea Haunert a Sylvia Huber-Dirr a kol., „Proces přípravy cyklopentenonu“, publikováno 25. 11. 2004
- ^ Charles H. DePuy a K.L. Eilers (1962). „2-cyklopentenon“. Org. Synth. 42: 38. doi:10.15227 / orgsyn.042.0038.CS1 maint: používá parametr autoři (odkaz)
- ^ Müller, Reto. "Syntéza cyklopentenonů". Portál organické chemie. Citováno 3. března 2015.
- ^ Danishefsky, Samuel; Zamboni, Robert; Kahn, Michael; Etheredge, Sarah Jane (březen 1980). "Celková syntéza dl-coriolinu". Journal of the American Chemical Society. 102 (6): 2097–2098. doi:10.1021 / ja00526a061.
- ^ Mussinan, Cynthia J .; Walradt, John P. (květen 1974). "Těkavé složky tlakově vařených vepřových jater". Journal of Agricultural and Food Chemistry. 22 (5): 827–831. doi:10.1021 / jf60195a002.