Molekuly uvolňující oxid uhelnatý - Carbon monoxide-releasing molecules - Wikipedia
Molekuly uvolňující oxid uhelnatý (CORMs) jsou chemické sloučeniny určené k uvolňování kontrolovaného množství kysličník uhelnatý (CO). CORM se vyvíjejí jako potenciální terapeutická činidla pro místní dodávání CO do buněk a tkání, čímž překonávají omezení protokolů inhalace plynů CO.[1]
CO je nejlépe známý svou toxicitou v otrava oxidem uhelnatým při vysokých dávkách. CO však patří mezi endogenní plynné signální molekuly a nízké dávkování CO bylo spojeno s terapeutickými přínosy. Předklinický výzkum se zaměřil na CO protizánětlivý aktivita s významnými aplikacemi v kardiovaskulárních chorobách, onkologii, transplantační chirurgii a neuroprotekci.[2]
Většina CO produkovaného u savců pochází z degradace heme třemi izoformami z hem oxygenáza, přičemž HO-1 je indukován oxidační stres, CO a řada xenobiotika.[3] HO-2 a HO-3 jsou konstitutivní. Jiné endogenní zdroje mohou zahrnovat peroxidaci lipidů,[4]
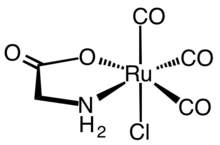
Enzymatická reakce hemové oxygenázy inspirovala vývoj syntetických CORM. První syntetické CORMy byly typicky karbonylové komplexy kovů. Reprezentativní CORM, který byl značně charakterizován jak z biochemického, tak farmakologického hlediska, je komplex ruthenia (II) Ru (glycinát ) Cl (CO)3, běžně známý jako CORM-3.
Klasifikace CORM
Nejjednodušší zdroj CO je z a spalovací reakce prostřednictvím zdrojů hoření jako fosilní paliva nebo palivové dřevo. Zdroje uvolňující CO při tepelný rozklad nebo spalování se obecně nepovažuje za CORM.
Přechodové kovové CORMy
Většina terapeuticky relevantních CORM jsou komplexy přechodných kovů primárně založené na žehlička, molybden, ruthenium, mangan, kobalt, a rhenium
PhotoCORMs
Uvolňování CO z nosičových látek může být indukováno fotochemicky. Tyto nosiče se nazývají photoCORM a zahrnují jak kovové komplexy, tak i nekovové (organický ) sloučeniny různých strukturních motivů, které lze považovat za speciální typ fotolabilní ochranná skupina.
ET-CORMY
Enzymem spouštěné CORM (ET-CORM) byly vyvinuty za účelem zlepšení selektivní lokální dodávky CO. Některé ET-CORM proléčiva jsou aktivovány pomocí esteráza enzymy pro místní specifické uvolňování CO.[5]
Organické CORMy
Organické malé molekuly jsou vyvíjeny, aby překonaly omezení toxicity anorganických CORM. Methylenchlorid byl první organický CORM orálně podávaný na základě předchozích zpráv o karboxyhemoglobin tvorba prostřednictvím metabolismu. Druhý organický CORM, CORM-A1 (boranokarbonát sodný), byl vyvinut na základě zprávy o uvolňování CO z borokarbonátu draselného ze 60. let.
V roce 2003 byly jako zdroj terapeutického CO navrženy cyklické oxokarbony kyselina deltová, kyselina čtvercová, kyselina krokonová, a kyselina rhodizonová a jejich soli.
Organické proléčiva CO
V posledních letech došlo k rostoucímu zájmu o proléčiva organických CO kvůli potřebě zohlednit problémy s vývojem léčiv při vývoji terapeutik založených na CO (Ji, X .; Damera, K .; Zheng, Y .; Yu, B; Otterbein, LE; a Wang, B. „Směrem k terapeutikám založeným na oxidu uhelnatém: kritické problémy s dodávkou a vývojem“, J. Pharm. Sci. 2016, 105, 406-416. PMID: 26869408). Tyto proléčiva CO mají nastavitelnou rychlost uvolňování, spouštěné uvolňování a schopnost uvolňovat více než jedno užitečné zatížení z jednoho proléčiva (Ji. X .; Wang, B. „Strategies towards Organic Carbon Monoxide Prodrugs“ Acc. Chem. Res. 2018, 51, 1377-85. PMID: 29762011).
Enzymové hybridy
Na základě synergie hem oxygenáza systémem a dodávkou CO se objevila nová třída molekulárních hybridů-CORM (HYCO) skládající se ze spojení HO-1 induktory a druhy CORM. Jeden takový HYCO zahrnuje a dimethylfumarát skupina, která se aktivuje NRF2 čímž indukuje HO-1, zatímco skupina CORM také uvolňuje CO.
Materiály uvolňující oxid uhelnatý
Materiály uvolňující oxid uhelnatý (CORMA) jsou v podstatě nové formulace léků a platformy pro podávání léků, které se objevily, aby překonaly farmaceutická omezení většiny druhů CORM.[6] Příkladná CORMA vyvinutá Hubbellem sestává z formulace micely připraveno z tribloku kopolymery s entitou CORM, která je spuštěna na vydání přidáním cystein. Mezi další lešení uvolňující CO patří polymery, peptidy, oxid křemičitý nanočástice, nanodiamant, magnetické nanočástice, nanovlákno gel, metallodendrimery a konjugáty CORM-protein (makromolekula).[7][8]
Infuze karboxyhemoglobinu
Karboxyhemoglobin může být naplněn k dodávání CO. Nejběžnější přístupy jsou založeny na polyethylenglykol (PEG) -lytovaný hovězí karboxyhemoglobin a maleimid Lidský karboxyhemoglobin konjugovaný s PEG.
Porfyriny
Porfyrin struktury jako heme, hemin a kovové protoporfyrin IX (PPIX) analogy (jako je kobalt PPIX) byly použity k indukci hem oxygenáza a následně podstoupit biotransformaci za účelem uvolnění CO, anorganického iontu a biliverdin /bilirubin.[9] Některé analogy PPIX, jako např cín PPIX, mesoporfyrin cínu a zinek PPIX, jsou hem oxygenáza inhibitory.
Endogenní CO
Na konci 60. let Tenhunen prokázal enzymatickou reakci na katabolismus hemu[10] čímž identifikuje hem oxygenáza (HO) enzym. HO je hlavním zdrojem endogenní produkce CO, ačkoli v posledních letech byly identifikovány další menší přispěvatelé. CO se tvoří v lidském těle rychlostí 16,4 µmol / hod., ~ 86% pochází z hemu prostřednictvím hemové oxygenázy a ~ 14% z jiných než hemových zdrojů, včetně: fotooxidace, peroxidace lipidů a xenobiotik.[11] Průměrný karboxyhemoglobin (CO-Hb) hladina u nekuřáka je mezi 0,2% a 0,85% CO-Hb (zatímco kuřák může mít mezi 4% a 10% CO-Hb),[12] ačkoli geografické umístění, povolání, zdraví a chování přispívají k proměnným.
Enzymy
Hem oxygenáza
Hem oxygenáza (HO) je člen obsahující hem protein tepelného šoku (HSP) rodina označená jako HSP32. Dosud byly identifikovány tři izoformy HO, včetně HO-1 a konstitutivních HO-2 a HO-3 vyvolaných stresem. HO-1 je považován za buněčný záchranný protein, který je indukován v reakci na oxidační stres a mnoho chorobných stavů. HO-1 je navíc indukován bezpočtem molekul včetně statiny, hemin, a přírodní produkty.[13]
HO katalyzuje degradaci hemu na biliverdin /bilirubin, železný iont a CO. I když je HO přítomen v těle, má významnou aktivitu v slezina při degradaci hemoglobin v době červená krvinka recyklace (0,8% zásob erytrocytů denně), což představuje ~ 80% endogenní produkce CO odvozené od hemů. Většina zbývajících 20% produkce CO odvozených od hemu je přičítána jaternímu katabolismu hemoproteiny (myoglobin, cytochromy, kataláza, peroxidázy, rozpustná guanylátcykláza, syntáza oxidu dusnatého ) a neúčinné erytropoéza v kostní dřeň.[14][15]
Peroxidace lipidů
Tvorba CO z lipid peroxidace byl poprvé uveden na konci 60. let a je považován za menšího přispěvatele k endogenní produkci CO.[16][17]
Farmakologie CO
Kysličník uhelnatý je jedním ze tří plynné signální molekuly vedle oxid dusnatý a sirovodík. Tyto plyny jsou souhrnně označovány jako plynové vysílače.
Signalizace
První důkaz CO jako signální molekuly se objevil po pozorování stimulace CO rozpustná guanylátcykláza a následující cyklický guanosinmonofosfát (cGMP) výroba sloužit jako vazodilatátor v cévní buňky hladkého svalstva.[18] The protizánětlivý účinky CO se připisují aktivaci p38 mitogenem aktivovaná protein kináza (MAPK) cesta. Zatímco CO běžně interaguje s atomem železa hemu v a hemoprotein bylo prokázáno, že CO aktivuje draslíkové kanály závislé na vápníku zapojením do vodíkové vazby s povrchovými zbytky histidinu.
CO má inhibiční účinek na řadu proteinů včetně cytochrom P450[19] a cytochrom c oxidáza
CO je modulátor iontových kanálů s excitačními i inhibičními účinky na četné třídy iontových kanálů, jako např napěťově řízené vápníkové kanály.
Rozdělení
CO má přibližně 210x větší afinitu k hemoglobin než kyslík.[20] Rovnováha disociační konstanta pro reakci Hb-CO ⇌ Hb + CO silně upřednostňuje komplex CO, takže uvolňování CO pro plicní vylučování nějakou dobu trvá.
Na základě této vazebné afinity je krev v podstatě nevratným záchytem CO a představuje terapeutickou výzvu pro dodávání CO do buněk a tkání.
Metabolismus
CO je považován za nereaktivní v těle a primárně prochází plicní vylučování a méně než 10% je oxidováno.[21]
Reference
- ^ Motterlini R, Otterbein LE (září 2010). "Terapeutický potenciál oxidu uhelnatého". recenzi článku. Recenze přírody. Objev drog. 9 (9): 728–43. doi:10.1038 / nrd3228. PMID 20811383.
- ^ Mahan VL (prosinec 2012). „Neuroprotektivní, neuroterapeutické a neurometabolické účinky oxidu uhelnatého“. recenzi článku. Lékařský výzkum plynu. 2 (1): 32. doi:10.1186/2045-9912-2-32. PMC 3599315. PMID 23270619.
- ^ Ferrándiz ML, Devesa I (2008). "Induktory hemu oxygenázy-1". recenzi článku. Současný farmaceutický design. 14 (5): 473–86. doi:10.2174/138161208783597399. PMID 18289074.
- ^ Wilkinson WJ, Kemp PJ (červenec 2011). „Oxid uhelnatý: nově vznikající regulátor iontových kanálů“. recenzi článku. The Journal of Physiology. 589 (Pt 13): 3055–62. doi:10.1113 / jphysiol.2011.206706. PMC 3145923. PMID 21521759.
- ^ Různý design enzymem spouštěných molekul uvolňujících CO (ET-CORM) odhaluje kvantitativní rozdíly v biologických aktivitách, pokud jde o toxicitu a zánět. Stamellou E, Storz D, Botov S, Ntasis E, Wedel J, Sollazzo S, Krämer BK, van Son W, Seelen M, Schmalz HG, Schmidt A, Hafner M, Yard BA, Redox Biol. 2014 5. června; 2: 739-48. doi: 10.1016 / j.redox.2014.06.002. eCollection 2014.
- ^ Heinemann SH, Hoshi T, Westerhausen M, Schiller A (duben 2014). "Oxid uhelnatý - fyziologie, detekce a řízené uvolňování". recenzi článku. Chemická komunikace (Cambridge, Anglie). 50 (28): 3644–60. doi:10.1039 / c3cc49196j. PMC 4072318. PMID 24556640.
- ^ Nguyen D, Boyer C (září 2015). „Makromolekulární a anorganické nanomateriály lešení pro dodávku oxidu uhelnatého: nedávný vývoj a budoucí trendy“. recenzi článku. ACS Biomaterials Science & Engineering. 1 (10): 895–913. doi:10.1021 / acsbiomaterials.5b00230.
- ^ Kautz AC, Kunz PC, Janiak C (listopad 2016). „Konjugované systémy molekuly uvolňující CO (CORM)“. recenzi článku. Daltonské transakce. 45 (45): 18045–18063. doi:10.1039 / c6dt03515a. PMID 27808304.
- ^ Maines MD (červenec 1988). "Hem oxygenáza: funkce, multiplicita, regulační mechanismy a klinické aplikace". recenzi článku. FASEB Journal. 2 (10): 2557–68. doi:10.1096 / fasebj.2.10.3290025. PMID 3290025. S2CID 22652094.
- ^ Tenhunen R, Marver HS, Schmid R (prosinec 1969). "Mikrozomální hemoxygenáza. Charakterizace enzymu". primární článek. The Journal of Biological Chemistry. 244 (23): 6388–94. PMID 4390967.
- ^ Wang R, ed. (2001). Oxid uhelnatý a kardiovaskulární funkce. recenze článek (první vydání). CRC Press. p. 5. ISBN 978-1-4200-4101-9.
- ^ Thom SR (2008). „Kapitola 15: Patofyziologie a léčba oxidu uhelnatého“. V Neuman TS, Thom SR (eds.). Fyziologie a medicína hyperbarické kyslíkové terapie. recenzi článku. 321–347. doi:10.1016 / B978-1-4160-3406-3.50020-2. ISBN 978-1-4160-3406-3.
- ^ Correa-Costa M, Otterbein LE (2014). „Eat to Heal: Natural Inducers of the Heme Oxygenase-1 System.“. Ve Folkerts G, Garssen J (eds.). Farmaceutická výživa. recenzi článku. AAPS Advances in the Pharmaceutical Sciences Series. 12. Springer, Cham. 243–256. doi:10.1007/978-3-319-06151-1_12. ISBN 978-3-319-06150-4.
- ^ Lundh B, Johansson MB, Mercke C, Cavallin-Stahl E (prosinec 1972). "Zvýšení katabolismu hemu kalorickou restrikcí u člověka". primární článek. Scandinavian Journal of Clinical and Laboratory Investigation. 30 (4): 421–7. doi:10.3109/00365517209080280. PMID 4639647.
- ^ Breman HJ, Wong RJ, Stevenson DK (30. října 2001). „Kapitola 15: Zdroje, jímky a měření oxidu uhelnatého“. Ve Wang R (ed.). Oxid uhelnatý a kardiovaskulární funkce. recenze článek (2. vyd.). CRC Press. ISBN 978-0-8493-1041-6.
- ^ Wolff DG (prosinec 1976). "Tvorba oxidu uhelnatého během peroxidace mikrozomálních lipidů". primární článek. Sdělení o biochemickém a biofyzikálním výzkumu. 73 (4): 850–7. doi:10.1016 / 0006-291X (76) 90199-6. PMID 15625852.
- ^ Nishibayashi H, Omma T, Sato R, Estabrook RW, Okunuki K, Kamen MD, Sekuzu I, eds. (1968). Struktura a funkce cytochromů. recenzi článku. University Park Press. str. 658–665.
- ^ Kim HP, Ryter SW, Choi AM (2006). "CO jako buněčná signální molekula". recenzi článku. Roční přehled farmakologie a toxikologie. 46: 411–49. doi:10.1146 / annurev.pharmtox.46.120604.141053. PMID 16402911.
- ^ Correia MA, Ortiz de Montellano PR (2005). "Inhibice enzymů cytochromu P450". Cytochrom P450. recenzi článku. Boston, MA: Springer. 247–322. doi:10.1007/0-387-27447-2_7. ISBN 978-0-306-48324-0.
- ^ Blumenthal I (červen 2001). „Otrava oxidem uhelnatým“. recenzi článku. Journal of the Royal Society of Medicine. 94 (6): 270–2. doi:10.1177/014107680109400604. PMC 1281520. PMID 11387414.
- ^ Wilbur S, Williams M, Williams R, Scinicariello F, Klotzbach JM, Diamond GL, Citra M (2012). "Zdravé efekty". Toxikologický profil oxidu uhelnatého. recenzi článku. Americké ministerstvo zdravotnictví a sociálních služeb, služba veřejného zdraví, Agentura pro toxické látky a registr nemocí. PMID 23946966.
Další čtení
- Kim HH, Choi S (srpen 2018). „Terapeutické aspekty oxidu uhelnatého při kardiovaskulárních onemocněních“. recenzi článku. International Journal of Molecular Sciences. 19 (8): 2381. doi:10,3390 / ijms19082381. PMC 6121498. PMID 30104479.
- Ismailova A, Kuter D, Bohle DS, Butler IS (2018). „Přehled potenciálních terapeutických aplikací molekul uvolňujících CO“. recenzi článku. Bioanorganická chemie a aplikace. 2018: 8547364. doi:10.1155/2018/8547364. PMC 6109489. PMID 30158958.
- Abeyrathna N, Washington K, Bashur C, Liao Y (říjen 2017). "Nekovové molekuly uvolňující oxid uhelnatý (CORM)". recenzi článku. Organická a biomolekulární chemie. 15 (41): 8692–8699. doi:10.1039 / c7ob01674c. PMID 28948260.
- Hopper C, Wollborn J (srpen 2019). "Dodávka oxidu uhelnatého pomocí halogenovaných etherových anestetik". recenzi článku. Oxid dusnatý. 89: 93–95. doi:10.1016 / j.niox.2019.05.006. PMID 31125687.
- Wilson JL, Jesse HE, Poole RK, Davidge KS (květen 2012). "Antibakteriální účinky oxidu uhelnatého". recenzi článku. Současná farmaceutická biotechnologie. 13 (6): 760–8. doi:10.2174/138920112800399329. PMID 22201612.
- Slanina T, Sebej P (květen 2018). „PhotoCORMs aktivované viditelným světlem: Racionální design organických molekul uvolňujících CO absorbujících v tkáňově průhledném okně“. recenzi článku. Fotochemické a fotobiologické vědy. 17 (6): 692–710. doi:10.1039 / C8PP00096D. PMID 29796556.
