Trimethylfosfit - Trimethyl phosphite
 | |||
| |||
| Jména | |||
|---|---|---|---|
| Preferovaný název IUPAC Trimethylfosfit[1] | |||
| Ostatní jména Trimethoxyfosfin Trimethoxyfosfan | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChemSpider | |||
| Informační karta ECHA | 100.004.065 | ||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C3H9Ó3P | |||
| Molární hmotnost | 124.08 | ||
| Vzhled | bezbarvá kapalina | ||
| Zápach | výrazný, štiplavý[2] | ||
| Hustota | 1.052 | ||
| Bod tání | -78 ° C (-108 ° F, 195 K) | ||
| Bod varu | 111 ° C (232 ° F; 384 K) | ||
| reaguje[2] | |||
| Tlak páry | 24 mmHg (25 ° C)[2] | ||
| Nebezpečí | |||
| Bod vzplanutí | 28 ° C; 82 ° F; 301 K. [2] | ||
| NIOSH (Limity expozice USA zdraví): | |||
PEL (Dovolený) | žádný[2] | ||
REL (Doporučeno) | PEL (časově vážený průměr) 2 ppm (10 mg / m3)[2] | ||
IDLH (Okamžité nebezpečí) | N.D.[2] | ||
| Související sloučeniny | |||
Související sloučeniny | Dimethylmethylfosfonát | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
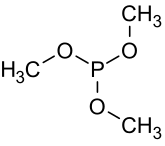
Trimethylfosfit je organofosforová sloučenina s vzorec P (OCH3)3, často zkráceně P (OMe)3. Je to bezbarvá kapalina s vysoce pronikavým zápachem. Používá se jako ligand v organokovová chemie a jako činidlo v organická syntéza. Molekula obsahuje pyramidový střed fosforu (III) vázaný na tři methoxy skupiny.
Syntéza a reakce
Trimethylfosfit se připravuje z chlorid fosforitý:
- PCl3 + 3 CH3OH → P (OCH3)3 + 3 HCl
Je citlivý na oxidaci trimethylfosfát.
Reaguje s katalytickým množstvím methyljodidu v Arbuzovova reakce dát dimethylmethylfosfonát:
- P (OCH3)3 → CH3P (O) (OCH3)2
Jako ligand má trimethylfosfit menší úhel kužele a lepší vlastnosti akceptoru ve vztahu k trimethylfosfin. Reprezentativním derivátem je bezbarvý čtyřboký komplex Ni (P (OMe)3)4 (t.t. 108 ° C).[3] Trojzubý ligand volal Kläui ligand je odvozen od trimethylfosfitu. Tvorba tohoto ligandu ilustruje citlivost trimethylfosfitu (a jeho kovových komplexů) na Arbuzovovu reakci.
Trimethylfosfit se také používá jako mírné odsiřovací činidlo v organické syntéze, například při přípravě derivátů tetrathiafulvalen.[4]
Toxicita
The LD50 je 1600–2890 mg / kg (orálně, potkan).[5]
Reference
- ^ Nomenklatura organické chemie: Doporučení IUPAC a preferovaná jména 2013 (modrá kniha). Cambridge: Královská společnost chemie. 2014. s. 931. doi:10.1039 / 9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ A b C d E F G NIOSH Kapesní průvodce chemickými nebezpečími. "#0640". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ Steven D. Ittel; Cushing, M. A. (1990). "Komplexy niklu (0)". Anorganické syntézy. Anorganické syntézy. 28: 98–104. doi:10.1002 / 9780470132593.ch25. ISBN 978-0-471-52619-3.
- ^ Larsen, Jan; Lenoir, Christine (1995). „2,2'-Bi-5,6-dihydro-l, 3-dithiolo [4,5-b] [l, 4] dithiinyliden (BEDT-TTF)". Org. Synth. 72: 265. doi:10.15227 / orgsyn.072.0265.
- ^ Svara, J .; Weferling, N .; Hofmann, T. "Fosforové sloučeniny, organické". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a19_545.pub2.


