Trimer (chemie) - Trimer (chemistry)
v chemie, a zastřihovač (/ˈtraɪm.r/ tri-, „tři“ + -mer, "části") je molekula nebo anion vytvořený kombinací nebo asociací tří molekul nebo iontů stejné látky. V technickém žargonu je něco jako ořezávač oligomer odvozeno od tří stejných prekurzorů, často konkurujících polymeraci.
Příklady
Alkyně trimerizace

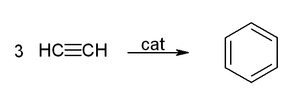
V roce 1866 Marcellin Berthelot uvedl první příklad cyklotrimerizace, převod z acetylén na benzen.[1] Tento proces byl komercializován:
Nitrilová trimerace
Symetrický 1,3,5-triaziny připravuje trimerizace jisté nitrily jako chlorkyan nebo kyanimid.
Chlorkyan a bromkyan každý trimeruje při zvýšených teplotách na uhlíkovém katalyzátoru.[1] Chlorid dává kyanurový chlorid:
Bromid má delší dobu použitelnosti, když je chlazen. Stejně jako chlorid podléhá abotermické trimeraci, aby se vytvořil kyanurový bromid. Tato reakce je katalyzována stopami bromu, solí kovů, kyselin a zásad.[2] Z tohoto důvodu se experimentátoři vyhýbají nahnědlým vzorkům.[3]
Průmyslová cesta do kyselina kyanurová znamená tepelný rozklad z močovina, s uvolňováním amoniaku. Konverze začíná při přibližně 175 ° C:[4]
- 3 H2N-CO-NH2 → [C (O) NH]3 + 3 NH3
Endotermická syntéza melamin lze pochopit ve dvou krocích.
Nejprve se močovina rozloží na kyselina kyanová a amoniak v endotermické reakci:
- (NH2)2CO → HOCN + NH3
Poté ve druhém kroku kyselina kyanová polymeruje za vzniku kyseliny kyanurové, která kondenzuje s uvolněným amoniakem z prvního kroku za uvolnění melaminu a vody.
- '3 HOCN → [C (O) NH]3
- [C (O) NH]3 + 3 NH3 → C.3H6N6 + 3 H2Ó
Tato voda poté reaguje s přítomnou kyselinou kyanovou, která pomáhá řídit trimerační reakci a vytváří oxid uhličitý a amoniak.
- 3 HOCN + 3 H2O → 3 CO2 + 3NH3
Druhým krokem je celkem exotermické:
- 6 HCNO + 3 NH3 → C.3H6N6 + 3 CO2 + 3NH3
ale celkový proces je endotermický.
Diene trimerizace
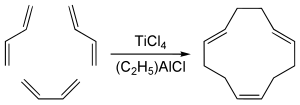
1,5,9-trans-trans-cis izomer z cyklododekatrien, který má určitý průmyslový význam, získává cyklotrimerizace z butadien s chlorid titaničitý a organohliník kokatalyzátor:[5]
Rozbití dvojných vazeb uhlík-hetero tvoří symetrické nasycené 1,3,5-heterocykly
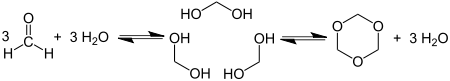
Cyklotrimerizace formaldehyd dovoluje 1,3,5-trioxan:
1,3,5-trithianu je cyklický trimer jinak nestabilního druhu thioformaldehyd. Tento heterocyklus sestává ze šestičlenného kruhu se střídáním methylenové můstky a thioetherové skupiny. Připravuje se zpracováním formaldehyd s sirovodík.[6]
Tři molekuly acetaldehyd kondenzovat do formy paraldehyd, cyklický trimer obsahující jednoduché vazby C-O.
Katalyzace a dehydratace kyselinou sírovou, trimerace aceton přes kondenzace aldolu dovoluje mesitylen[7]
Trisiloxany
Dimethylsilandiol dehydratuje na trimer Me2SiO stejně jako polydimethylsiloxan. Reakce ilustruje konkurenci mezi trimerací a polymerací. Polymer a trimer jsou formálně odvozeny z hypotetického sila-ketonu Me2Si = O, i když tento druh není meziprodukt.
Koordinační chemie
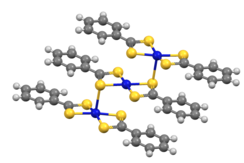
The dithiobenzoát komplexy [M (S2CPh)2] krystalizuje jako trimery (M = Ni, Pd).[8]
Viz také
Reference
- ^ A b Hillis O. Folkins (2005). „Benzen“. Ullmann's Encyclopedia of Industrial Chemistry. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a03_475. ISBN 3527306730.
- ^ Morris, Joel; Kovács, Lajos; Ohe, Kouichi (2015). „Cyanogen Bromide“. Encyklopedie činidel pro organickou syntézu. s. 1–8. doi:10.1002 / 047084289X.rc269.pub3. ISBN 9780470842898.
- ^ Joel Morris; Lajos Kovács (2008). „Cyanogen Bromide“. Encyklopedie činidel pro organickou syntézu. doi:10.1002 / 047084289X.rc269.pub2. ISBN 978-0471936237.
- ^ Klaus Huthmacher, Dieter Most "Kyselina kyanurová a chlorid kyanurový" "Ullmann's Encyclopedia of Industrial Chemistry" 2005, Wiley-VCH, Weinheim. Doi 10,1002 / 14356007.a08 191
- ^ Průmyslová organická chemieKlaus Weissermel, Hans-Jurgen Arpe John Wiley & Sons; 3. místo 1997 ISBN 3-527-28838-4
- ^ Bost, R. W .; Constable, E. W. „sym-Trithiane“ Organic Syntheses, Collected Volume 2, str. 610 (1943). „Archivovaná kopie“ (PDF). Archivovány od originál (PDF) dne 29.03.2012. Citováno 2014-05-05.CS1 maint: archivovaná kopie jako titul (odkaz)
- ^ Cumming, W. M. (1937). Systematická organická chemie (3E). New York, USA: D. Van Nostrand Company. str. 57.
- ^ Bonamico, M .; Dessy, G .; Fares, V .; Scaramuzza, L. (1975). „Strukturální studie kovových komplexů s bidentátovými ligandy obsahujícími síru. Část I. Krystalické a molekulární struktury trimérního bis- (dithiobenzoato) -niklu (II) a -palladia (II)“. Journal of the Chemical Society, Dalton Transactions (21): 2250–2255. doi:10.1039 / DT9750002250.CS1 maint: používá parametr autoři (odkaz)