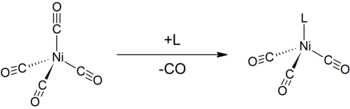Tolmanův elektronický parametr - Tolman electronic parameter

The Tolmanův elektronický parametr (TEP) je míra schopnosti elektronu darovat nebo vybírat elektrony ligand. Určuje se měřením frekvence A1 Vibrační režim CO (ν (CO)) (pseudo) -C3v symetrický komplex, [LNi (CO)3] od infračervená spektroskopie, kde L je požadovaný ligand. [LNi (CO)3] byla vybrána jako modelová sloučenina, protože takové komplexy jsou snadno připravitelné z tetrakarbonylnikel (0).[1][2] Posun ν (CO) se používá k odvození elektronických vlastností ligandu, což může pomoci pochopit jeho chování v jiných komplexech. Analýzu představil Chadwick A. Tolman.
A1 karbonylový pás je zřídka zakryt jinými pásmy v infračerveném spektru analytu. Karbonyl je malý ligand, takže sterické faktory analýzu nekomplikují. Po koordinaci CO na kov ν (CO) typicky klesá z 2143 cm−1 volného CO. Tento posun lze vysvětlit π zpětné vazby: kov tvoří vazbu π s karbonylovým ligandem darováním elektronů prostřednictvím svých d orbitalů do prázdných π * anti-vazebných orbitalů na CO. Tato interakce posiluje vazbu kov-uhlík, ale také oslabuje vazbu uhlík-kyslík, což vede k nižší vibrační frekvence. Pokud jiné ligandy zvyšují hustotu elektronů π na kovu, vazba C-O je oslabena a ν (CO) dále klesá; naopak, pokud jiné ligandy soutěží s CO o zpětné vazby π, zvyšuje se ν (CO).

| L | ν (CO) cm−1 |
|---|---|
| P (t-Bu)3 | 2056.1 |
| P (NMe2)3 | 2061.9 |
| PMe3 | 2064.1 |
| P (C.6H4OMe)3 | 2066 |
| PPh3 | 2068.9 |
| P (C.6H4F)3 | 2071.3 |
| Básník)3 | 2076.3 |
| PCl3 | 2097.0 |
| PF3 | 2110.8 |
The Tolmanův úhel kužele a TEP byly použity k charakterizaci sterických a elektronických vlastností fosfiny, což jsou populární ligandy pro katalyzátory.
Při léčbě podobné analýze TEP byly vlastnosti dárce N-heterocyklický karben (NHC) ligandy byly seřazeny podle IR dat zaznamenaných na cis- [RhCl (NHC) (CO)2] komplexy.[3][4]
Viz také
Reference
- ^ Robert H. Crabtree (2005). Karbonyly, fosfinové komplexy a substituční reakce ligandů. str. 87–124. doi:10.1002 / 0471718769.ch4.
- ^ A b Tolman, C. A. (1977). "Sterické účinky fosforových ligandů v organokovové chemii a homogenní katalýze". Chem. Rev. 77 (3): 313–348. doi:10.1021 / cr60307a002.
- ^ Nonnenmacher, Michael; Buck, Dominik M; Kunz, Doris (23. srpna 2016). „Experimentální a teoretické výzkumy charakteru vysoce elektronových donorů pyrido-anlovaných N-heterocyklických karbenů“. Beilstein Journal of Organic Chemistry. 12: 1884–1896. doi:10,3762 / bjoc.12.178. PMC 5082490.
- ^ Huynh, Han Vinh (30. března 2018). "Elektronické vlastnosti N-heterocyklických karbenů a jejich experimentální stanovení". Chemické recenze. 118 (19): 9457–9492. doi:10.1021 / acs.chemrev.8b00067.
Další čtení
- Tonner, Ralf; Frenking, Gernot (2009). "Tolmanovy elektronické parametry pro sloučeniny dvojmocného uhlíku (0)". Organometallics. 28 (13): 3901–3905. doi:10.1021 / om900206w.
- Gusev, Dmitrij G. (2009). „Elektronické a sterické parametry 76 N-heterocyklických karbenů v Ni (CO)3(NHC) ". Organometallics. 28 (22): 6458–6461. doi:10,1021 / om900654g.