Nitroalken - Nitroalkene
A nitroalken, nebo nitro olefin, je a funkční skupina kombinující funkčnost jeho základních částí, an alken a nitroskupina, zatímco zobrazuje své vlastní chemické vlastnosti prostřednictvím aktivace alkenu, což činí funkční skupinu užitečnou při speciálních reakcích, jako je Michaelova reakce nebo Diels-Alder dodatky.[1]
Syntéza
Nitroalkeny jsou syntetizovány různými způsoby, pozoruhodné příklady zahrnují:
- Nitrace alkenu s vytvořeným nitryljodidem in situ z dusitan stříbrný a elementární jód:[5]

- Přímá nitrace alkenů s oxid dusnatý a oxid hlinitý katalyzátor v kyselé podmínky:[6]

- Přímá nitrace alkenů s Clayfen (Dusičnan železitý podporováno dne Montmorillonit jíl):[7]

- Dehydratace nitroalkoholů:[8]

Reakce
Nitroalkeny jsou užitečné meziprodukty pro různé chemické funkce.
- Nitroalken chující se jako Michael akceptor při syntéze lycoricidinu:[1][9]

- Nitroalken působí jako aktivovaný dienophile k butadien v Diels-Alder cykloadice:[1][10]

- Syntéza pyrrol deriváty přes Barton-Zardova reakce:[11]

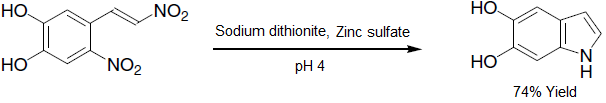
- Pericyklická reakce nitroalkenu poskytující an indol:[12]
- Částečný hydrogenace k alkenovému obnažení a hydroxylamin funkční skupina:[13]


- Asymetrický Stetterova reakce:[15]

Reference
- ^ A b C d Furniss, Brian; Hannaford, Antony; Smith, Peter & Tatchell, Austin (1996). Vogelova učebnice praktické organické chemie 5. vyd. London: Longman Science & Technical. str.635, 768, 1035–1036, & 1121. ISBN 9780582462366.
- ^ Ballini, Roberto; Castagnani, Roberto; Petrini, Marino (1992). "Chemoselektivní syntéza funkcionalizovaných konjugovaných nitroalkenů". The Journal of Organic Chemistry. 57 (7): 2160–2162. doi:10.1021 / jo00033a045.
- ^ Worrall, David E. (1929). „Nitrostyren“. Org. Synth. 9: 66. doi:10.15227 / orgsyn.009.0066.
- ^ Chandrasekhar, S .; Shrinidhi, A. (2014). „Užitečná rozšíření Henryho reakce: Rychlé cesty k nitroalkanům a nitroalkenům ve vodném prostředí“. Syntetická komunikace. 44 (20): 3008–3018. doi:10.1080/00397911.2014.926373.
- ^ Waldman, Steve; Monte, Aaron, Monte; Bracey, Ann & Nichols, David (1996). "One-pot Claisenův přesmyk / O-methylace / alkenová izomerizace při syntéze ortho-methoxylovaných fenylisopropylaminů". Čtyřstěn dopisy. 37 (44): 7889–7892. doi:10.1016/0040-4039(96)01807-2.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Mukaiyama, T .; Hata E. a Yamada, T. (1995). "Pohodlná a jednoduchá příprava nitroolefinů Nitrace olefinů oxidem dusnatým". Chemické dopisy. 24 (7): 505–506. doi:10.1246 / cl.1995.505.
- ^ Varma, Rajender; Naicker, Kannan; Liesen, Per (1998). „Selektivní nitrace styrenů pomocí jílu a jínu: Syntéza β-nitrostyrenů bez obsahu rozpouštědel“. Čtyřstěn dopisy. 39 (23): 3977–3980. doi:10.1016 / S0040-4039 (98) 00740-0.
- ^ Ranganathan, Darshan; Rao, Bhushan; Ranganathan, Subramania; Mehrotra, Ashok & Iyengar, Radha (1980). „Nitroethylen: stabilní, čisté a reaktivní činidlo pro organickou syntézu“. The Journal of Organic Chemistry. 45 (7): 1185–1189. doi:10.1021 / jo01295a003.
- ^ Jubert, Carole a Knochel, Paul (1992). „Příprava polyfunkčních nitro-olefinů a nitroalkanů za použití měď-zinkových činidel RCu (CN) ZnI.“ The Journal of Organic Chemistry. 57 (20): 5431–5438. doi:10.1021 / jo00046a027.
- ^ Noboru Ono; Hideyoshi Miyake; Akio Kamimura a Aritsune, Kaji (1987). „Regioselektivní Diels – Alderovy reakce. Nitroskupina jako regiochemický kontrolní prvek“. Perkinovy transakce. 1: 1929–1935. doi:10.1039 / P19870001929.
- ^ Jie Jack Li (2013). Heterocyklická chemie v objevu drog. New York: Wiley. ISBN 9781118354421. 43-4
- ^ Novellino, Luisa; d'Ischia, Marco & Prota, Giuseppe (1999). „Účelná syntéza 5,6-dihydroxyindolu a derivátů prostřednictvím vylepšeného přístupu Zn (II) - 2, β-dinitrostyrenu“. Syntéza. 5: 793–796. doi:10,1055 / s-1999-3469.
- ^ A b Masahiko Kohno; Shigehiro Sasao & Shun-Ichi Murahashi (1990). "Syntéza fenethylaminů hydrogenací β-nitrostyrenů". Bulletin of the Chemical Society of Japan. 63 (4): 1252–1254. doi:10,1246 / bcsj.63.1252.
- ^ Koch, Werner & Reichert, Benno (1935). „Über die katalytische Hydrierung substituierter ω-Nitrostyrole“. Archiv der Pharmazie. 273 (18–20): 265–274. doi:10,1002 / ardp.19352731802.
- ^ DiRocco, D. A .; Oberg, K. M .; Dalton, D. M .; Rovis, T. (2009). „Katalytická asymetrická intermolekulární stetterová reakce heterocyklických aldehydů s nitroalkeny: Fluorace páteře zlepšuje selektivitu“. Journal of the American Chemical Society. 131 (31): 10872–10874. doi:10.1021 / ja904375q. PMC 2747345. PMID 19722669.

