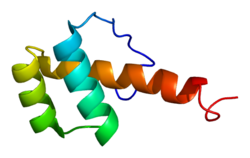
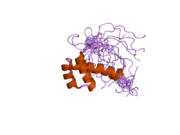
Husí protein - Goosecoid protein
Homeobox proteinový husí tuk je protein že u lidí je kódován GSC gen.[5][6]Tento gen kóduje člena bikoidní podrodiny spárované (PRD) rodiny proteinů. Kódovaný protein funguje jako transkripční faktor a může být autoregulační. Podobný protein u myší hraje roli ve vývoji kraniofaciálního a hrudního koše během embryogeneze.[6]
Kollerův srp je první, kdo exprimuje kuřecí homeoboxový gen husí kůže (GSC).[7]
Funkce
Gen GSC definuje specifikaci osudu buněk neurální lišty a přispívá k dorzální - ventrální struktuře. Nad aktivací v Xenopus podporuje dorso-přední migraci a dorsalizaci mezodermální tkáň buněk spolu s BMP-4.[8] Naopak analýza ztráty funkce nepřímo zabránila tvorbě hlavy v Xenopus [9] a vady hlavy u zebrafish.[10] Přestože knock-out studie na myších ukázaly, že gen GSC není pro gastrulaci nutný, stále existuje redukce báze lebky. Mutace genu GSC v Drosophila je smrtící.[11]
Gen Gsc podporuje tvorbu Spemannova organizátoru. Tento organizér brání BMP-4 ve vyvolání ektoderm v budoucí oblasti hlavy embrya se stane epidermis; místo toho umožňuje budoucí oblasti hlavy tvořit nervové záhyby, které se nakonec promění v mozek a míchu. Aby došlo k normálnímu přednímu vývoji, nemůže Spemannův organizátor vyjádřit transkripční faktory Xwnt-8 nebo BMP-4. Gsc přímo potlačuje expresi Xwnt-8 a nepřímo potlačuje BMP-4.[12] Inhibice Xwnt-8 a BMP-4 zajišťuje, že může dojít k normálnímu přednímu vývoji podporovanému Spemannovým organizátorem.
Exprese Gsc se vyskytuje ve vývoji dvakrát, první během gastrulace a druhá během organogeneze.[13] Gsc se nachází ve vysokých koncentracích v dorzálním mezodermu a endoderm během gastrulace. Pozdější výraz Gsc je omezen na oblast hlavy. V Xenopus se buňky, které exprimují Gsc, stávají faryngeálním endodermem, mesodermem hlavy, ventrální kosterní tkání hlavy a záznamem.[14]
Mutace
Mutace v genu GSC způsobuje nízký vzrůst, atrézii sluchového kanálu, hypoplázii mandibuly a abnormality skeletu (SAMS). SAMS se dříve považovala za autosomálně-recesivní poruchu, ale studie s molekulárním karyotypem a sekvenováním celého exomu (WES) ukázaly opak.[15]
Mutace v genu Gsc mohou vést ke specifickým fenotypům vyplývajícím z druhé exprese genu Gsc během organogeneze. Myší knock-out modely genu vyjadřují defekty v jazyku, nosní dutině, nosních jamkách, vnitřním uchu a zevním zvukovodu.[16] Novorozené myši narozené s touto mutací umírají do 24 hodin kvůli komplikacím s dýcháním a sáním mléka v důsledku kraniofaciálních abnormalit způsobených mutací. Mutace genu Gsc u lidí mohou vést ke stavu známému jako SAMS syndrom, charakterizovaný nízkým vzrůstem, atrézií sluchového kanálu, hypoplázií dolní čelisti a abnormalitami skeletu.[15][17]
Role ve vývoji rakoviny
Vzhledem ke své roli jako transkripční faktor v buněčné migraci během embryonálního vývoje byla GSC považována za potenciálního hráče ve vývoji rakoviny a metastáz, protože embryonální vývoj a vývoj rakoviny mají podobné vlastnosti. GSC, spolu s dalšími transkripčními faktory, jako je Kroutit, FOXC2, a Hlemýžď, vyvolat epiteliální až mezenchymální přechody regulací proteinů adheze buněk E-kadherin, α-katenin a exprese y-kateninu v epitelových buňkách.[18] Studie prokázaly, že ve vysoce metastatických buňkách vaječníků, plic, prsu a dalších rakovinných buňkách je GSC vysoce exprimován na počátku progrese nádoru.[19] Kromě toho vysoké hladiny exprese GSC v rakovinných buňkách korelují se špatnou mírou přežití, a lze je tedy použít jako prognostický nástroj.[20] Vysoká exprese GSC také koreluje s chemorezistencí rakoviny. GSC „proto připravuje buňky pro expresi agresivních fenotypů[19]„A“ mohou být nejpotenciálnějším biomarkerem reakce na léky a špatné prognózy.[20]”
Reference
- ^ A b C GRCh38: Vydání souboru 89: ENSG00000133937 - Ensembl, Květen 2017
- ^ A b C GRCm38: Vydání souboru 89: ENSMUSG00000021095 - Ensembl, Květen 2017
- ^ „Human PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ „Myš PubMed Reference:“. Národní centrum pro biotechnologické informace, Americká národní lékařská knihovna.
- ^ Blum M, De Robertis EM, Kojis T, Heinzmann C, Klisak I, Geissert D, Sparkes RS (květen 1994). "Molekulární klonování humánního homeobox genu husíhocoidu (GSC) a mapování genu na lidský chromozom 14q32.1". Genomika. 21 (2): 388–93. doi:10.1006 / geno.1994.1281. PMID 7916327.
- ^ A b „Entrez Gene: GSC goosecoid“.
- ^ Izpisúa-Belmonte JC, De Robertis EM, Storey KG, Stern CD (srpen 1993). "Homeobox gen goosecoid a původ organizátorových buněk v raném kuřatém blastodermu". Buňka. 74 (4): 645–59. doi:10.1016 / 0092-8674 (93) 90512-o. PMID 7916659.
- ^ Niehrs C, Keller R, Cho KW, De Robertis EM (1993). „Homeoboxový gen goosecoid řídí migraci buněk dovnitř Xenopus embrya ". Buňka. 72 (4): 491–503. doi:10.1016/0092-8674(93)90069-3. PMID 8095000.
- ^ Steinbeisser H, Fainsod A, Niehrs C, Sasai Y, De Robertis EM (listopad 1995). „Role gsc a BMP-4 při dorzálně-ventrální tvorbě okrajové zóny u Xenopus: studie ztráty funkce s použitím antisense RNA“. Časopis EMBO. 14 (21): 5230–43. doi:10.1002 / j.1460-2075.1995.tb00208.x. PMC 394633. PMID 7489713.
- ^ Rivera-Pérez JA, Mallo M, Gendron-Maguire M, Gridley T, Behringer RR (září 1995). „Goosecoid není nezbytnou součástí organizéru myší gastruly, ale je nezbytný pro vývoj kraniofaciální oblasti a žeber“. Rozvoj. 121 (9): 3005–12. PMID 7555726.
- ^ Goriely A, Stella M, Coffinier C, Kessler D, Mailhos C, Dessain S, Desplan C (květen 1996). "Funkční homolog husí kůže v Drosophile". Rozvoj. 122 (5): 1641–50. PMID 8625850.
- ^ Yao J, Kessler DS (srpen 2001). „Goosecoid podporuje aktivitu hlavního organizátora přímým potlačením Xwnt8 v organizátoru Spemanna“. Rozvoj. 128 (15): 2975–87. PMID 11532920.
- ^ Yamada G, Mansouri A, Torres M, Stuart ET, Blum M, Schultz M, De Robertis EM, Gruss P (září 1995). "Cílená mutace myšího genu pro husí kůži má za následek kraniofaciální defekty a smrt novorozence". Rozvoj. 121 (9): 2917–22. PMID 7555718.
- ^ De Robertis E, Blum M, Niehrs C, Steinbeisser H (duben 1992). „Mezodermová indukce a počátky embryonální osy: husí kůže a organizátor“. Rozvoj. 116: 167–171.
- ^ A b Parry DA, Logan CV, Stegmann AP, Abdelhamed ZA, Calder A, Khan S, Bonthron DT, Clowes V, Sheridan E, Ghali N, Chudley AE, Dobbie A, Stumpel CT, Johnson CA (prosinec 2013). „SAMS, syndrom krátkého věku, atrézie sluchového kanálu, hypoplázie mandibuly a poruchy skeletu, je jedinečná neurocristopatie způsobená mutacemi v husí kůži“. American Journal of Human Genetics. 93 (6): 1135–42. doi:10.1016 / j.ajhg.2013.10.027. PMC 3853132. PMID 24290375.
- ^ Yamada G, Ueno K, Nakamura S, Hanamure Y, Yasui K, Uemura M, Eizuru Y, Mansouri A, Blum M, Sugimura K (duben 1997). „Abnormality nosu a hltanu způsobené mutací genu myšího husího střeva“. Sdělení o biochemickém a biofyzikálním výzkumu. 233 (1): 161–5. doi:10.1006 / bbrc.1997.6315. PMID 9144415.
- ^ Lemire EG, Hildes-Ripstein GE, Reed MH, Chudley AE (leden 1998). „SAMS: prozatímně jedinečný syndrom mnohočetných vrozených anomálií sestávající z malého vzrůstu, atrézie sluchového kanálu, hypoplázie dolní čelisti a kostních abnormalit“. American Journal of Medical Genetics. 75 (3): 256–60. doi:10.1002 / (sici) 1096-8628 (19980123) 75: 3 <256 :: aid-ajmg5> 3.0.co; 2-o. PMID 9475592.
- ^ Mani SA, Yang J, Brooks M, Schwaninger G, Zhou A, Miura N, Kutok JL, Hartwell K, Richardson AL, Weinberg RA (červen 2007). „Mesenchyme Forkhead 1 (FOXC2) hraje klíčovou roli při metastázách a je spojován s agresivními bazálními karcinomy prsu“. Sborník Národní akademie věd Spojených států amerických. 104 (24): 10069–74. doi:10.1073 / pnas.0703900104. PMC 1891217. PMID 17537911.
- ^ A b Hartwell KA, Muir B, Reinhardt F, Carpenter AE, Sgroi DC, Weinberg RA (prosinec 2006). „Spemannův organizérový gen, Goosecoid, podporuje metastázy v nádoru“. Sborník Národní akademie věd Spojených států amerických. 103 (50): 18969–74. doi:10.1073 / pnas.0608636103. PMC 1748161. PMID 17142318.
- ^ A b Kang KW, Lee MJ, Song JA, Jeong JY, Kim YK, Lee C, Kim TH, Kwak KB, Kim OJ, An HJ (červenec 2014). „Nadměrná exprese husíhocoidního homeoboxu je spojena s chemorezistencí a špatnou prognózou u ovariálního karcinomu“. Zprávy o onkologii. 32 (1): 189–98. doi:10.3892 / nebo 2014.3203. PMID 24858567.
Další čtení
- Schlade-Bartusiak K, Macintyre G, Zunich J, Cox DW (leden 2008). "Dítě s vypuštěním (14) (q24.3q32.13) a sluchovou neuropatií". American Journal of Medical Genetics Part A. 146A (1): 117–23. doi:10,1002 / ajmg.a.32064. PMID 18074379.
- Hartwell KA, Muir B, Reinhardt F, Carpenter AE, Sgroi DC, Weinberg RA (prosinec 2006). „Spemannův organizérový gen, Goosecoid, podporuje metastázy v nádoru“. Sborník Národní akademie věd Spojených států amerických. 103 (50): 18969–74. doi:10.1073 / pnas.0608636103. PMC 1748161. PMID 17142318.
- Barrios-Rodiles M, Brown KR, Ozdamar B, Bose R, Liu Z, Donovan RS, Shinjo F, Liu Y, Dembowy J, Taylor IW, Luga V, Przulj N, Robinson M, Suzuki H, Hayashizaki Y, Jurisica I, Wrana JL (březen 2005). "Vysoce výkonné mapování dynamické signalizační sítě v savčích buňkách". Věda. 307 (5715): 1621–5. doi:10.1126 / science.1105776. PMID 15761153.
- Namciu SJ, Friedman RD, Marsden MD, Sarausad LM, Jasoni CL, Fournier RE (březen 2004). "Sekvenční organizace a oblasti připojení matrice genu klastru lidského inhibitoru serinové proteázy na 14q32.1". Savčí genom. 15 (3): 162–78. doi:10.1007 / s00335-003-2311-r. PMID 15014966.
- Foucher I, Montesinos ML, Volovitch M, Prochiantz A, Trembleau A (květen 2003). „Společná regulace promotoru MAP1B HNF3beta / Foxa2 a Engrailed je výsledkem vysoce konzervativního mechanismu pro přímou interakci homeoproteinů a Fox transkripčních faktorů.“. Rozvoj. 130 (9): 1867–76. doi:10,1242 / dev.00414. PMID 12642491.
- Danilov V, Blum M, Schweickert A, Campione M, Steinbeisser H (leden 1998). „Negativní autoregulace husíhooidu genu homeoboxu specifického pro organizátor“. The Journal of Biological Chemistry. 273 (1): 627–35. doi:10.1074 / jbc.273.1.627. PMID 9417125.