Pokožka - Epidermis
| Pokožka | |
|---|---|
 Mikroskopický obrázek epidermis, který tvoří vnější vrstvu kůže, zde zobrazený bílým pruhem | |
 Mikroskopický snímek ukazující vrstvy epidermis. The stratum corneum na tomto obrázku vypadá kompaktněji než výše kvůli odlišné přípravě vzorků. | |
| Detaily | |
| Část | Kůže |
| Systém | Mezistátní systém |
| Identifikátory | |
| latinský | Pokožka |
| Pletivo | D004817 |
| TA98 | A16.0.00.009 |
| TA2 | 7046 |
| TH | H3.12.00.1.01001 |
| FMA | 70596 |
| Anatomické termíny mikroanatomie | |
The pokožka je nejvzdálenější ze tří vrstev, které tvoří kůže, přičemž vnitřní vrstvy jsou dermis a podkoží.[1] Vrstva epidermis poskytuje bariéru infekce z prostředí patogeny[2] a reguluje množství vody uvolněné z těla do atmosféra přes transepidermální ztráta vody.[3] Epidermis se skládá z více vrstev zploštělých buněk[4] překrývající základní vrstvu (stratum basale ) složen z sloupcové buňky uspořádány kolmo.
Řady buněk se vyvíjejí z kmenové buňky v bazální vrstvě. Buněčné mechanismy pro regulaci hladiny vody a sodíku (ENaCs ) se nacházejí ve všech vrstvách epidermis.[5]
Slovo epidermis je odvozeno z latiny od Starořečtina pokožka, sám od Starořečtina epi „přes, po“ a od Starořečtina derma 'kůže'. Něco, co souvisí nebo je součástí epidermis, se nazývá epidermální.
Lidská pokožka je známým příkladem epitel, zejména a vrstvený dlaždicový epitel.
Struktura
Buněčné komponenty
Epiderma primárně sestává z keratinocyty[4] (množí se bazální a diferencované suprabasal), který obsahuje 90% jeho buněk, ale také obsahuje melanocyty, Langerhansovy buňky, Buňky Merkelové,[6]:2–3 a zánětlivé buňky. Volaly epidermální zesílení Rete hřebeny (nebo rete pegs) se táhnou dolů mezi dermální papily.[7]Krev kapiláry se nacházejí pod epidermis a jsou spojeny s arteriol a a venule Samotná epidermis nemá dodávka krve a je vyživován téměř výlučně rozptýleným kyslíkem z okolního vzduchu.[8]
Spojení buněk
Epidermální buňky jsou pevně propojeny, aby sloužily jako těsná bariéra proti vnějšímu prostředí. Spoje mezi epidermálními buňkami jsou adherens křižovatka typu, tvořeného transmembránovými proteiny zvanými kadheriny. Uvnitř buňky jsou spojeny kadheriny aktin vlákna. V imunofluorescenční mikroskopii se síť aktinových vláken jeví jako silná hranice obklopující buňky,[5] Ačkoliv aktinová vlákna jsou skutečně umístěny uvnitř buňky a probíhají rovnoběžně s buněčnou membránou. Kvůli blízkosti sousedních buněk a těsnosti spojů, aktinu imunofluorescence se objeví jako hranice mezi buňkami.[5]
Vrstvy

Epiderma se skládá ze 4 nebo 5 vrstev, v závislosti na uvažované oblasti kůže.[9] Tyto vrstvy v sestupném pořadí jsou:[2]

- Skládá se z 10 až 30 vrstev polyedrického, anukleačního korneocyty (poslední krok keratinocytů diferenciace ), přičemž dlaně a chodidla mají nejvíce vrstev. Korneocyty obsahují a protein obal (zrohovatělé obalové proteiny) pod plazmatickou membránou, jsou naplněny zadržující vodou keratin proteiny, spojené dohromady korneodesmosomy a obklopen v extracelulární prostor skládanými vrstvami lipidy.[10] Většina bariérových funkcí epidermis se lokalizuje do této vrstvy.[11]
- čirá / průsvitná vrstva (stratum lucidum, pouze v dlaních a chodidlech)
- Tato úzká vrstva se nachází pouze na dlaních a chodidlech. Epiderma těchto dvou oblastí je známá jako „tlustá kůže“, protože s touto další vrstvou má pokožka 5 epidermálních vrstev místo 4.
- zrnitá vrstva (stratum granulosum )

- Keratinocyty ztrácejí své jádra a jejich cytoplazma vypadá zrnitě. Lipidy obsažené v těchto keratinocytech uvnitř lamelová tělesa, jsou uvolňovány do extracelulárního prostoru skrz exocytóza k vytvoření lipidové bariéry. Tyto polární lipidy jsou poté převedeny na nepolární lipidy a uspořádány rovnoběžně s povrchem buňky. Například glykosfingolipidy stát se ceramidy a fosfolipidy stát se volné mastné kyseliny.[10]
- trnitá vrstva (stratum spinosum )

- Keratinocyty jsou propojeny desmosomy a vyrábět lamelová tělesa zevnitř Golgi, obohacený o polární lipidy, glykosfingolipidy, volný, uvolnit steroly, fosfolipidy a katabolické enzymy.[3] Langerhansovy buňky, imunologicky aktivní buňky, jsou umístěny uprostřed této vrstvy.[10]
- bazální / zárodečná vrstva (stratum basale / germinativum ).

- Skládá se hlavně z proliferujících a neproliferujících keratinocytů připojených k bazální membrána podle hemidesmosomy. Jsou přítomny melanocyty spojené s mnoha keratinocyty v této a dalších vrstvách dendrity. Buňky Merkelové se také nacházejí v stratum basale s velkým počtem na dotykových webech, jako je konečky prstů a rty. Jsou úzce spojeny s kožními nervy a zdá se, že jsou zapojeni do pocitu lehkého dotyku.[10]
The Malpighianská vrstva (stratum malpighi) je jak stratum basale, tak stratum spinosum.[4]
Epidermis je oddělena od dermis, jeho podkladu tkáň, a bazální membrána.
Buněčná kinetika
Buněčné dělení
Jako vrstvený dlaždicový epitel, epidermis je udržována buněčné dělení ve stratum basale. Diferenciace buňky se oddělí od bazální membrána a jsou přemístěny ven skrz epidermální vrstvy, prochází několika stadii diferenciace, dokud ve stratum corneum neztratí jádro a fúzují s plochými vrstvami, které se nakonec zbaví povrchu (deskvamace ). Diferencované keratinocyty vylučují keratinové proteiny, které přispívají k tvorbě extracelulární matrice, která je nedílnou součástí funkce kožní bariéry. U normální kůže se rychlost produkce keratinocytů rovná rychlosti ztráty,[4] cesta buňky ze stratum basale na vrchol stratum granulosum trvá asi dva týdny a další čtyři týdny překlenutí stratum corneum.[2] Celá epidermis je nahrazena novou buňkou růst po dobu přibližně 48 dnů.[12]
Koncentrace vápníku
Diferenciace keratinocytů v celé pokožce je částečně zprostředkována a vápník gradient, zvyšující se od stratum basale do vnější stratum granulosum, kde dosahuje svého maxima, a klesající ve stratum corneum. Koncentrace vápníku ve stratum corneum je částečně velmi nízká, protože tyto relativně suché buňky nejsou schopny rozpustit ionty. Tento gradient vápníku odpovídá diferenciaci keratinocytů a jako takový je považován za klíčový regulátor při tvorbě epidermálních vrstev.[3]
Zvýšení extracelulárních koncentrací vápníku vyvolává zvýšení intracelulární koncentrace volného vápníku.[13] Část tohoto intracelulárního zvýšení pochází z vápníku uvolněného z intracelulárních zásob[14] a další část pochází z transmembránového přítoku vápníku,[15] prostřednictvím citlivých na vápník chloridové kanály[16] a napěťově nezávislé kationtové kanály propustné pro vápník.[17] Kromě toho bylo navrženo, že extracelulární snímání vápníku receptor (CaSR) také přispívá ke zvýšení intracelulární koncentrace vápníku.[18]
Rozvoj
Epidermální organogeneze, tvorba epidermis, začíná v buňkách pokrývajících embryo po neurulace, vznik centrální nervový systém. Ve většině obratlovců, tato původní jednovrstvá struktura se rychle přemění na dvouvrstvou tkáň; dočasná vnější vrstva, periderm, který je uložen jednou vnitřní bazální vrstva nebo stratum germinativum se vytvořil.[19]
Tato vnitřní vrstva je a zárodečný epitel což vede ke vzniku všech epidermálních buněk. Rozděluje se a tvoří vnější trnitá vrstva (stratum spinosum ). Buňky těchto dvou vrstev, společně nazývané Malpighianská vrstva (s) po Marcello Malpighi, rozdělte a vytvořte povrchní zrnitý vrstva (Stratum granulosum) epidermis.[19]
Buňky ve stratum granulosum se nedělí, ale místo toho tvoří kožní buňky zvané keratinocyty z granule z keratin. Tyto kožní buňky se nakonec stávají zrohovatělá vrstva (stratum corneum), nejvzdálenější epidermální vrstva, kde se buňky stávají zploštěl pytle s jádry umístěnými na jednom konci buňky. Po narození tyto nejvzdálenější buňky jsou nahrazeny novými buňkami ze stratum granulosum a dále život jsou vylučovány rychlostí 0,001 - 0,003 unce kožních vloček každou hodinu nebo 0,024-0,072 uncí denně.[20]
Epidermální rozvoj je produktem několika růstové faktory, z nichž dva jsou:[19]
- Transformující růstový faktor Alfa (TGFα ) je autokrinní růstový faktor, kterým bazální buňky stimulují své vlastní divize.
- Keratinocytový růstový faktor (KGF nebo FGF7 ) je parakrin růstový faktor produkovaný podkladem kožní fibroblasty ve kterém proliferace bazálních buněk je regulován.
Funkce
Bariéra
Epidermis slouží jako bariéra k ochraně těla před mikrobiální patogeny, oxidační stres (UV světlo ), a chemikálie sloučeniny a poskytuje mechanické odolnost vůči lehkému zranění. Většinu této bariéry hraje stratum corneum.[11]
- Vlastnosti
- Fyzická bariéra: Epidermální keratinocyty jsou pevně spojeny spojení buňka-buňka spojené s cytoskeletální proteiny, což dodává pokožce mechanickou pevnost.[3]
- Chemická bariéra: Vysoce organizované lipidy, kyseliny, hydrolytické enzymy, a antimikrobiální peptidy[3] inhibují průchod vnějších chemikálií a patogenů do těla.
- Imunologicky aktivní bariéra: Humorný a buněčný složky imunitní systém[3] nalezené v pokožce aktivně bojují proti infekci.
- Obsah vody v stratum corneum klesá k povrchu a vytváří nepřátelské podmínky pro patogenní mikroorganismus růst.[11]
- Kyselý pH (kolem 5,0) a nízké množství vody činí epidermis nepřátelskou vůči mnoha mikroorganickým patogenům.[11]
- Nepatogenní mikroorganismy na povrchu epidermis pomáhají chránit před patogeny tím, že soutěží o jídlo, omezuje jeho dostupnost a vyrábí chemikálie sekrece které inhibují růst patogenní mikrobioty.[11]
- Propustnost
- Psychologický stres prostřednictvím zvýšení glukokortikoidy, ohrožuje stratum corneum a tím bariérovou funkci.[21]
- Náhlé a velké posuny vlhkost vzduchu alter stratum corneum hydratace způsobem, který by umožňoval vstup patogenních mikroorganismů.[22]
Hydratace pokožky
Schopnost pokožky zadržovat vodu je primárně způsobena stratum corneum a je rozhodující pro udržení zdravý kůže.[23] Hydratace pokožky je kvantifikována pomocí korneometrie.[24] Lipidy uspořádané prostřednictvím a spád a organizovaným způsobem mezi buňkami stratum corneum tvoří bariéru transepidermální ztráta vody.[25][26]
Barva kůže
Částka a rozdělení melanin pigment v epidermis je hlavním důvodem pro změnu v barva kůže v Homo sapiens. Melanin se nachází v malém melanosomy, částice vytvořené v melanocytech, odkud jsou přeneseny do okolních keratinocytů. Velikost, počet a uspořádání melanosomů se mezi rasovými skupinami liší, ale zatímco počet melanocytů se může mezi různými oblastmi těla lišit, jejich počet zůstává stejný v jednotlivých oblastech těla u všech lidí. U bílé a asijské kůže jsou melanosomy zabaleny do „agregátů“, ale u černé kůže jsou větší a distribuovány rovnoměrněji. Počet melanosomů v keratinocytech se zvyšuje s UV záření jejich distribuce zůstávají do značné míry nedotčeny.[27]
Klinický význam
Laboratoř kultura keratinocytů k vytvoření 3D struktury (umělá kůže ) rekapitulace většiny vlastností epidermis se běžně používá jako nástroj pro lék vývoj a testování.
Hyperplazie
Epidermální hyperplazie (zahušťování vyplývající z proliferace buněk ) má různé formy:
- Akantóza je rozptýlený epidermální hyperplazie (zesílení kůže, a nezaměňovat s akantocyty ).[28] To znamená větší tloušťku Malpighianská vrstva (stratum basale a stratum spinosum ).[29] Acanthosis nigricans je černá, špatně definovaná, sametová hyperpigmentovaný akantóza, obvykle pozorovaná v zadní části krku, podpaží a dalších složených oblastech kůže.
- Fokální hyperplazie epitelu (Heckova choroba) je asymptomatický, benigní neoplastický stav charakterizovaný mnoha bílými až růžovými papuly které se vyskytují difúzně v ústní dutině.[30][6]:411
- Pseudoepitheliomatous hyperplasia (PEH) je benigní stav charakterizovaný hyperplazií epidermis a epitelu kožní přídavky,[31] s nepravidelnými dlaždicovými prameny sahajícími dolů do dermis,[32] a důkladně simulující spinocelulární karcinom (SCC).[31]

Pseudoepitheliomatous hyperplasia (PEH), malé zvětšení, s acanthotic dlaždicového epitelu s nepravidelnými tlustými prsty jako downgrowths do podkladové dermis.
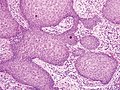
PEH, vysoké zvětšení, s reaktivně se objevujícími plochými výrůstky bez významné cytologické atypie.
Ve smlouvě, hyperkeratóza je zahuštění stratum corneum, a nemusí to nutně být způsobeno hyperplazií.
Další obrázky
Epidermis a dermis lidské kůže
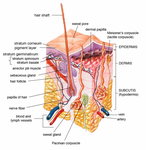
Průřez všech vrstev kůže

Ilustrace epidermálních vrstev

Optická koherentní tomografie konečku prstu
Viz také
Reference
- ^ Young, Barbara (2014). Wheatova funkční histologie a textový a barevný atlas. Elsevier. 160 a 175. ISBN 9780702047473.
- ^ A b C Marks, James G; Miller, Jeffery (2006). Lookingbill a Marksovy principy dermatologie (4. vydání). Elsevier. s. 1–7. ISBN 978-1-4160-3185-7.
- ^ A b C d E F Proksch, E .; Brandner, J .; Jensen, J.M. (2008). "Kůže: nepostradatelná bariéra". Experimentální dermatologie. 17 (12): 1063–1072. doi:10.1111 / j.1600-0625.2008.00786.x. PMID 19043850. S2CID 31353914.
- ^ A b C d McGrath, J. A.; Eady, R. A.; Papež, F.M. (2004). Rookova učebnice dermatologie (7. vydání). Blackwell Publishing. str. 3.1–3.6. ISBN 978-0-632-06429-8.
- ^ A b C Hanukoglu I, Boggula VR, Vaknine H, Sharma S, Kleyman T, Hanukoglu A (leden 2017). "Exprese epiteliálního sodíkového kanálu (ENaC) a CFTR v lidské epidermis a epidermálních přídavcích". Histochemie a buněčná biologie. 147 (6): 733–748. doi:10.1007 / s00418-016-1535-3. PMID 28130590. S2CID 8504408.
- ^ A b James, William D .; Berger, Timothy G .; et al. (2006). Andrewsovy nemoci kůže: klinická dermatologie. Saunders Elsevier. ISBN 0-7216-2921-0.
- ^ TheFreeDictionary> rete ridge Citace: The American Heritage Medical Dictionary Copyright 2007, 2004
- ^ Stücker, M; Struk, A; Altmeyer, P; Herde, M; Baumgärtl, H; Lübbers, DW (2002). „Kožní absorpce kyslíku v atmosféře významně přispívá k dodávce kyslíku do lidské dermis a epidermis“. The Journal of Physiology. 538 (3): 985–994. doi:10.1113 / jphysiol.2001.013067. PMC 2290093. PMID 11826181.
- ^ Stárnutí kůže - struktura
- ^ A b C d "Prosím aktualizujte" (PDF). Archivovány od originál (PDF) dne 14.12.2010. Citováno 2015-01-07.
- ^ A b C d E Elias, P.M. (2007). "Kožní bariéra jako vrozený imunitní prvek". Semináře z imunopatologie. 29 (1): 3–14. doi:10.1007 / s00281-007-0060-9. PMID 17621950. S2CID 20311780.
- ^ Iizuka, Hajime (1994). "Doba epidermálního obratu". Journal of Dermatological Science. 8 (3): 215–217. doi:10.1016/0923-1811(94)90057-4. PMID 7865480.
- ^ Hennings, H; Kruszewski, FH; Yuspa, SH; Tucker, RW (1989). „Intracelulární změny vápníku v reakci na zvýšení vnějšího vápníku v normálních a neoplastických keratinocytech“. Karcinogeneze. 10 (4): 777–80. doi:10.1093 / carcin / 10.4.777. PMID 2702726.
- ^ Pillai, S; Bikle, DD (1991). „Role vápníku bez intracelulárních buněk v tvorbě zrohovatělé obálky keratinocytů: Rozdíly v mechanismu působení extracelulárního vápníku a 1,25 dihydroxyvitaminu D3.“ Journal of Cellular Physiology. 146 (1): 94–100. doi:10.1002 / jcp.1041460113. PMID 1990023. S2CID 21264605.
- ^ Reiss, M; Lipsey, LR; Zhou, ZL (1991). „Extracelulární na vápníku závislá regulace transmembránových toků vápníku v myších keratinocytech“. Journal of Cellular Physiology. 147 (2): 281–91. doi:10.1002 / jcp.1041470213. PMID 1645742. S2CID 25858560.
- ^ Mauro, TM; Pappone, PA; Isseroff, RR (1990). „Extracelulární vápník ovlivňuje membránové proudy kultivovaných lidských keratinocytů“. Journal of Cellular Physiology. 143 (1): 13–20. doi:10.1002 / jcp.1041430103. PMID 1690740. S2CID 8072916.
- ^ Mauro, TM; Vydávání, RR; Lasarow, R; Pappone, PA (1993). "Ionové kanály jsou spojeny s diferenciací v keratinocytech". The Journal of Membrane Biology. 132 (3): 201–9. doi:10.1007 / BF00235738. PMID 7684087. S2CID 13063458.
- ^ Tu, CL; Oda, Y; Bikle, DD (1999). "Účinky aktivátoru vápníkového receptoru na buněčnou reakci na vápník v lidských keratinocytech". The Journal of Investigative Dermatology. 113 (3): 340–5. doi:10.1046 / j.1523-1747.1999.00698.x. PMID 10469331.
- ^ A b C Gilbert, Scott F (2000). „Epidermis a původ kožních struktur“. Vývojová biologie. Sinauer Associates. ISBN 978-0-87893-243-6.
- ^ Weschler, Charles J. (8. dubna 2011). „Skvalen a cholesterol v prachu z dánských domovů a center denní péče“ (PDF). Environ. Sci. Technol. 45 (9): 3872–3879. Bibcode:2011EnST ... 45,3872 W.. doi:10.1021 / es103894r. PMID 21476540.
- ^ Denda, M .; Tsuchiya, T .; Elias, P.M .; Feingold, K.R. (2000). "Stres mění homeostázu bariéry kožní permeability". Am J Physiol Regul Integr Comp Compiol. 278 (2): R367–372. doi:10.1152 / ajpregu.2000.278.2.R367. PMID 10666137. S2CID 558526.
- ^ Tsai, Jui-Chen; Guy, Richard H .; Thornfeldt, Carl R .; Gao, Wen Ni; Feingold, Kenneth R .; Elias, Peter M. (1996). „Metabolické přístupy ke zvýšení transdermálního podávání léků. 1. Účinek inhibitorů syntézy lipidů“. Journal of Pharmaceutical Sciences. 85 (6): 643–648. doi:10.1021 / js950219p. PMID 8773963.
- ^ Blank, IH (1952). "Faktory, které ovlivňují obsah vody ve stratum corneum". The Journal of Investigative Dermatology. 18 (6): 433–40. doi:10.1038 / jid.1952.52. PMID 14938659.
- ^ C. W. Blichmann, J. Serup: Posouzení vlhkosti pokožkyActa Derm. Venereol. (Stockli) 1988; 68: 284–290
- ^ Downing, DT; Stewart, ME; Wertz, PW; Colton, SW; Abraham, W; Strauss, JS (1987). "Kožní lipidy: aktualizace". The Journal of Investigative Dermatology. 88 (3 doplňky): 2 s – 6 s. doi:10.1111 / 1523-1747.ep12468850. PMID 2950180.
- ^ Bonté, F; Saunois, A; Pinguet, P; Meybeck, A (1997). „Existence lipidového gradientu v horní stratum corneum a jeho možný biologický význam“. Archiv dermatologického výzkumu. 289 (2): 78–82. doi:10,1007 / s004030050158. PMID 9049040. S2CID 10787600.
- ^ Montagna, William; Prota, Giuseppe; Kenney, John A. (1993). Černá kůže: struktura a funkce. Gulf Professional Publishing. str. 69. ISBN 978-0-12-505260-3.
- ^ Kumar, Vinay; Fausto, Nelso; Abbas, Abul (2004) Robbins & Cotran Pathologic Basis of Disease (7. vydání). Saunders. Stránka 1230. ISBN 0-7216-0187-1.
- ^ M. S. Stone; T. L. Ray (září 1995). "Acanthosis". DermPathTutor. Ústav dermatologie, University of Iowa. Archivovány od originál dne 29. května 2012. Citováno 17. května 2012.
- ^ Tenore, G .; Palaia, G .; Del Vecchio, A .; Galanakis, A .; Romeo, U. (2013-10-24). „Fokální hyperplazie epitelu (Heckova choroba)“. Annali di Stomatologia. 4 (Suppl 2): 43. ISSN 1824-0852. PMC 3860189. PMID 24353818.
- ^ A b Chakrabarti, Suvadip; Chakrabarti, PreetiRihal; Agrawal, Deepak; Somanath, Shreyas (2014). „Pseudoepitheliomatous hyperplasia: a Clinical entity misgot for spinoous cell carcinoma“. Journal of Kožní a estetická chirurgie. 7 (4): 232–4. doi:10.4103/0974-2077.150787. ISSN 0974-2077. PMC 4338470. PMID 25722605.
- ^ Lynch, Jane M. (2004). "Porozumění pseudoepiteliomatózní hyperplazii". Recenze případů patologie. 9 (2): 36–45. doi:10.1097 / 01.pcr.0000117275.18471.5f. ISSN 1082-9784. S2CID 71497554.








