Difenylfosfin - Diphenylphosphine
 | |
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC difenylfosfan | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.011.447 |
| Číslo ES |
|
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C12H11P | |
| Molární hmotnost | 186,19 g / mol |
| Vzhled | bezbarvá kapalina |
| Hustota | 1,07 g / cm3, kapalný |
| Bod varu | 280 ° C (536 ° F; 553 K) |
| Nerozpustný | |
| Nebezpečí | |
| Bezpečnostní list | Externí bezpečnostní list |
| Piktogramy GHS |   |
| Signální slovo GHS | Nebezpečí |
| H250, H315, H319, H335 | |
| P210, P222, P261, P264, P271, P280, P302 + 334, P302 + 352, P304 + 340, P305 + 351 + 338, P312, P321, P332 + 313, P337 + 313, P362, P370 + 378, P403 + 233, P405, P422, P501 | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
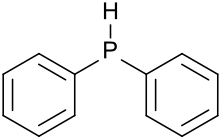
Difenylfosfin, také známý jako difenylfosfan, je organofosforová sloučenina se vzorcem (C6H5)2PH. Tato páchnoucí bezbarvá kapalina se snadno oxiduje na vzduchu. Je předchůdcem organofosforových ligandů pro použití jako katalyzátory.
Syntéza
Difenylfosfin lze připravit z trifenylfosfin snížením na difenylfosfid lithný, kterou lze protonovat, čímž se získá sloučenina uvedená v názvu:[1]
- PPh3 + 2 Li → LiPPh2 + LiPh
- LiPPh2 + H2O → Ph2PH + LiOH
Použití a reakce
V laboratoři je běžným meziproduktem difenylfosfin. Může být deprotonován za vzniku derivátů difenylfosfidu:[2]
- Ph2PH + nBuLi → Ph2PLi + nBuH
Příprava fosfinu ligandy, Wittig-Hornerova činidla, a fosfoniové soli se běžně provádí alkylací difenylfosfinu. Atom vodíku připojený k fosforu prochází Michaelovým přídavkem k aktivovaným alkenům, což poskytuje produkty, pomocí kterých se vyrábějí fosfinové ligandy, jako je 1,2-bis (difenylfosfino) ethan (Ph2PC2H4PPh2). Difenylfosfin a zejména deriváty difenylfosfidu jsou nukleofily, takže přispívají k dvojným vazbám uhlík - heteroatom.[2] Například v přítomnosti koncentrované kyseliny chlorovodíkové při 100 ° C se difenylfosfin přidává k atomu uhlíku v benzaldehyd čímž se získá (fenyl- (fenylmethyl) fosforyl) benzen.
- Ph2PH + PhCHO → Ph2P (O) CH2Ph
Ve srovnání s terciárními fosfiny je difenylfosfin slabě zásaditý. PKa protonovaného derivátu je 0,03:[3]
- Ph2PH2+ ⇌ Ph2PH + H+
Vlastnosti manipulace
Difenylfosfin snadno oxiduje.[4]
- Ph2PH + O2 → Ph2P (O) OH
Meziprodukt v této oxidaci je difenylfosfinoxid. Použití komplexu difenylfosfin-boran, Ph2PH • BH3 vyhýbá se problému oxidace fosfinu ochranou fosfinu před oxidací a je k dispozici u prodejců chemických látek.[2]
Reference
- ^ V. D. Bianco; S. Doronzo (1976). "Difenylfosfin". Anorganické syntézy. 16: 161–188. doi:10.1002 / 9780470132470.ch43.
- ^ A b C Piotrowski, D. W. (2001). "Difenylfosfin". Encyklopedie činidel pro organickou syntézu. New York: John Wiley & Sons. doi:10.1002 / 047084289X.rd427.
- ^ C. A. Streuli, "Stanovení bazicity substituovaných fosfinů pomocí nevodné titrace", Analytical Chemistry 1960, svazek 32, strany 985-987.doi:10.1021 / ac60164a027
- ^ Svara, J .; Weferling, N .; Hofmann, T. "Fosforové sloučeniny, organické". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a19_545.pub2.
