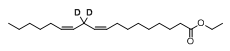
Ethylester di-deuterované kyseliny linolové - Di-deuterated linoleic acid ethyl ester
 | |
| Klinické údaje | |
|---|---|
| Trasy z správa | Ústní |
| ATC kód |
|
| Právní status | |
| Právní status |
|
| Identifikátory | |
| |
| Číslo CAS | |
| PubChem CID | |
| UNII | |
| Chemické a fyzikální údaje | |
| Vzorec | C20H34D2Ó2 |
| Molární hmotnost | 310.517 g · mol−1 |
| 3D model (JSmol ) | |
| Hustota | 0,88 g / cm3 |
| Bod varu | 173–177 ° C (343–351 ° F) |
| |
| |
| | |
Di-deuterovaný ethyl linoleát (také známý jako RT001; ethylester kyseliny linolové di-deuterované linolové kyseliny, 11,11-d2-ethyl linoleát, ethyl 11,11-d2-linoleát)[1] je experimentální, orálně biologicky dostupný syntetický deuterát polynenasycená mastná kyselina (PUFA), izotopolog esenciálního omega-6 PUFA, kyselina linolová. The deuterovaný sloučenina, i když je identická s přírodní kyselinou linolovou, je rezistentní vůči peroxidace lipidů který dělá studie jeho ochrana buněk vlastnosti stojí za to.
Mechanismus účinku
Kyselina di-deuterovaná linolová je buňkami rozpoznávána jako identická s přírodní kyselinou linolovou. Po absorpci se ale převede na kyselinu 13,13-D2-arachidonovou, těžkou izotopovou verzi kyselina arachidonová, který je začleněn do lipidových membrán. Deuterovaná sloučenina odolává neenzymatickým látkám peroxidace lipidů (LPO) prostřednictvím mechanismu bez antioxidačního účinku, který chrání mitochondriální, neuronové a jiné lipidové membrány, čímž výrazně snižuje hladinu mnoha toxických produktů odvozených od LPO, jako jsou reaktivní karbonyly.[2][3]
Klinický vývoj
Friedreichova ataxie
Dvojitě slepý komparátorem řízený Klinická studie fáze I / II pro Friedreichova ataxie, sponzorováno Retrotop a Friedreichova aliance pro výzkum ataxie, bylo provedeno za účelem stanovení bezpečnostního profilu a vhodného dávkování pro následné studie.[4] RT001 byl okamžitě absorbován a bylo zjištěno, že je bezpečný a tolerovatelný po dobu 28 dnů při maximální dávce 9 g / den. Zlepšilo se to špičková pracovní zátěž a maximální spotřeba kyslíku v testované skupině ve srovnání s kontrolní skupinou, která dostávala stejné dávky normálního nedeuterovaného ethyl linoleátu.[5] Další randomizovaná, dvojitě zaslepená, placebem kontrolovaná klinická studie začala v roce 2019.[6]
Infantilní neuroaxonální dystrofie
Otevřená klinická studie pro infantilní neuroaxonální dystrofie hodnocení dlouhodobého hodnocení účinnosti, bezpečnosti, snášenlivosti a farmakokinetiky přípravku RT001, který, pokud je užíván s jídlem, může chránit neuronální buňky před degenerací, bylo zahájeno v létě 2018.[7]
Neurodegenerace spojená s fosfolipázou 2G6
V roce 2017 FDA udělen RT001 lék na vzácná onemocnění označení při zacházení s fosfolipáza 2G6 - související neurodegenerace (PLÁN ).[8]
Amyotrofní laterální skleróza
V roce 2018 byla RT001 podána pacientovi s Amyotrofní laterální skleróza (ALS) v rámci „systému soucitu použití“.[9]
Progresivní supranukleární obrna
V roce 2020 FDA udělil léku na vzácná onemocnění označení RT001 pro léčbu pacientů s progresivní supranukleární obrna (PSP). PSP je onemocnění zahrnující modifikaci a dysfunkci tau proteinu; Mechanismus účinku RT001 jak snižuje peroxidaci lipidů, tak zabraňuje smrti neuronů mitochondriálními buňkami, což je spojeno s nástupem a progresí nemoci.[10]
Předklinický výzkum
Alzheimerova choroba
RT001 se ukázal jako účinný v modelu Alzheimerova choroba u myší.[11]
Reference
- ^ „Ethylester kyseliny 9-cis, 12-cis-11,11-D2-linolové“. PubChem.
- ^ Hill S, Lamberson CR, Xu L, To R, Tsui HS, Shmanai VV a kol. (Srpen 2012). „Malé množství polynenasycených mastných kyselin vyztužených izotopy potlačuje autoxidaci lipidů“. Radikální biologie a medicína zdarma. 53 (4): 893–906. doi:10.1016 / j.freeradbiomed.2012.06.004. PMC 3437768. PMID 22705367.
- ^ Demidov, Vadim V. (duben 2020). „Místně specificky deuterované esenciální lipidy jako nové léky proti neuronové, retinální a vaskulární degeneraci“. Objev drog dnes. doi:10.1016 / j.drudis.2020.03.014. PMID 32247036.
- ^ Číslo klinického hodnocení NCT02445794 pro „První v lidské studii RT001 u pacientů s Friedreichovou ataxií“ na ClinicalTrials.gov
- ^ Zesiewicz T, Heerinckx F, De Jager R, Omidvar O, Kilpatrick M, Shaw J, Shchepinov MS (červenec 2018). „Randomizovaná, klinická studie RT001: Časné signály účinnosti při Friedreichově ataxii“. Poruchy pohybu. 33 (6): 1000–1005. doi:10,1002 / mds.27353. PMID 29624723.
- ^ Číslo klinického hodnocení NCT04102501 pro „Studii k hodnocení účinnosti, dlouhodobé bezpečnosti a snášenlivosti RT001 u subjektů s Friedreichovou ataxií“ na ClinicalTrials.gov
- ^ Číslo klinického hodnocení NCT03570931 pro „Studii k hodnocení účinnosti a bezpečnosti RT001 u subjektů s infantilní neuroaxonální dystrofií“ na ClinicalTrials.gov
- ^ „FDA USA uděluje označení léčivých přípravků pro vzácná onemocnění pro retrotopovou RT001 při léčbě neurodegenerace asociované s fosfolipázou 2G6 (PLA2G6)“. Globální Newswire. 2. listopadu 2017.
- ^ Inacio P (2018-09-18). „Experimentální RT001 nyní k dispozici pro ALS v rámci rozšířeného přístupu“. ALS News Today.
- ^ https://www.neurologylive.com/clinical-focus/rt001-gets-orphan-drug-designation-in-progressive-supranuclear-palsy-
- ^ Butterfield DA, Halliwell B (březen 2019). „Oxidační stres, nefunkční metabolismus glukózy a Alzheimerova choroba“. Recenze přírody. Neurovědy. 20 (3): 148–160. doi:10.1038 / s41583-019-0132-6. PMID 30737462.

