Cyclododecahexaene - Cyclododecahexaene
tento článek potřebuje další citace pro ověření. (Srpna 2011) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
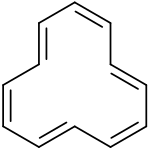 Tri-trans izomer cyklododekahexaenu | |
| Jména | |
|---|---|
| Název IUPAC 1,3,5,7,9,11-Cyclododecahexaene | |
| Ostatní jména [12] annulen | |
| Identifikátory | |
3D model (JSmol ) | |
PubChem CID | |
| |
| |
| Vlastnosti | |
| C12H12 | |
| Molární hmotnost | 156.228 g · mol−1 |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Cyclododecahexaene nebo [12] annulen (C12H12) je členem řady annulenes s určitým zájmem o organická chemie s ohledem na studium aromatičnost.[1] Cyclododecahexaene je nearomatický kvůli nedostatku rovinnosti struktury.[Citace je zapotřebí ] Na druhou stranu di-anion se 14 elektrony je a Hückel aromat a stabilnější.
Podle in silico experimentujetrans izomer Očekává se, že bude nejstabilnější, následovaný 1,7-ditrans a všemi cis-izomery (+1 kcal / mol) a 1,5-ditrans-izomerem (+5 kcal / mol).
První [12] annulen s konfigurací sym-tri-trans byl syntetizován v roce 1970 z tricyklického předchůdce fotolýza při nízkých teplotách. Při zahřívání směsi se přeskupí na bicyklické [6,4,0] izomer. Snižování sloučenina při nízkých teplotách umožnila analýzu dianionu pomocí protonová NMR s vnitřními protony rezonujícími - 4,5 ppm vzhledem k TMS, důkaz o aromatický diamagnetický kruhový proud.[2]
V jedné studii je 1,7-ditrans izomer generován při nízkých teplotách v THF podle dehydrohalogenace hexabromcyklododekanu s draslík tert-butoxid. Redukce této sloučeniny při nízké teplotě s cesium kov vede nejprve k radikální anion a pak na dianion. The chemický posun pro vnitřní protony v této sloučenině je s +0,2 ppm mnohem skromnější než v tri-trans izomeru.
Zahřívání roztoku radikálových iontů na pokojová teplota vede ke ztrátě jednoho ekvivalentu vodíku a tvorbě heptalen radikální anion.
Reference
- ^ Kiesewetter, Matthew K .; Gard, Matthew N .; Reiter, Richard C .; Stevenson, Cheryl D. (2006). „Reakce zahrnující di-trans- [12] annuleny“. Journal of the American Chemical Society. 128 (49): 15618–15624. doi:10.1021 / ja062846u. PMID 17147369.
- ^ Oth, J. F. M .; Schröder, G. (1971). "Annulenes. Část XII. Dianion [12] annulene". J. Chem. Soc. B. 0: 904–907. doi:10.1039 / j29710000904. ISSN 0045-6470.

![[12] syntéza annulenu](http://upload.wikimedia.org/wikipedia/commons/thumb/4/4a/12-annulene.svg/500px-12-annulene.svg.png)
![[12] syntéza annulenu](http://upload.wikimedia.org/wikipedia/commons/thumb/d/db/12annulene2006.png/400px-12annulene2006.png)