Canaline - Canaline
 | |
| Jména | |
|---|---|
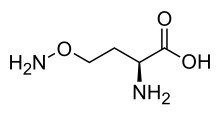
| Název IUPAC (2S) -2-Amino-4-aminooxybutanová kyselina | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| KEGG | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C4H10N2Ó3 | |
| Molární hmotnost | 134.135 g · mol−1 |
| Hustota | 1,298 g / ml |
| Bod tání | 213 ° C |
| Bod varu | 378,1 ° C (712,6 ° F; 651,2 K) |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
l-Canalin (Název IUPAC 2-amino-4- (aminooxy) máselná kyselina)) je non-proteinogenní aminokyselina. Sloučenina se nachází v luštěniny které obsahují kanavanin, ze kterého je vyroben působením argináza. Nejčastěji používaným zdrojem této aminokyseliny je jack fazole, Canavalia ensiformis.
l-Canalin je jediná známá přirozeně se vyskytující aminokyselina, která má Ó-alkyl hydroxylamin funkčnost v bočním řetězci. Tato aminokyselina strukturně souvisí s ornitin (je to derivát 5-oxa) a je silný insekticid. Tabákový hornworm larvy krmené dietou obsahující 2,5 mM kanál vykazovaly masivní vývojové aberace a většina takto ošetřených larev uhynula ve stádiu kukly. Rovněž vykazuje silné neurotoxické účinky na můru.
Jeho toxicita pramení především ze skutečnosti, že se snadno tvoří oximy s ketokyselinami a aldehydy, zejména pyridoxal fosfát kofaktor mnoha vitaminů B.6-závislé enzymy. Inhibuje to ornitinaminotransferáza při koncentracích pouhých 10 nM.
l-Canalin je substrát pro ornitinaminotransferáza což má za následek syntézu l-ureidohomoserin (odpovídající analog l-citrulin). Na druhé straně se tvoří druhá l-kyselina kanavaninosukcinová v reakci zprostředkované syntetáza kyseliny argininosukcinové. lKyselina kanavaninosukcinová se štěpí za vzniku l-kanavanin syntetázou kyseliny argininosukcinové. Těmito sekvenčními reakcemi se vytváří kanaline-močovinový cyklus (analogický s ornithin-močovinovým cyklem). Pokaždé, když molekula kanavaninu prochází cyklem kanaline-močovina, jsou dva koncové atomy dusíku uvolňovány jako močovina. Močovina je důležitým vedlejším produktem této reakční sekvence, protože vytváří amoniakální amoniak (zprostředkovaný ureázou), který je k dispozici pro podporu intermediárního metabolismu dusíku. l-Canalin může být redukčně štěpen l-homoserin, nebílkovinová aminokyselina, která má velký význam při tvorbě hostitele esenciálních aminokyselin. Tímto způsobem vstoupí třetí atom dusíku kanavaninu do reakcí metabolismu dusíku v rostlině. Jako homoserin má důležité využití také jeho uhlíková kostra.
Reference
- Rosenthal, Gerald A. (1982). Rostlinné neproteinové aminokyseliny a imino kyseliny: biologické, biochemické a toxikologické vlastnosti. Boston: Academic Press. ISBN 0-12-597780-8.[stránka potřebná ]
