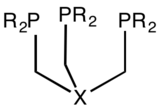
Stativový ligand - Tripodal ligand

Trojnohé ligandy jsou tri- a tetradentát ligandy s C.3 symetrie. Jsou populární ve výzkumu v oblastech koordinační chemie a homogenní katalýza. Jelikož jsou ligandy polydentátové, nedochází snadno k jejich disociaci od středu kovu.
Koordinační chemie
Při použití v koordinační komplexy s oktaedrická molekulární geometrie the trojzubec stativové ligandy zaujímají jednu tvář, což vede k fixaci obličeje (nebo fac) geometrie. The tetradentát trojnohé ligandy zabírají čtyři sousedící místa, přičemž dvě zůstávají cis pozice dostupné na oktaedrickém kovovém středu. Když jsou vázány na čtyř- a pět-souřadnicových kovových center, tyto ligandy ukládají C3 symetrie, což může vést k neobvyklosti ligandové pole štípací vzory. Tripodální ligandy jsou často schopné koordinovat saturaci kovových iontů nižšími koordinační čísla.
Jeden stativový ligand komerčního významu je nitrilotriacetát, N (CH2CO2−)3 protože je levně vyráběn a má vysokou afinitu k dvojmocným kovovým iontům. Mezi další trojnohé triaminové ligandy patří tren (N (CH2CH2NH2)3) a cis-1,3,5-triaminocyklohexan.[1] Určitý trifosfiny jako RC (CH2PPh2)3 jsou také stativové. Mnoho druhů dárcovských skupin bylo začleněno do ramen trojnohých ligandů, včetně amida (R.2N−),[2] a N-heterocyklické karbeny.
- Příklady stativových ligandů

Tris (2-pyridylmethyl) amin, tetradentátový trojnohý ligand populární v bioanorganická chemie.[5]
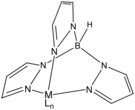
Struktura kovového komplexu trispyrazolylborát, aniontový trojsložkový ligand, protože simuluje tři imidazolové ligandy.[6]

NTA je komerčně důležitý trojnohý ligand. Jeho tři skupiny karboxylových kyselin procházejí po komplexaci deprotonací.
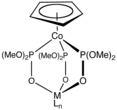
The Kläui ligand, dianiontový organokovový ligand.
Reference
- ^ Aimee J. Gamble, Jason M. Lynam, Robert J. Thatcher, Paul H. Walton, Adrian C. Whitwood (2013). „cis-1,3,5-Triaminocyklohexan jako ligand s omezením obličeje pro ruthenium (II)“. Inorg. Chem. 52: 4517–4527. doi:10.1021 / ic302819j.CS1 maint: používá parametr autoři (odkaz)
- ^ Verkade, J. G. (1993). "Atranes: Nové příklady s neočekávanými vlastnostmi". Acc. Chem. Res. 26: 483. doi:10.1021 / ar00033a005.
- ^ Schwarzenbach, Gerold; Bürgi, Hans-Beat; Jensen, William P .; Lawrance, Geoffrey A .; Mønsted, Lene; Sargeson, Alan M. (1983). „Kyselé štěpení komplexů niklu (Ii) s obsahem cis, cis-1,3,5-cyklohexanetriaminu (TACH), krystalové struktury [Ni (tach) (H2Ó)3](NE3)2a korelace mezi strukturou a reaktivitou nikl-polyaminových komplexů “. Anorganická chemie. 22 (26): 4029–4038. doi:10.1021 / ic00168a042.
- ^ Saouma, C. T., Peters, J. C. (2011). "M-E a M = E komplexy železa a kobaltu, které zdůrazňují trojí symetrii (E = O, N, NR)". Coord. Chem. Rev. 255: 920. doi:10.1016 / j.ccr.2011.01.009.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Blackman, A. G. (2008). "Tripodální tetraaminové ligandy obsahující tři pyridinové jednotky: další polypyridyl ligandy". Eur. J. Inorg. Chem.: 2633. doi:10.1002 / ejic.200800115.
- ^ Parkin, G. (2000). „Bioinorganic Chemistry of Zinc: Synthetic Analogues of Zinc Enzymes that Feature Tripodal Ligands“. Chemická komunikace: 1971-1985. doi:10.1039 / B004816J.