Prelog kmen - Prelog strain

v organická chemie, transanulární kmen (také zvaný Prelog kmen po chemikovi, který získal Nobelovu cenu Vladimír Prelog ) jsou nepříznivé interakce kruhových substituentů na nesousedících uhlících. Tyto interakce, nazývané transanulární interakce, vznikají z nedostatku prostoru uvnitř kruhu, což nutí substituenty do vzájemného konfliktu. Ve střední velikosti cykloalkany, které mají mezi 8 a 11 atomy uhlíku tvořícími prsten, může být transanulární deformace hlavním zdrojem overalu kmen, zejména u některých konformací, ke kterým také přispívá napětí pod velkým úhlem a Kmen Pitzer.[1][2] Ve větších prstencích transanulární deformace klesá, dokud kruh není dostatečně velký, aby mohl přijmout konformace bez negativních interakcí.[1][3]
Transanulární kmen lze také prokázat v jiných cykloorganických molekulách, jako je např laktony, laktamy, ethery, cykloalkeny, a cykloalkyny. Tyto sloučeniny nejsou bezvýznamné, protože jsou zvláště užitečné při studiu transanulárního kmene. Transanulární interakce navíc nejsou odsunuty pouze na konflikty mezi atomy vodíku, ale mohou také vzniknout z větších a složitějších substituentů interagujících napříč kruhem.
Termodynamika

Podle definice kmen znamená diskomfort, takže by mělo vyplývat, že molekuly s velkým množstvím transanulárního kmene by měly mít vyšší energie než ty bez nich. Cyklohexan je z velké části bez napětí, a proto je poměrně stabilní a má nízkou energii. Kroužky menší než cyklohexan, jako cyklopropan a cyklobutan, mají značné napětí způsobené napětí v malém úhlu, ale neexistuje transanulární napětí. I když ve středních prstencích není přítomno napětí v malém úhlu, existuje něco, co se nazývá napětí pod velkým úhlem. Některé úhlové a torzní namáhání používají kroužky s více než devíti členy k úlevě od nouze způsobené transannulárním namáháním.[1][3]
Jak naznačuje graf nalevo, relativní energie cykloalkanů se zvyšuje s rostoucí velikostí kruhu, s vrcholem u cyklononanu (s devíti členy v jeho kruhu). V tomto bodě se flexibilita kruhů zvyšuje s rostoucí velikostí; to umožňuje konformace, které mohou významně zmírnit transanulární interakce.[1]
Kinetika
| Druhy reakce | Prsteny | ||||||
|---|---|---|---|---|---|---|---|
| Malý | Normální | středně pokročilí | Velký | ||||
| 3- | 4- | 5- | 6- | 7- | 8-12 | 13- a větší | |
| SN1, SN2 a volný radikál | velmi pomalý | pomalý | rychle | pomalý | rychle | rychle | střední sazba |
| adice na karbonylovou skupinu | velmi rychle | rychle | pomalý | rychle | pomalý | pomalý | střední sazba |
Rychlost reakce může být ovlivněna velikostí prstenů. Každá reakce by měla být v zásadě studována případ od případu, ale byly pozorovány některé obecné trendy. Výpočty molekulární mechaniky rozdílů deformační energie SI mezi stavem sp2 a sp3 v cykloalkanech ukazují lineární korelace s rychlostí (jako logk) mnoha reakcí zahrnujících přechod mezi stavy sp2 a sp3, jako je redukce ketonu, oxidace alkoholu nebo nukleofilní substituce, příspěvek transanulární deformace je nižší než 3%. [4]
Kroužky s transanulární deformací mají rychlejší průběh SN1, SN2, a reakce volných radikálů ve srovnání s většinou menších a normálně velkých kroužků. Pětičlenné prsteny vykazují výjimku z tohoto trendu. Na druhou stranu někteří nukleofilní adice reakce zahrnující přidání do karbonylové skupiny obecně ukazují opačný trend. Menší a normální prstence, přičemž anomálií jsou pětičlenné prstence, mají rychlejší reakční rychlosti, zatímco ty s transanulární deformací jsou pomalejší.[5]

| n | k1 h−1 při 25 ° C | Relativní sazba |
|---|---|---|
| 4 | 0.00224 | 0.211 |
| 5 | 1.32 | 124 |
| 6 | 0.0106 | 1.00 |
| 7 | 1.15 | 108 |
| 8 | 3.03 | 286 |
| 9 | 0.465 | 43.9 |
| 10 | 0.188 | 17.7 |
| 11 | 0.127 | 12.0 |
| 13 | 0.0302 | 2.85 |
| 15 | 0.0192 | 1.81 |
| 17 | 0.0201 | 1.90 |
Jeden konkrétní příklad studie rychlostí reakcí pro S.N1 reakce je zobrazena vpravo. K porovnání relativních rychlostí a lepšímu pochopení vlivu transanulární deformace na tuto reakci byly použity kruhy různých velikostí, od čtyř do sedmnácti členů. The solvolýza reakce v kyselině octové zahrnovala vznik a karbokace když chloridový iont opouští cyklickou molekulu. Tato studie odpovídá obecnému trendu, který je vidět výše, že kroužky s transanulární deformací vykazují vyšší reakční rychlosti ve srovnání s menšími kroužky v S.N1 reakce.[5]
Příklady transanulární deformace
Vliv na regioselektivitu
The regioselektivita eliminace vody je silně ovlivněna velikostí prstence. Když je voda z cyklických terciárních alkoholů vylučována pomocí Trasa E1, jsou formovány tři hlavní produkty. Předpokládá se, že bude převládat semicyklický izomer (tzv. Protože dvojná vazba je sdílena atomem kruhu a exocyklickým atomem) a (E) endocyklický izomer; neočekává se, že se vytvoří (Z) endocyklický izomer, dokud velikost kruhu nebude dostatečně velká, aby pojala nepříjemné úhly trans konfigurace. Přesná populace každého produktu ve srovnání s ostatními se značně liší v závislosti na velikosti příslušného prstence. Jak se zvětšuje velikost kruhu, semicyklický izomer rychle klesá a (E) endocyklický izomer se zvyšuje, ale po určitém okamžiku se semicyklický izomer začne znovu zvyšovat. To lze připsat transannulární deformaci; tento kmen je významně redukován v (E) endocyklickém izomeru, protože má v kruhu jeden menší substituent než semicyklický izomer.[6]

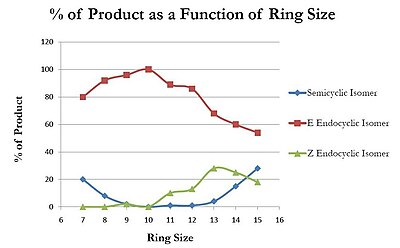
Vliv na středně velkou kruhovou syntézu
Jedním z účinků transanulárního kmene je obtížnost syntetizace středních prstenců. Illuminati a kol. studovali kinetika uzavření intramolekulárního kruhu pomocí jednoduché nukleofilní substituční reakce ortho-bromalkoxyfenoxidů. Konkrétně studovali uzavření kruhu 5 až 10 uhlíkových cyklických etherů. Zjistili, že se zvyšujícím se počtem uhlíků rostl i počet uhlíků entalpie aktivace reakce. To naznačuje, že napětí v cyklických přechodových stavech je vyšší, pokud je v kruhu více uhlíků. Vzhledem k tomu, že transannulární kmen je největším zdrojem kmene v prstencích této velikosti, mají větší entalpie aktivace za následek mnohem pomalejší cyklizaci v důsledku transanulární interakce v cyklických etherech.[7]
Vliv mostů na transanulární napětí
Transanulární napětí lze eliminovat jednoduchým přidáním uhlíkového můstku. E, Z, E, Z, Z- [10] -annulen je docela nestabilní; zatímco má požadovaný počet π-elektronů, aby byl aromatický, jsou z velké části izolovány. Nakonec je samotná molekula velmi těžko pozorovatelná. Avšak jednoduchým přidáním methylenového můstku mezi polohami 1 a 6 lze vytvořit a pozorovat stabilní, plochou, aromatickou molekulu.[8]

Reference
- ^ A b C d Smith a March, March's Advanced Organic Chemistry, John Wiley & Sons Inc., 2007, ISBN 978-0-471-72091-1
- ^ Raphael, R.A. (1962). „Proceedings of the Chemical Society. March 1962“. Proc. Chem. Soc.: 97. doi:10.1039 / PS9620000097.
- ^ A b Anslyn a Dougherty, Moderní fyzikální organická chemie, University Science Books, 2006, ISBN 978-1-891389-31-3
- ^ Schneider, H.-J .; Schmidt, G .; Thomas F. J. Am. Chem. Soc., 1983, 105, 3556.https://pubs.acs.org/doi/pdf/10.1021/ja00349a031
- ^ A b C Goldfarb; Belenkii (1960). "Kmen a reaktivita v monocyklických systémech". Ruské chemické recenze. 29 (4): 214–235. Bibcode:1960RuCRv..29..214G. doi:10.1070 / RC1960v029n04ABEH001228.
- ^ Greve a Imming .; Imming, Peter (1997). „Regio- a stereoselektivita eliminace vody jako funkce velikosti prstence“. J. Org. Chem. 62 (23): 8058. doi:10.1021 / jo970989g.
- ^ Ilumináti; et al. (1975). "Reakce uzavření kruhu. V. Kinetika tvorby pětičlenného až desetičlenného kruhu z o-o-bromalkylfenoxidů. Vliv O-heteroatomu.". JACS. 97 (17): 4961. doi:10.1021 / ja00850a032.
- ^ Slayden a Liebman. (2001). „Energetika aromatických uhlovodíků: experimentální termochemická perspektiva“. Chem. Rev. 101 (5): 1541–66. doi:10.1021 / cr990324 +. PMID 11710232.
externí odkazy
- Definice kmene Prelog: Odkaz
- IUPAC, Kompendium chemické terminologie, 2. vyd. („Zlatá kniha“) (1997). Online opravená verze: (2006–) “transanulární kmen ". doi:10.1351 / goldbook.T06434
