Porfin - Porphine
 | |
 | |
| Jména | |
|---|---|
| Ostatní jména Porfín | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
| Informační karta ECHA | 100.002.690 |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C20H14N4 | |
| Molární hmotnost | 310,35 196 g / mol |
| Vzhled | Tmavě červené, lesklé letáky |
| Bod tání | N / A |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
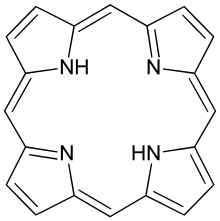
Porfin nebo porfín je organická chemická sloučenina se vzorcem C
20H
14N
4. Molekula se skládá ze čtyř pyrrol -jako prsteny spojené čtyřmi methinu (=CH -) skupiny tvoří větší makrocyklus prsten, což je nejjednodušší z tetrapyrroly. Je to aromatický a heterocyklický sloučenina, pevná látka při teplotě místnosti.[1]
Porfin se v přírodě nevyskytuje a je téměř pouze teoretický; substituované deriváty však zahrnují mnoho biochemicky významných sloučenin nazývaných porfyriny, přičemž dominantním příkladem je protoporfyrin IX.[2] Je také známo mnoho syntetických analogů, včetně oktaethylporfyrin[3] a tetrafenylporfyrin.[4]
Strukturní charakteristiky porfinu a jeho derivátů
- Běžné porfyriny
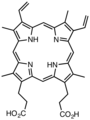
Deriváty protoporfyrin IX jsou v přírodě běžné, předchůdce lemy.

Oktaethylporfyrin (H2OEP) je syntetický analog protoporfyrinu IX. Na rozdíl od přírodních porfyrinových ligandů, OEP2− je vysoce symetrický.

Tetraphenylporphyrin (H2TPP) je další syntetický analog protoporfyrinu IX. Na rozdíl od přírodních porfyrinových ligandů, TPP2− je vysoce symetrický. Dalším rozdílem je, že jeho metinová centra jsou obsazena fenylovými skupinami.
Porfin je rovinný. Dvě centra NH jsou trans.

Komplex s kovem uprostřed
Souběžně s posunem dvou N-H protony, porfin váže kovové ionty ve svém středu. Zasunutí kovového středu je pomalé bez přítomnosti katalyzátorů. V přírodě se tyto katalyzátory (enzymy) nazývají chelatázy. Pokud ve středu není na dusíky vázán žádný kovový ion (nebo atom), pak se sloučeniny nazývají volný porfin nebo volný porfyrin. Pokud jsou spojeny s kovem ve středu, pak jsou vázaný. Porfyrin s atomem železa typu nalezeného v myoglobin, hemoglobin nebo jisté cytochromy je nazýván heme. Viz Porfyrin článek pro další podrobnosti.
Sloučeniny podobné porfinu jsou původní sloučeniny pro podobné kruhové systémy s jinými centrálními atomy kovů v biochemii. Tyto zahrnují chlor, který má hořčík ion v několika typech chlorofyl; bakteriochlorin, nalezen v bakteriochlorofyl; a corrin, který má kobalt centrum v kobalamin (vitamin B12 ).
Viz také
Další čtení
- Budavari, Susan (1989). "7574. Porfin". Index Merck (11. vydání). Merck & Co., Inc. str.1210. ISBN 0-911910-28-X. LCCN 89-60001.
Reference
- ^ „Porfyrin“. Encyklopedie anorganické a bioanorganické chemie. Wiley-VCH. 2011. doi:10.1002 / 9781119951438.eibd0638. ISBN 9781119951438.
- ^ Paul R. Ortiz de Montellano (2008). "Hemes v biologii". Wiley Encyclopedia of Chemical Biology. John Wiley & Sons. doi:10.1002 / 9780470048672.wecb221. ISBN 978-0470048672.
- ^ Jonathan L. Sessler; Azadeh Mozaffari; Martin R. Johnson (1992). „3,4-Diethylpyrol a 2,3,7,8,12,13,17,18-oktaethylporfyrin“. Org. Synth. 70: 68. doi:10.15227 / orgsyn.070.0068.
- ^ Lindsey, Jonathan S. (2000). "Syntéza meso-substituovaných porfyrinů". V Kadish, Karl M .; Smith, Kevin M .; Guilard, Roger (eds.). Příručka o porfyrinu. 1. str. 45–118. ISBN 0-12-393200-9.



