Molekulární rozpoznávání - Molecular recognition
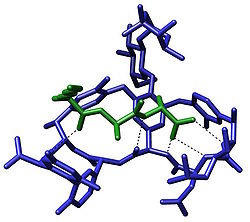


Termín molekulární rozpoznávání se týká specifické interakce mezi dvěma nebo více molekuly přes nekovalentní vazba jako vodíkové vazby, kovová koordinace, hydrofobní síly,[3][4] van der Waalsovy síly, Interakce π-π, halogenová vazba nebo rezonanční interakce[5] účinky. Kromě toho Přímo interakce mohou hrát dominantní roli rozpouštědla nepřímý role v řízení molekulárního rozpoznávání v řešení.[6][7] The hostitel a host podílí se na výstavě molekulárního rozpoznávání molekulární komplementarita. Výjimkou jsou molekulární kontejnery,[8][9] včetně např. nanotrubice, kde portály v zásadě řídí selektivitu.[10][11][12][13]
Biologické systémy

Molekulární rozpoznávání hraje důležitou roli v biologický systémů a je pozorován mezi receptorem-ligandem,[14][15] antigen -protilátka, DNA -protein, cukr -lektin, RNA -ribozom atd. Důležitým příkladem molekulárního rozpoznávání je antibiotikum vankomycin který se selektivně váže na peptidy s terminálním D-alanyl-D-alaninem v bakteriálních buňkách prostřednictvím pěti vodíkových vazeb. Vankomycin je pro bakterie smrtelný, protože jakmile se naváže na tyto konkrétní peptidy, nelze je použít ke konstrukci bakterií buněčná stěna.[Citace je zapotřebí ]
Syntetické molekulární rozpoznávání
Nedávná práce naznačuje, že prvky molekulárního rozpoznávání lze synteticky vyrobit v nanoměřítku,[16] obejít potřebu přirozeně se vyskytujících prvků rozpoznávání molekul pro vývoj snímacích nástrojů pro malé molekuly. Bio-mimetické polymery, jako jsou peptoidy, lze použít k rozpoznání větších biologických cílů, jako jsou proteiny [17] a konjugace polymerů na syntetické fluorescenční nanomateriály mohou generovat syntetické makromolekulární struktury, které slouží jako syntetické protilátky pro optické rozpoznávání a detekci proteinů.[18]
Supramolekulární systémy
Chemici prokázali, že mnoho umělých supramolekulární mohou být navrženy systémy, které vykazují molekulární rozpoznání.[19] Jedním z prvních příkladů takového systému je ethery koruny které jsou schopné selektivně vázat specifické kationty. Od té doby však byla zavedena řada umělých systémů.
Statický vs. dynamický
Molekulární rozpoznávání lze rozdělit na statické molekulární rozpoznávání a dynamické molekulární rozpoznávání. Statické molekulární rozpoznávání je přirovnáváno k interakci mezi klíčem a klíčovou dírkou; jedná se o komplexační reakci typu 1: 1 mezi hostitelskou molekulou a hostující molekulou za vzniku a komplex host – host. K dosažení pokročilého statického molekulárního rozpoznávání je nutné vytvořit rozpoznávací místa, která jsou specifická pro hostující molekuly.
V případě dynamického molekulárního rozpoznávání ovlivňuje vazba prvního hosta na první vazebné místo hostitele asociační konstantu druhého hosta s druhým vazebným místem. vedoucí k spolupráce vazby.[20] V případě pozitivních alosterických systémů vazba prvního hosta zvyšuje asociační konstantu druhého hosta. Zatímco u negativních alosterických systémů vazba prvního hosta snižuje asociační konstantu s druhým. Dynamická povaha tohoto typu molekulárního rozpoznávání je obzvláště důležitá, protože poskytuje mechanismus k regulaci vazby v biologických systémech. Dynamické molekulární rozpoznávání může zvýšit schopnost rozlišovat mezi několika konkurenčními cíli prostřednictvím konformační korektury mechanismus. Dynamické molekulární rozpoznávání se také studuje pro použití ve vysoce funkčních aplikacích chemické senzory a molekulární zařízení.
Složitost
Nedávná studie založená na molekulárních simulacích a konstantách shody popisuje molekulární rozpoznávání jako fenomén organizace. Dokonce ani u malých molekul, jako jsou sacharidy, nelze proces rozpoznávání předvídat ani navrhnout, a to ani za předpokladu, že síla každé jednotlivé vodíkové vazby je přesně známa.[21] Jak však Mobley et al.[22] dospěl k závěru, že přesná předpověď událostí molekulárního rozpoznávání musí jít nad rámec statického snímku jediného snímku mezi hostem a hostitelem. Entropie jsou klíčovými přispěvateli k vázání termodynamiky a je třeba je zohlednit, aby bylo možné přesněji předpovědět proces rozpoznávání.[23] Entropie jsou zřídka pozorovatelné v jednoduchých vázaných strukturách (statický snímek).
Intragenní komplementace
Jehle[24] poukázal na to, že když jsou ponořeny do kapaliny a smíchány s jinými molekulami, síly fluktuace náboje upřednostňují asociaci identických molekul jako nejbližších sousedů. V souladu s tímto principem je více kopií polypeptidu kódovaných a gen často procházejí vzájemným molekulárním rozpoznáváním a vytvářejí uspořádanou strukturu multi-polypeptidového proteinu. Když se takový protein vytvoří z polypeptidů produkovaných dvěma různými mutant alely konkrétního genu může protein složený ze směsi polypeptidů vykazovat větší funkční aktivitu než multi-polypeptidový protein vytvořený každou z mutantů samotných. V takovém případě je jev označován jako intragenní komplementace.
Intragenní komplementace (nazývaná také inter-alelická komplementace) byla prokázána v mnoha různých genech v různých organismech.[25] Crick a Orgel [26] analyzoval výsledky těchto studií a dospěl k závěru, že intragenní komplementace obecně vzniká z interakce různě defektních polypeptidových monomerů, když tvoří uspořádaný agregát, který nazývají „multimer“.
Viz také
- Journal of Molecular Recognition
- Výzva SAMPL
- Nekovalentní interakce
- Supramolekulární chemie
- Allostery
- Spolupráce
Reference
- ^ Knox, James R .; Pratt, R. F. (červenec 1990). "Různé způsoby vazby vankomycinu a D-alanyl-D-alanin peptidázy na peptid buněčné stěny a možná role proteinu rezistence na vankomycin" (Volný plný text). Antimikrobiální látky a chemoterapie. 34 (7): 1342–7. doi:10.1128 / AAC.34.7.1342. PMC 175978. PMID 2386365.
- ^ Bielawski, Christopher; Chen, Yuan-Shek; Zhang, Peng; Perst, Peggy-Jean; Moore, Jeffrey S. (1998). „Modulární přístup ke konstrukci vícemístných receptorů pro kyselinu isoftalovou“. Chemická komunikace. 0 (12): 1313–4. doi:10,1039 / a707262g.
- ^ Lockett, M. R.; Lange, H .; Breiten, B .; Heroux, A .; Sherman, W .; Rappoport, D .; Yau, P.O .; Snyder, P. W .; Whitesides, G. M. (2003). „Vazba benzoarylsulfonamidových ligandů na lidskou karboanhydrázu je necitlivá na formální fluoraci ligandu“. Angew. Chem. Int. Vyd. 52 (30): 7714–7717. doi:10,1002 / anie.201301813. PMID 23788494.
- ^ Breiten, B .; Lockett, M. R.; Sherman, W .; Fujita, S .; Al-Sayah, M .; Lange, H .; Bowers, C. M .; Heroux, A .; Krilov, G .; Whitesides, G. M. (2013). „Vodní sítě přispívají ke kompenzaci entalpie / entropie při vazbě na proteiny a ligandy“. J. Am. Chem. Soc. 135 (41): 15579–15584. CiteSeerX 10.1.1.646.8648. doi:10.1021 / ja4075776. PMID 24044696.
- ^ Cosic, I (1994). „Makromolekulární bioaktivita: je to rezonanční interakce mezi makromolekulami? - teorie a aplikace“. Transakce IEEE na biomedicínském inženýrství. 41 (12): 1101–14. doi:10.1109/10.335859. PMID 7851912.
- ^ Baron, Riccardo; Setny, Piotr; McCammon, J. Andrew (2010). „Voda v dutině - rozpoznávání ligandu“. Journal of the American Chemical Society. 132 (34): 12091–12097. doi:10.1021 / ja1050082. PMC 2933114. PMID 20695475.
- ^ Baron, Riccardo; McCammon, J. Andrew (2013). "Molekulární rozpoznávání a vazba ligandů". Roční přehled fyzikální chemie. 64: 151–175. Bibcode:2013ARPC ... 64..151B. doi:10.1146 / annurev-physchem-040412-110047. PMID 23473376.
- ^ Cram, D. J .; Cram, J. M. Kontejnerové molekuly a jejich hosté; Royal Society of Chemistry: Cambridge, 1997. ISBN 0851869726
- ^ Brotin, Thierry; Dutasta, Jean-Pierre (2009). „Kryptofany a jejich komplexy - současnost a budoucnost“. Chemické recenze. 109 (1): 88–130. doi:10.1021 / cr0680437. PMID 19086781.
- ^ Lehn, Jean-Marie (1995). Supramolekulární chemie. Weinheim: Wiley-VCH. ISBN 978-3-527-29312-4. OCLC 315928178.[stránka potřebná ]
- ^ Gellman, Samuel H. (1997). „Úvod: Molekulární rozpoznávání“. Chemické recenze. 97 (5): 1231–1232. doi:10.1021 / cr970328j. PMID 11851448.
- ^ Dipankar Chatterji, Základy molekulárního rozpoznávání , CRC Press; 2016, ISBN 1482219689
- ^ Molekulární rozpoznávání a polymery: Řízení struktury polymerů a vlastní montáž V. Rotello, S. Thayumanavan, Eds. Wiley,2008 ISBN 0470277386
- ^ Lockett, M. R.; Lange, H .; Breiten, B .; Heroux, A .; Sherman, W .; Rappoport, D .; Yau, P.O .; Snyder, P. W .; Whitesides, G. M. (2003). „Vazba benzoarylsulfonamidových ligandů na lidskou karboanhydrázu je necitlivá na formální fluoraci ligandu“. Angew. Chem. Int. Vyd. 52 (30): 7714–7717. doi:10,1002 / anie.201301813. PMID 23788494.
- ^ Breiten, B .; Lockett, M. R.; Sherman, W .; Fujita, S .; Al-Sayah, M .; Lange, H .; Bowers, C. M .; Heroux, A .; Krilov, G .; Whitesides, G. M. (2013). „Vodní sítě přispívají ke kompenzaci entalpie / entropie při vazbě na proteiny a ligandy“. J. Am. Chem. Soc. 135 (41): 15579–15584. CiteSeerX 10.1.1.646.8648. doi:10.1021 / ja4075776. PMID 24044696.
- ^ Zhang, Jingqing; et al. (2013). „Molekulární rozpoznávání pomocí komplexů koronové fáze vyrobených ze syntetických polymerů adsorbovaných na uhlíkových nanotrubičkách“. Přírodní nanotechnologie. 8 (12): 959–968. Bibcode:2013NatNa ... 8..959Z. doi:10.1038 / nnano.2013.236. PMC 5051352. PMID 24270641.
- ^ Mannige, Ranjan V .; Haxton, Thomas K .; Proulx, Caroline; Robertson, Ellen J .; Battigelli, Alessia; Butterfoss, Glenn L .; Zuckermann, Ronald N .; Whitelam, Stephen (2015-10-15). „Peptoidní nanosety vykazují nový motiv sekundární struktury“. Příroda. 526 (7573): 415–420. Bibcode:2015 Natur.526..415M. doi:10.1038 / příroda15363. ISSN 0028-0836. PMID 26444241.
- ^ Beyene, Abraham G .; Demirer, Gozde S .; Landry, Markita P. (01.01.2009). Platformy molekulárního rozpoznávání s templátem nanočástic pro detekci biologických analytů. Současné protokoly v chemické biologii. 8. John Wiley & Sons, Inc., str. 197–223. doi:10,1002 / cpch.10. ISBN 9780470559277. PMID 27622569.
- ^ Biedermann, Frank; Schneider, Hans-Jörg (2016). "Experimentální vazebné energie v supramolekulárních komplexech". Chemické recenze. 116 (9): 5216–5300. doi:10.1021 / acs.chemrev.5b00583. PMID 27136957.
- ^ Shinkai, Seiji; Ikeda, Masato; Sugasaki, Atsushi; Takeuchi, Masayuki (2001). "Pozitivní alosterické systémy navržené na dynamických supramolekulárních lešeních: k přepínání a zesilování afinity a selektivity hostů". Účty chemického výzkumu. 34 (6): 494–503. doi:10.1021 / ar000177r. PMID 11412086.
- ^ Grunenberg, Jörg (2011). "Složitost v molekulárním rozpoznávání". Fyzikální chemie Chemická fyzika. 13 (21): 10136–46. Bibcode:2011PCCP ... 1310136G. doi:10.1039 / C1CP20097F. PMID 21503359.
- ^ Mobley, D. L .; Dill, K. A. (2009). „Vazba ligandů s malou molekulou na proteiny:„ to, co vidíte “, není vždy„ to, co dostanete"". Struktura. 17 (4): 489–98. doi:10.1016 / j.str.2009.02.010. PMC 2756098. PMID 19368882.
- ^ Schmidtchen, Franz P. (2010). „Hostující anionty. Energetická perspektiva“. Recenze chemické společnosti. 39 (10): 3916–35. doi:10.1039 / C0CS00038H. PMID 20820595.
- ^ Jehle H. Mezimolekulární síly a biologická specificita. Proč Natl Acad Sci U S. A. 1963; 50 (3): 516-524. doi: 10,1073 / pnas.50.3.516
- ^ Bernstein H, Edgar RS, Denhardt GH. Intragenní komplementace mezi teplotně citlivými mutanty bakteriofága T4D. Genetika. 1965; 51 (6): 987-1002.
- ^ Crick FH, Orgel LE. Teorie inter-alelické komplementace. J Mol Biol. 1964 Jan; 8: 161-5. doi: 10,1016 / s0022-2836 (64) 80156-x. PMID: 14149958
externí odkazy
- http://www.mdpi.org/ijms/sections/molecular-recognition.htm Zvláštní vydání o molekulárním rozpoznávání v Int. J. Mol. Sci.
