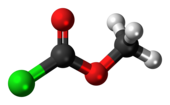
Methylchlorformiát - Methyl chloroformate
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC Methylkarbonochloridát | |
| Ostatní jména Methylchlorformiát, methylkarbonát methylester, methylchlorkarbonát | |
| Identifikátory | |
3D model (JSmol ) | |
| 605437 | |
| ChemSpider | |
| Informační karta ECHA | 100.001.080 |
| Číslo ES |
|
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C2H3ClÓ2 | |
| Molární hmotnost | 94.49 g · mol−1 |
| Hustota | 1,223 g / ml |
| Bod varu | 70 až 72 ° C (158 až 162 ° F; 343 až 345 K) |
| Nebezpečí | |
Klasifikace EU (DSD) (zastaralý) | |
| R-věty (zastaralý) | R34 R50 / 53 |
| S-věty (zastaralý) | (S1 / 2) S26 S45 S60 S61 |
| Bod vzplanutí | 10 ° C (50 ° F; 283 K) |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Methylchlorformiát je methyl ester z kyselina chloroformová. Je to olejovitá bezbarvá kapalina, ačkoli staré vzorky vypadají žlutě. Je také známý svým štiplavým zápachem.
Příprava
Methylchlorformiát lze syntetizovat za použití methanolu a fosgen.
Použití
Methylchlorformiát se používá v organická syntéza pro zavedení methoxykarbonylové funkční skupiny do vhodné nukleofil (tj. karbomethoxylace).[2]
Bezpečnost
Methylchlorformiát po zahřátí uvolňuje fosgen. Při kontaktu s vodou produkuje chlorovodík. Při kontaktu s pokožkou způsobí její poškození.
Viz také
Reference
- ^ Methylchlorformiát v Sigma-Aldrich
- ^ Fischer, Emil (1914). „Syntéza depsidů, lišejníkových látek a tříslovin“. Journal of the American Chemical Society. 36 (6): 1170–1201. doi:10.1021 / ja02183a009.

