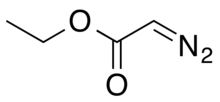
Ethyl diazoacetát - Ethyl diazoacetate
 | |
| Jména | |
|---|---|
| Preferovaný název IUPAC Ethyl diazoacetát | |
| Ostatní jména Ethyl-2-diazoacetát Ethylester kyseliny 2-diazoctové | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.009.828 |
| Číslo ES |
|
PubChem CID | |
| UNII | |
| |
| |
| Vlastnosti | |
| C4H6N2Ó2 | |
| Molární hmotnost | 114,10 g / mol |
| Vzhled | žlutý olej |
| Hustota | 1,085 g / cm3 |
| Bod tání | -22 ° C (-8 ° F; 251 K) |
| Bod varu | 140 až 141 ° C (284 až 286 ° F; 413 až 414 K) 720 mmHg |
| Nebezpečí | |
| Bezpečnostní list | Ethyl diazoacetát |
| Piktogramy GHS |     [3] [3] |
| Signální slovo GHS | Nebezpečí |
| H226, H240, H302, H315, H320, H351[3] | |
| P281, P305 + 351 + 338, P501[3] | |
| NFPA 704 (ohnivý diamant) | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Ethyl diazoacetát (N = N = CHC (0) OC2H5) je diazo sloučenina a činidlo v organická chemie. Objevil jej Theodor Curtius v roce 1883.[4] Sloučenina může být připravena reakcí ethyl ester z glycin s dusitan sodný a octan sodný ve vodě.
Jako karben předchůdce, používá se v cyklopropanace alkenů.
Ačkoli je sloučenina nebezpečná, používá se v chemickém průmyslu jako předchůdce trovafloxacin.[5] Byly zveřejněny postupy pro bezpečnou průmyslovou manipulaci.[6]
Dalším místem, kde byla použita EDA, je výroba BI-4752, nedávno vynalezený agonista 5HT2C, který je dokonce lepší než lorcaserin.
Reference
- ^ Womack, E. B .; Nelson, A. B. (1944). "Ethyldiazoacetát". Organické syntézy. 24: 56.; Kolektivní objem, 3, str. 392
- ^ "Ethyl diazoacetát". Sigma-Aldrich.
- ^ A b C http://www.chemblink.com/MSDS/MSDSFiles/623-73-4_Sigma-Aldrich.pdf
- ^ Curtius, T. (1883). „Ueber die Einwirkung von salpetriger Säure auf salzsauren Glycocolläther“ [O reakci kyseliny dusité s hydrochloridem ethylesteru glycinu]. Berichte der Deutschen Chemischen Gesellschaft. 16 (2): 2230–2231. doi:10,1002 / cber.188301602136.
- ^ Maas, G. (2009). "Nové syntézy diazosloučenin". Angewandte Chemie International Edition. 48 (44): 8186–8195. doi:10.1002 / anie.200902785.
- ^ Clark, J. D .; Shah, A. S .; Peterson, J. C. (2002). „Pochopení rozsáhlé chemie ethyl diazoacetátu pomocí reakční kalorimetrie“. Thermochimica Acta. 392–393: 177–186. doi:10.1016 / S0040-6031 (02) 00100-4.

