Příčina obsedantně-kompulzivní poruchy - Cause of obsessive-compulsive disorder
The Příčinou obsedantně kompulzivní porucha se zabývá identifikací biologických rizikových faktorů podílejících se na expresi symptomů obsedantně-kompulzivní poruchy (OCD). Hlavní hypotézy navrhují zapojení orbitofrontální kůra, bazální ganglia a / nebo limbický systém s objevy v oblasti neuroanatomie, neurochemie, neuroimunologie, neurogenetiky a neuroetologie.
OCD vyvolaná drogami
Mnoho různých typů léků může vytvořit / vyvolat čistý OCD u pacientů, kteří nikdy předtím neměli příznaky. Nová kapitola o OCD v DSM-5 (2013) nyní konkrétně zahrnuje OCD vyvolanou drogami.
Atypická antipsychotika (antipsychotika druhé generace), jako je olanzapin (Zyprexa), bylo prokázáno, že indukuje u pacientů de novo OCD.[1][2][3][4]
Neuroanatomy
Tato část je o události nebo předmětu který stále probíhá a mění se a používání časově orientovaného jazyka je nepřesné. |
Ačkoli se o hodnocení OCD vedla značná debata, současný výzkum tíhl ke strukturálním a funkčním neuroimaging. Tyto technologické inovace umožnily lepší pochopení neuroanatomický rizikové faktory OCD. Tyto studie lze rozdělit do čtyř základních kategorií: (1) klidové studie, které porovnávají mozkovou aktivitu v klidu u pacientů s OCD s kontrolami, (2) provokační studie příznaků, které porovnávají mozkovou aktivitu před a po podněcování příznaků, (3) léčebné studie které porovnávají mozkovou aktivitu před a po léčbě farmakoterapie a (4) studie kognitivní aktivace, které porovnávají mozkovou aktivitu při provádění úkolu u pacientů s OCD s kontrolami.[5]
Údaje získané z tohoto výzkumu naznačují, že OCD zahrnuje tři oblasti mozku: orbitofrontální kůra (OFC) přední cingulární kůra (ACC) a vedoucí kádové jádro.[5] Několik studií zjistilo, že u pacientů s OCD jsou tyto oblasti: (1) v klidu hyperaktivní ve srovnání se zdravou kontrolou; (2) se zvýšenou aktivitou s provokací symptomů; a (3) již nevykazují hyperaktivitu po úspěšné léčbě pomocí SRI farmakoterapie nebo kognitivní terapie.[6] Toto porozumění je často uváděno jako důkaz, že abnormalita v těchto neuroanatomických oblastech může způsobit OCD.
OFC a ACC jsou složitě spojeny s bazálními gangliemi prostřednictvím Kortiko-bazální ganglia-thalamo-kortikální smyčka.[7] Současné teorie naznačují, že OCD může být výsledkem nerovnováhy mezi „přímou“ a „nepřímou“ cestou přes bazální ganglia. Přímé cesty jsou popsány jako běh z kůry do striata, poté do vnitřního segmentu globus pallidus (GPi) a substantia nigra pars reticulate (SNr), pak do thalamu a nakonec zpět do kůry. Nepřímé cesty jsou popsány jako běh z kůry do striata, poté do vnějšího segmentu globus pallidus (GPe), subthalamického jádra (STN), GPi a SNr, pak do thalamu a nakonec zpět do kůry.[8] Zatímco čistý účinek přímé dráhy je excitační, čistý účinek nepřímé dráhy je inhibiční. Byla tedy vyslovena hypotéza, že nadměrná relativní aktivita v přímé dráze ve smyčkách OFC / ACC CBGTC může mít za následek smyčku pozitivní zpětné vazby, při níž jsou uvězněny obsedantní myšlenky.[8] Ačkoli strukturální a funkční neuroimagingové studie poskytly silný základ pro tento předpoklad, stále není jasné, proč se u pacientů s OCD vyvine specifická posedlost místo obecného obsedantního chování vůči všemu. Zatímco vědci naznačují, že existuje zkreslení reakce na konkrétní podněty, jako je kontaminace, základní příčina je stále nejasná.[9]
Neurochemie
I když se zdá, že je to všudypřítomné pochopení neurochemický fungování je zodpovědné za zprostředkování příznaků OCD, nedávné psychofarmakologické studie zjistily, že serotoninový (5-HT) neurotransmiterový systém hraje obzvláště důležitou roli.[10] Ve srovnání se zdravými kontrolami je dlouhodobé podávání selektivní inhibitory zpětného vychytávání serotoninu (SSRI) bylo zjištěno, že jsou účinnější než noradrenergní inhibitory zpětného vychytávání při léčbě OCD.[10] Například Rapoport et al. to prokázal klomipramin byl účinnější než desipramin při snižování několika typů opakujícího se chování.[11] Výzkum také ukázal, že podávání 5-HT antagonistů často zhoršuje příznaky OCD.[12] Pokud by to měla být pravda, dalo by se očekávat mirtazapin (který je mimo jiné 5-HT2A antagonista receptoru) a atypická antipsychotika, která mají také antagonistické účinky na tento receptor ke zmírnění účinku SSRI. Klinické studie s těmito léky však ukázaly opak. Mirtazapin, i když sám o sobě není účinný, bylo prokázáno, že urychluje účinek paroxetin (Pallanti a kol., 2004) a několik studií ukázalo, že atypická antipsychotika zvyšují účinky SSRI u refrakterních pacientů s OCD (Bloch a kol., 2006).[13] I když tato zjištění neposkytují výslovnou příčinu, připravují půdu pro představu, že psychiatrické stavy lze farmakologicky rozřezat. Účinnost při kontrole posedlostí a nutkání pomocí SSRI tedy naznačuje, že OCD má základní neurochemickou etiologii.
Dopaminergní systémy jsou do OCD zapojeny účinností dopaminergních látek, skutečností, že PANDAS může být zapleten,[14] a různými neuroimagingovými studiemi.[15] OCD mohou být léčeni antipsychotiky, nicméně psychostimulancia také prokázala určitý příslib při zmírňování příznaků OCD.[16] I když je třeba je sladit, oba implikují dopaminergní systémy. OCD má také vysokou komorbiditu s ADHD,[17] který je léčen psychostimulanty a může být důsledkem zvýšené fázické a snížené tonické signalizace dopaminergních neuronů. PANDAS také ovlivňuje bazální ganglia, kde dopamin hraje velkou roli jako neurotransmiter.
Neuroimunologie
Henrietta Leonard a Susan Swedo poskytují důkazy neuroimunologické rizikové faktory ve svém článku „Pediatrické autoimunitní neuropsychiatrické poruchy spojené se streptokokovou infekcí (PANDAS).[18]„Vědci naznačují, že post-streptokokový autoimunita může být potenciální příčinou OCD v dětství. V 80. letech byla prospektivně hodnocena velká skupina dětí s OCD. Po a streptokokový infekce, podskupina dětí vyjádřila exacerbace symptomů OCD, které byly charakterizovány jako „přicházející přes noc.[18]„Primární hypotéza odvozená z této studie je, že v některých případech se OCD může vyvinout v důsledku autoimunitní reakce, při které protilátky proti streptokokovým infekcím napadají a poškozují bazální ganglia.
Obsese a nutkání jsou také velmi časté u několika dalších zdravotních stavů, včetně: Tourettův syndrom, Parkinsonova choroba, epilepsie, schizofrenie, Huntingtonova choroba, encefalitida lethargica, Sydenham chorea a poškození konkrétních oblastí mozku.[19] Podobně jako u OCD vykazují tyto poruchy také abnormality v bazálních gangliích. Tato část mozku je zodpovědná za zprostředkování poznání, emocí a pohybu. Narušení bazálních ganglií vede k řadě příznaků, které se vyznačují nutkavostí (vzorce chování, které se uvolňují opakovaně) a impulzivitou (vzorce chování, které se náhle uvolňují různými podněty).[5] To naznačuje, že u pacientů s OCD může být porucha výsledkem abnormálního fungování bazálních ganglií.
Neurogenetika
Studie naznačující genetické faktory pro OCD
Studie dvojčat[20] a rodinné asociační studie prokázaly, že za obsedantně-kompulzivní poruchou stojí určité genetické faktory. Většina studií rodinné asociace prokázala, že alespoň některé formy OCD jsou familiární. Míra OCD u příbuzných postižených jedinců byla významně vyšší než odhadovaná populační prevalence OCD a míra u kontrol. Příbuzní dospělých s OCD měli přibližně dvakrát větší pravděpodobnost postižení než kontrolní skupiny, zatímco příbuzní dětí a dospívajících s OCD měli asi desetkrát vyšší pravděpodobnost, že budou mít OCD také. Toto rodinné sdružení však mohlo být způsobeno také kulturními nebo environmentálními faktory.[21] V současné době existuje jen velmi málo studií zkoumajících faktory prostředí, které stojí za OCD. V retrospektivní studii rizikových faktorů prostředí však vědci zjistili, že prodloužený porod a otoky během těhotenství korelovaly s OCD,[22] což naznačuje, že prostředí hraje určitou roli při určování jeho projevu.
Ve výsledku byly provedeny studie dvojčat, které ukázaly, že příznaky OCD jsou dědičné a tedy geneticky příbuzné.[20] Monozygotní nebo identická dvojčata sdílejí 100% svých genů, zatímco dizygotní nebo bratrská dvojčata sdílejí v průměru 50% svých genů. Klasická studie dvojčat porovnává monozygotická a dizygotická dvojčata. Pokud se monozygotní dvojčata podobají mnohem blíže než dvojčata dizygotická, je pravděpodobné, že při vývoji zvláštnosti hraje důležitou roli genetika. Tyto studie ukázaly, že genetické vlivy na obsedantně-kompulzivní příznaky byly u dětí 45 až 65%. U dospělých byl vliv menší, pohyboval se od 27 do 47%.[20] Výsledky studií však komplikuje skutečnost, že přítomnost jedinců s OCD ve vzorku byla často nízká. Výsledkem bylo, že vědci často zahrnovali jedince s obsedantně-kompulzivními příznaky nebo subklinickou OCD.[21] Tímto způsobem pravděpodobně zahrnovali subjekty trpící jinými souvisejícími poruchami. Rané studie dvojčat byly replikovány později pomocí dvojčat s OCD splňujícími kritéria DSM a zjištění probandi, ale bylo provedeno jen několik.[20]
Počáteční OCD
OCD s časným nástupem, projevující se v dětství nebo dospívání, je podtypem OCD etiologicky odlišným od OCD s dospělým nástupem. Uvádí se, že tento OCD s časným nástupem geneticky souvisí s tickými poruchami a Tourettův syndrom, protože jedna studie zjistila, že pacienti s časným nástupem OCD mají vyšší výskyt Tourettových a jiných tikových poruch.[22] Rodinné asociační studie[23] navrhli, že časný nástup OCD koreluje se zvýšeným rodinným a případně genetickým rizikem. Míra OCD a subklinické OCD mezi příbuznými probandů, jejichž OCD se projevila v dětství nebo dospívání, byla nejméně dvakrát tak vysoká jako míra mezi příbuznými probandů, jejichž OCD se projevila v dospělosti.[23] Další studie rovněž ukázaly, že existuje inverzní vztah mezi věkem nástupu probandu a rizikem OCD u příbuzných.[24] V důsledku toho je možné, že za dvěma typy OCD jsou různé genetické mechanismy; při zkoumání kandidátských genů proto může být nutné kontrolovat věk nástupu.
Kandidátský gen SLC1A1
Je pravděpodobné, že pro vývoj OCD je důležitá řada genů. Některé z těchto kandidátských genů byly identifikovány, ale žádná ze studií kandidátních genů nebyla důsledně replikována, kromě těch, které se týkají genu pro transport glutamátu, SLC1A1 (rodina nosičů solutů 1, člen 1), která kóduje transportér glutamátu, EAAC1.[21] Bylo navrženo, že potíže s identifikací kandidátských genů mohou souviset se skutečností, že většina genových výzkumů ignorovala faktory prostředí. [9] V důsledku toho může být nutné vyvinout modely interakce mezi genetickými a environmentálními faktory pro určité podtypy OCD pro další genetický výzkum. Tři genomové asociační studie byly také dokončeny OCD, které navrhly potenciální oblasti zájmu, včetně oblasti obsahující SLC1A1, 9p24.[21] SLC1A1 je exprimován v kůře, striatu a thalamu (kortiko-striato-thalamokortikální okruh) a souvisí s glutamátovou neurotransmisí.[25] Neuroimaging, kandidátské geny a zvířecí modelové studie poskytly důkazy spojující SLC1A1 a glutamátovou signalizaci s výskytem OCD. Neuroimagingové studie zjistily, že kaudátové glutamatergické koncentrace jsou nižší v přední cingulate a výše v caudate u pacientů s časným nástupem OCD ve srovnání s kontrolami, což naznačuje, že transport glutamátu (a zase glutamátový transportní gen SLC1A1) souvisí s nástupem OCD.[26]
Jednonukleotidové polymorfismy (SNP) v genu SLC1A1 bylo důsledně zjištěno, že souvisí s OCD. Kromě transportu glutamátu byl EAAC1, transportér kódovaný SLC1A1, také spojen se syntézou GABA, která by mohla podporovat náchylnost k OCD. Počáteční studie prokázala významnou souvislost mezi OCD a 3 vázanými polymorfismy v genu SLC1A1.[27] Tento výsledek byl replikován v mnoha studiích. Jedna studie testovaná na čtyři SNP v genu SLC1A1 u jedinců s časným nástupem OCD u čínské populace Han[28] a zjistili, že jeden SNP, rs10491734, byl významně častější u pacientů s OCD než u kontrol. Přesné SNP identifikované v různých studiích se však liší, i když je možné, že je to proto, že studie byly prováděny na různých etnických populacích.[28] Například rodinná asociační studie analyzovala případy SNP v SLC1A1 a jeho okolí v rodinách z celých USA a zjistila, že odlišný SNP, rs4740788 a haplotyp 3-SNP, rs4740788-rs10491734-rs10491733, byly spojeny s OCD.[29]
Pro studium obsedantně-kompulzivní poruchy bylo vyvinuto několik modelů myší. Modelové organismy jsou užitečné pro umožnění zkoumání aspektů některých psychiatrických poruch u jednoho druhu (v tomto případě lidí) u jiných druhů (v tomto případě myší). Je pozoruhodné, že SLC1A1 nulové myši vykazovaly nutkavé chování tím, že vykazovaly zvýšenou agresi a nadměrné samočinné ošetřování, které vedlo ke ztrátě srsti. Jelikož však šlo pouze o dvě chování volně spojená s OCD, neposkytlo to přesvědčivé důkazy o vztahu mezi ztrátou EAAC1 a chováním podobným OCD. Vzhledem k silné korelaci mezi genem SLC1A1 a OCD to naznačuje, že nedostatek EAAC1 vede pouze k chování podobnému OCD, když je kombinován s jinými vzácnými mutacemi v genech souvisejících s CSTC nebo kortiko-striato-thalamokortikálním okruhem.[30]
Neuroetologie
Obrovský monolit psychiatrického výzkumu klade důraz na blízké mechanismy jako příčinu nemoci. V porovnání, evoluční teorie vyvolal otázky týkající se toho, jak mohou být distální mechanismy zapleteny do patogeneze. OCD zahrnuje několik schémat chování, které se mohly uchovat v průběhu evoluční historie. Četné druhy zdědily kognitivní vzorce, které umožňují kontrolu nebezpečí, zabránění kontaminaci a hromadění potravy.[31] Teoretici předpokládali, že dysfunkce kterékoli z těchto strategií by mohla vést k expresi OCD. Tato domněnka je dále podpořena důkazy, že takové zděděné, druhově specifické strategie jsou uloženy v bazálních gangliích.[5]
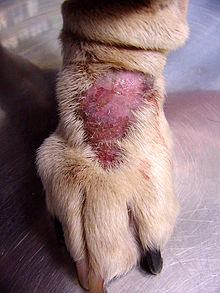
Při zvažování exprese OCD u nelidských druhů vědci studovali akrální lízací dermatitida (také známý jako lízat granulom ) ve velkých špičácích. Tato porucha je charakterizována nadměrným olizováním nebo škrábáním, které vede k alopecii (vypadávání vlasů) a následným granulomatózním lézím (vaskulární tkáň na povrchu rány).[11] Rapoport a kol. zjistili, že toto obsedantně-kompulzivní chování bylo u postižených špičáků po podání klomipraminu zmírněno.[11] Je tedy myslitelné, že by se evoluční vybrané rysy mohly stát maladaptivně postupující neurologickou dysfunkcí.
Reference
- ^ Alevizos, Basil; Papageorgiou, Charalambos; Christodoulou, George N. (1. září 2004). „Obsedantně-kompulzivní příznaky s olanzapinem“. International Journal of Neuropsychopharmacology. 7 (3): 375–377. doi:10.1017 / S1461145704004456. ISSN 1461-1457. PMID 15231024.
- ^ Kulkarni, Gajanan; Narayanaswamy, Janardhanan C .; Math, Suresh Bada (1. ledna 2012). „Olanzapinem vyvolaná de-novo obsedantně kompulzivní porucha u pacienta se schizofrenií“. Indian Journal of Pharmacology. 44 (5): 649–650. doi:10.4103/0253-7613.100406. ISSN 0253-7613. PMC 3480803. PMID 23112432.
- ^ Lykouras, L .; Zervas, I.M .; Gournellis, R .; Malliori, M .; Rabavilas, A. (1. září 2000). „Olanzapin a obsedantně-kompulzivní příznaky“. Evropská neuropsychofarmakologie. 10 (5): 385–387. doi:10.1016 / s0924-977x (00) 00096-1. ISSN 0924-977X. PMID 10974610.
- ^ Schirmbeck, Frederike; Zink, Mathias (1. března 2012). „Obsedantně-kompulzivní příznaky vyvolané klozapinem u schizofrenie: kritický přehled“. Současná neurofarmakologie. 10 (1): 88–95. doi:10.2174/157015912799362724. ISSN 1570-159X. PMC 3286851. PMID 22942882.
- ^ A b C d Maia, T. V., Cooney, R. E. a Peterson, B. S. (2008). Nervové základy obsedantně-kompulzivní poruchy u dětí a dospělých. Development and Psychopathology, 1251-1283.
- ^ Whiteside, S.P .; Port, J.D .; Abramowitz, J.S. (2004). „Metaanalýza funkčního neuroimagingu u obsedantně-kompulzivní poruchy“. Psychiatrický výzkum. 132 (1): 69–79. doi:10.1016 / j.pscychresns.2004.07.001. PMID 15546704.
- ^ Alexander, G. E.; DeLong, M. R.; Strick, P. L. (1986). "Paralelní organizace funkčně oddělených obvodů spojujících bazální ganglia a kůru". Roční přehled neurovědy. 9: 357–381. doi:10.1146 / annurev.neuro.9.1.357.
- ^ A b Saxena, S .; Rauch, S.L. (2000). "Funkční neuroimaging a neuroanatomie obsedantně-kompulzivní poruchy". Psychiatrické kliniky Severní Ameriky. 23 (3): 563–586. doi:10.1016 / s0193-953x (05) 70181-7. PMID 10986728.
- ^ Sasson, Y .; Zohar, J .; Chopra, M .; Lustig, M .; Iancu, I .; Hendler, T. (1997). „Epidemiologie obsedantně-kompulzivní poruchy“. Semináře z klinické neuropsychiatrie. 6: 82–101.
- ^ A b Zohar, J (1987). "Obsedantně-kompulzivní porucha: psychobiologické přístupy k diagnostice, léčbě a patofyziologii". Biologická psychiatrie. 22 (6): 667–687. doi:10.1016/0006-3223(87)90199-5.
- ^ A b C Rapoport, J. L .; Ryland, D. H .; Kriete, M. (1992). "Léčba psího akrálního lízání: zvířecí model obsedantně-kompulzivní poruchy". Archiv obecné psychiatrie. 49: 517–521. doi:10.1001 / archpsyc.1992.01820070011002.
- ^ Hollander, E .; Liebowitz, M. R.; DeCaria, C. M. (1994). "Serotonergní citlivost u hraniční poruchy osobnosti: předběžné nálezy". American Journal of Psychiatry. 151 (2): 277–280. doi:10.1176 / ajp.151.2.277.
- ^ van Dijk, Addy; Klompmakers, Andre; Denys, Damiaan (2010). „Serotonergní systém u obsedantně-kompulzivní poruchy“. Příručka behaviorální neurobiologie serotoninu. Handbook of Behavioral Neuroscience. 21. str. 547–563. doi:10.1016 / s1569-7339 (10) 70100-4. ISBN 9780123746344.
- ^ Orefici, Graziella; Cardona, Francesco; Cox, Carol; Cunningham, Madeleine. Pediatrické autoimunitní neuropsychiatrické poruchy spojené se streptokokovými infekcemi (PANDAS). Oklahoma City: University of Oklahoma Health Sciences Center.
- ^ Maia, Tiago; Cooney, Rebecca; Peterson, Bradley (2008). „Neurální základy obsedantně-kompulzivní poruchy u dětí a dospělých“. Dev psychopatologie.
- ^ Koran, Lorrin; Aboujaoude, Elias; Gamel, Nona (2009). „DoubleBlind Study of Dextroamphetamine Versus Caffeine Augmentation for TreatmentResistant ObsessiveCompulsive Disorder“. The Journal of Clinical Psychiatry: 1530–1535.
- ^ Dar, Reuven; Mittelman, Andrew; Wilhelm, Sabine (2015). „Komorbidita mezi poruchou pozornosti / hyperaktivitou a obsedantně-kompulzivní poruchou po celou dobu životnosti“. Harvardská recenze psychiatrie: 245–262.
- ^ A b Leonard, H. L. a Swedo, S. E. (2001). Pediatrické autoimunitní neuropsychiatrické poruchy spojené s treptokokovou infekcí (PANDAS). International Journal of Neuropsychopharmacology (4), 191-198
- ^ Nestadt, G., Grados, M., & Samuels, J. F. (2010). Genetika obsedantně-kompulzivní poruchy. Psychiatrické kliniky Severní Ameriky, 141-158.
- ^ A b C d van Grootheest, Daniel S .; Cath, Danielle C .; Beekman, Aartjan T .; Boomsma, Dorret I. (2005). „Studie dvojčat o obsedantně-kompulzivní poruše: recenze“. Twin Research a genetika člověka. 8 (5): 450–458. doi:10,1375 / twin.8.5.450.
- ^ A b C d Pauls, David L. (2010). „Genetika obsedantně-kompulzivní poruchy: recenze“. Dialogy v klinické neurovědě. 12 (2): 149–163.
- ^ A b Salem Vasconcelos, Marcos; Santos Sampaio, Aline; et al. (2007). „Prenatální, perinatální a postnatální rizikové faktory u obsedantně-kompulzivní poruchy“. Biologická psychiatrie. 61 (3): 301–307. doi:10.1016 / j.biopsych.2006.07.014. PMID 17123475.
- ^ A b Eichstedt, Julie A .; Arnold, Sharon L. (2001). „Obsedantně kompulzivní porucha začínající v dětství: podtyp OCD související s tiky?“. Recenze klinické psychologie. 21 (1): 137–158. doi:10.1016 / s0272-7358 (99) 00044-6.
- ^ Nestadt, Gerald; Grados, Marco; Samuels, J. F. (2010). "Genetika OCD". Psychiatrické kliniky Severní Ameriky. 33 (1): 141–158. doi:10.1016 / j.psc.2009.11.001. PMC 2824902. PMID 20159344.
- ^ Yoshikatsu Kanai a Matthias A. Hediger, „Rodina transportérů glutamát / neutrální aminokyselina SLC1: Molekulární, fyziologické a farmakologické aspekty,“ Pflügers Archiv: European Journal of Physiology 447, no. 5 (2003): 467-479.
- ^ Rosenberg, David R .; MacMaster, Frank P .; Keshavan, Matcheri S .; et al. (2000). „Pokles glutamatergických koncentrací Caudate u pediatrických pacientů s obsedantně-kompulzivní poruchou užívajících paroxetin“. Journal of the American Academy of Child and Adolescent Psychiatry. 39 (9): 1096–1103. doi:10.1097/00004583-200009000-00008.
- ^ Daniel Arnold, Paul; Sicard, Tricia; Burroughs, Eliza; Richter, Margaret A .; Kennedy, James L. (2006). „Glutamátový transportní gen SLC1A1 spojený s obsedantně-kompulzivní poruchou“. Archiv obecné psychiatrie. 63 (7): 769–776. doi:10.1001 / archpsyc.63.7.769.
- ^ A b Wu, Haisu; Wang, Xuemei; Xiao, Zeping; et al. (2013). „Sdružení mezi genem SLC1A1 a OCD s počátečním nástupem v populaci čínských Han: Případová kontrolní studie“. Journal of Molecular Neuroscience. 50 (2): 353–359. doi:10.1007 / s12031-013-9995-6.
- ^ Samuels, Jack; Wang, Ying; Riddle, Mark A .; et al. (2011). „Komplexní rodinná asociační studie genu SLC1A1 pro glutamátový transportér u obsedantně-kompulzivní poruchy“. American Journal of Medical Genetics Part B: Neuropsychiatric Genetics. 156 (4): 472–477. doi:10,1002 / ajmg.b.31184. PMC 3082623. PMID 21445956.
- ^ Ting, Jonathan T .; Feng, Guoping (2011). „Neurobiologie obsedantně-kompulzivní poruchy: Pohledy na poruchu nervové soustavy prostřednictvím genetiky myší“. Aktuální názor v neurobiologii. 21 (6): 842–848. doi:10.1016 / j.conb.2011.04.010. hdl:1721.1/102180.
- ^ O'Connor, J. J. (2008). Chyba v látce. Journal of Contemporary Psychotherapy, 87-96.
