Hmotnostní bilance - Mass balance
A hmotnostní bilance, také nazývaný a materiálová bilance, je aplikace zachování hmoty k analýze fyzických systémů. Účtováním materiálu vstupujícího a opouštějícího systém hromadné toky lze identifikovat, které by bez této techniky mohly být neznámé nebo obtížně měřitelné. Přesný zákon o ochraně přírody použitý při analýze systému závisí na kontextu problému, ale vše se točí kolem hromadné ochrany, tj. toho hmota nemůže zmizet nebo být vytvořen spontánně.[1]:59–62
Proto se hromadné váhy používají v inženýrství a environmentální analýzy. Například k návrhu se používá teorie hmotnostní bilance chemické reaktory, analyzovat alternativní procesy výroby chemických látek a také modelovat znečištění disperze a další procesy fyzických systémů. Úzce související a doplňkové analytické techniky zahrnují populační bilance, energetická bilance a poněkud složitější entropie Zůstatek. Tyto techniky jsou vyžadovány pro důkladný návrh a analýzu systémů, jako je chladicí cyklus.
V monitorování životního prostředí termín výpočty rozpočtu se používá k popisu rovnic hmotnostní bilance, kde se používají k vyhodnocení údajů z monitorování (porovnání vstupu a výstupu atd.). V biologii dynamický rozpočet na energii teorie metabolické organizace výslovně využívá hmotnostní a energetickou rovnováhu.
Úvod
Obecná forma uvedená pro hmotnostní bilanci je Hmota, která vstupuje do systému, musí zachováním hmotnosti buď opustit systém, nebo se hromadit v systému.
Matematicky je hmotnostní bilance systému bez chemické reakce následující:[1]:59–62
Přísně vzato platí výše uvedená rovnice také pro systémy s chemické reakce pokud se výrazy v rovnovážné rovnici vztahují na celkovou hmotnost, tj. součet všech chemických druhů systému. Při absenci chemické reakce bude množství chemických látek proudících dovnitř a ven stejné; tím vznikne rovnice pro každý druh přítomný v systému. Pokud tomu tak však není, musí být rovnice hmotnostní bilance změněna tak, aby umožňovala tvorbu nebo vyčerpání (spotřebu) každého chemického druhu. Někteří používají v této rovnici jeden termín k popisu chemických reakcí, které budou negativní pro vyčerpání a pozitivní pro generaci. Konvenční forma této rovnice je však napsána tak, aby odpovídala jak pozitivnímu generačnímu termínu (tj. Produktu reakce), tak negativnímu termínu spotřeby (reaktanty použité k výrobě produktů). Ačkoli celkově jeden člen bude odpovídat za celkovou rovnováhu v systému, má-li se tato rovnovážná rovnice použít na jednotlivý druh a pak na celý proces, jsou oba pojmy nezbytné. Tuto upravenou rovnici lze použít nejen pro reaktivní systémy, ale také pro populační bilance, jaké vznikají v mechanika částic problémy. Rovnice je uvedena níže; Všimněte si, že zjednodušuje předchozí rovnici v případě, že generační člen je nula.[1]:59–62
- Při absenci a jaderná reakce počet atomy proudění dovnitř a ven musí zůstat stejné, i za přítomnosti chemické reakce.
- Aby mohla být vytvořena rovnováha, musí být jasně definovány hranice systému.
- Hromadné bilance lze převzít nad fyzickými systémy ve více měřítcích.
- Hmotnostní bilance lze zjednodušit s předpokladem ustálený stav, ve kterém je akumulační termín nulový.
Ilustrativní příklad

Koncept může ilustrovat jednoduchý příklad. Zvažte situaci, ve které a kejda proudí do a usazovací nádrž k odstranění pevných látek v nádrži. Pevné látky se shromažďují ve spodní části pomocí a pásový dopravník částečně ponořen v nádrži a voda vytéká přes přepadový výstup.
V tomto příkladu existují dvě látky: pevné látky a voda. Výstup přepadu vody nese zvýšenou koncentraci vody vzhledem k pevným látkám ve srovnání se vstupem kejdy a výstup z dopravního pásu nese zvýšenou koncentraci pevných látek vzhledem k vodě.
Předpoklady
- Rovnovážný stav
- Nereaktivní systém
Analýza
Předpokládejme, že složení vstupní kaše (hmotnostně) je 50% pevné látky a 50% vody, s hmotnostním průtokem 100 kg /min. Předpokládá se, že nádrž pracuje v ustáleném stavu, a proto je její akumulace nulová, takže vstup a výstup musí být stejné pro pevné látky i vodu. Pokud víme, že účinnost odstraňování pro nádrž na kejdu je 60%, pak bude obsahovat výstup vody 20 kg /min pevných látek (40% krát 100 kg /min krát 50% pevných látek). Pokud změříme průtok kombinovaných pevných látek a vody a výstup vody se ukáže být 65 kg /min, potom musí být množství vody vystupující z dopravníkového pásu 5 kg /min. To nám umožňuje zcela určit, jak byla hmota distribuována v systému pouze s omezenými informacemi a pomocí vztahů hmotnostní bilance přes hranice systému. Hmotnostní bilanci tohoto systému lze popsat v tabulce:
| Proud | |||
|---|---|---|---|
| Materiál | Vstup čističe | Vyčištěný odtok vody | Extrahovaná Soilds |
| Pevné látky | 50 kg / min | 20 kg / min | 30 kg / min |
| Voda | 50 kg / min | 45 kg / min | 5 kg / min |
| Celkový | 100 kg / min | 65 kg / min | 35 kg / min |
Hromadná zpětná vazba (recyklace)
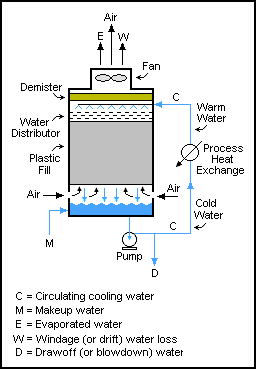
Hromadné bilance lze provádět napříč systémy, které mají cyklické toky. V těchto systémech jsou výstupní toky přiváděny zpět do vstupu jednotky, často pro další zpracování.[1]:97–105
Takové systémy jsou běžné v broušení okruhy, kde se zrno drtí a poté prosévá, aby se z okruhu uvolnily pouze jemné částice a větší částice se vracely do válcového mlýna (drtiče). Toky recyklace však v žádném případě nejsou omezeny na operace mechaniky pevných látek; používají se také v proudech kapalin a plynů. Jeden takový příklad je v chladicí věže, kde je voda mnohokrát čerpána věží, přičemž při každém průchodu je odtaženo pouze malé množství vody (aby se zabránilo hromadění pevných látek), dokud se s vypuštěnou vodou neodpaří nebo neopustí. Hmotnostní bilance pro vodu je M = D + W + E.
Použití recyklace pomáhá při zvyšování celkové konverze vstupních produktů, což je užitečné pro procesy konverze s nízkým průchodem (jako je Haberův proces ).
Diferenciální hmotnostní bilance
Rovněž lze provést hmotnostní bilanci odlišně. Koncept je stejný jako u velké hmotnostní bilance, ale provádí se v kontextu omezujícího systému (například lze uvažovat omezující případ v čase nebo, častěji, v objemu). Ke generování se používá diferenciální hmotnostní bilance diferenciální rovnice který může poskytnout účinný nástroj pro modelování a porozumění cílovému systému.
Diferenciální hmotnostní bilance je obvykle řešena ve dvou krocích: nejprve musí být získána sada řídících diferenciálních rovnic a poté musí být tyto rovnice vyřešeny, buď analyticky, nebo pro méně přijatelné problémy numericky.
Následující systémy jsou dobrým příkladem použití diferenciální hmotnostní bilance:
- Ideální (míchaný) dávkový reaktor
- Ideální tankový reaktor, také pojmenovaný Kontinuální míchaný tankový reaktor (CSTR)
- Ideál Plug Flow Reactor (PFR)
Ideální dávkový reaktor
Ideálním kompletně smíšeným dávkovým reaktorem je uzavřený systém. Izotermické podmínky Předpokládá se, že míchání zabraňuje koncentračním gradientům, protože koncentrace reaktantů se snižují a koncentrace produktu se časem zvyšují.[2]:40–41 Mnoho učebnic chemie implicitně předpokládá, že studovaný systém lze popsat jako dávkový reaktor, když píší o reakční kinetice a chemická rovnováha Hmotnostní bilance látky A se stane
kde rA označuje rychlost, při které se látka A vyrábí, PROTI je objem (který může být konstantní nebo ne), nA počet krtků (n) látky A.
Ve vsádkovém reaktoru jsou některé reaktanty / přísady přidávány kontinuálně nebo pulzně (porovnejte přípravu kaše buď nejprve smícháním všech složek a následným necháním vařit, což lze popsat jako vsádkový reaktor, nebo nejprve smícháním pouze vody a soli a toto se vaří před přidáním dalších přísad, které lze popsat jako vsádkový reaktor). Hmotnostní bilance pro vsádkové reaktory jsou o něco komplikovanější.
Reaktivní příklad
V prvním příkladu si ukážeme, jak použít hmotnostní bilanci k odvození vztahu mezi procenta přebytečného vzduchu pro spalování uhlovodíkového základního topného oleje a procenta kyslíku v plynném produktu spalování. Nejprve obsahuje normální suchý vzduch 0.2095 mol kyslíku na mol vzduchu, takže existuje jeden mol Ó
2 v 4,773 mol suchého vzduchu. U stechiometrického spalování jsou vztahy mezi hmotností vzduchu a hmotností každého hořlavého prvku v topném oleji:
Vzhledem k přesnosti typických analytických postupů je rovnicí pro hmotnost vzduchu na hmotnost paliva při stechiometrickém spalování:
kde wC, wH, wS a wO se vztahují k hmotnostnímu podílu každého prvku v topném oleji, spalování síry na SO2 a AFRHmotnost Odkazuje na poměr vzduch-palivo v hmotnostních jednotkách.
Pro 1 kg topného oleje obsahujícího 86,1% C, 13,6% H, 0,2% O a 0,1% S, je stechiometrická hmotnost vzduchu 14,56 kg, takže AFR = 14,56. Hmotnost produktu spalování je tedy 15,56 kg. Při přesné stechiometrii Ó
2 by měl chybět. Při 15% přebytku vzduchu je AFR = 16,75 a hmotnost spalin je 17,75 kg, který obsahuje 0,505 kg přebytečného kyslíku. Spalovací plyn tak obsahuje 2,84 procenta Ó
2 hmotností. Vztahy mezi procenty přebytečného vzduchu a%Ó
2 ve spalinách jsou přesně vyjádřeny kvadratickými rovnicemi platnými v rozsahu 0–30 procent přebytečného vzduchu:
Ve druhém příkladu použijeme zákon hromadné akce na odvodit výraz pro chemická rovnováha konstantní.
Předpokládejme, že máme uzavřený reaktor, ve kterém dochází k následující reverzibilní reakci v kapalné fázi:
Hmotnostní bilance pro látku A se stane
Protože máme reakci v kapalné fázi, můžeme (obvykle) předpokládat konstantní objem a od té doby dostaneme
nebo
V mnoha učebnicích je to uvedeno jako definice rychlost reakce aniž bychom specifikovali implicitní předpoklad, že mluvíme o reakční rychlosti v uzavřeném systému pouze s jednou reakcí. To je nešťastná chyba, která v průběhu let zmátla mnoho studentů.
Podle zákon hromadné akce rychlost dopředné reakce lze zapsat jako
a rychlost zpětné reakce jako
Rychlost, při které se látka A vyrábí, je tedy
a protože v rovnováze je koncentrace A konstantní, kterou dostaneme
nebo přeskupené
Ideální tankový reaktor / kontinuálně míchaný tankový reaktor
Kontinuálně míchaný tankový reaktor je otevřený systém s přítokem proudu reaktantů a odtokem proudu produktů.[2]:41 Jezero lze považovat za tankový reaktor a jezera s dlouhou dobou obratu (např. S nízkým poměrem toku k objemu) lze z mnoha důvodů považovat za kontinuálně míchaná (např. Homogenní ve všech ohledech). Hmotnostní bilance se pak stane
kde Q0 a Q označit objemový tok do systému a ven ze systému a CA, 0 a CA koncentrace A v přítoku a odtoku. V otevřeném systému nikdy nemůžeme dosáhnout chemické rovnováhy. Můžeme však dosáhnout a ustálený stav kde všichni stavové proměnné (teplota, koncentrace atd.) zůstávají konstantní ().
Příklad
Zvažte vanu, ve které je rozpuštěna trochu soli ke koupání. Nyní naplníme více vody a spodní zástrčku necháme zasunutou. Co se stane?
Protože nedochází k žádné reakci, a protože neexistuje žádný odtok . Hmotnostní bilance se stává
nebo
Při použití hmotnostní bilance pro celkový objem je však zřejmé, že a to . Tak dostaneme
Všimněte si, že neexistuje žádná reakce, a proto ne rychlost reakce nebo zákon o sazbách zapojen, a přesto . Můžeme tedy vyvodit závěr, že reakční rychlost nelze obecně definovat pomocí . Jeden musí nejprve si zapište hmotnostní bilanci před spojením mezi a lze zjistit rychlost reakce. Mnoho učebnic však definuje reakční rychlost jako
aniž bychom zmínili, že tato definice implicitně předpokládá, že systém je uzavřen, má konstantní objem a že existuje pouze jedna reakce.
Ideální reaktor s pístovým tokem (PFR)
Idealizovaný reaktor s pístovým tokem je otevřený systém připomínající trubku bez míchání ve směru proudění, ale s dokonalým mícháním kolmým ke směru proudění, které se často používá u systémů, jako jsou řeky a vodní potrubí, pokud je proudění turbulentní. Když je pro trubku vytvořena hmotnostní bilance, nejprve se uvažuje o infinitezimální část trubice a provést hmotnostní bilanci nad tím pomocí ideálního modelu reaktoru v nádrži.[2]:46–47 Ta hmotnostní bilance tedy je integrovaný po celém objemu reaktoru k získání:
V numerických řešeních, např. při použití počítačů se ideální trubice často převádí na řadu tankových reaktorů, protože je možné ukázat, že PFR je ekvivalentní nekonečnému počtu míchaných nádrží v sérii, ale analýza druhé je často snazší, zvláště v ustáleném stavu .
Složitější problémy
Ve skutečnosti jsou reaktory často neideální, ve kterých se k popisu systému používají kombinace výše uvedených modelů reaktorů. Nejen rychlosti chemických reakcí, ale také hromadný přenos sazby mohou být důležité v matematickém popisu systému, zejména v heterogenní systémy.[3]
Jako chemikálie rychlost reakce v závislosti na teplotě je často nutné udělat obojí energetická bilance (často tepelná bilance spíše než plnohodnotná energetická bilance), jakož i hmotnostní bilance, které plně popisují systém. Pro energetickou bilanci může být zapotřebí jiný model reaktoru: Systém, který je uzavřen s ohledem na hmotnost, může být otevřený s ohledem na energii, např. protože do systému může pronikat teplo vedení.
Komerční použití
V průmyslových provozech s využitím skutečnosti, že hmota vstupující a opouštějící jakoukoli část provozovny musí být vyvážená, validace a odsouhlasení údajů mohou být použity algoritmy pro korekci měřených toků za předpokladu, že existuje dostatečná redundance měření průtoku, aby bylo možné statistické odsouhlasení a vyloučení detekovatelně chybných měření. Jelikož všechny měřené hodnoty v reálném světě obsahují inherentní chybu, sladěná měření poskytují lepší základ než naměřené hodnoty pro finanční výkaznictví, optimalizaci a regulační výkaznictví. Softwarové balíčky existují, aby to bylo komerčně proveditelné denně.
Viz také
Reference
- ^ A b C d Himmelblau, David M. (1967). Základní principy a výpočty v chemickém inženýrství (2. vyd.). Prentice Hall.
- ^ A b C Weber, Walter J., Jr. (1972). Fyzikálně-chemické procesy pro kontrolu kvality vody. Wiley-Interscience. ISBN 0-471-92435-0.
- ^ Perry, Robert H .; Chilton, Cecil H .; Kirkpatrick, Sidney D. (1963). Příručka chemických inženýrů (4. vydání). McGraw-Hill. s. 4–21.
externí odkazy
- Výpočty materiálové bilance
- Základy materiálové bilance
- Materiálová bilance pro chemické reaktory
- Materiálová a energetická bilance
- Metoda tepelné a materiálové bilance řízení procesu pro petrochemické závody a rafinerie ropy, patent USA 6751527
- Morris, Arthur E .; Geiger, Gordon; Fajn, H. Alan (2011). Příručka pro výpočty materiálové a energetické bilance při zpracování materiálu (3. vyd.). Wiley. ISBN 978-1-118-06565-5.















![r_1 = k_1 [ mathrm {A}] ^ a [ mathrm {B}] ^ b](https://wikimedia.org/api/rest_v1/media/math/render/svg/39705e7b067feb34083145780fca904558471a3d)
![{ displaystyle r _ {- 1} = k _ {- 1} [ mathrm {C}] ^ {c} [ mathrm {D}] ^ {d}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/27a0bd516fe71d6b0f717db6bda90c725636c033)


![frac {k_1} {k _ {- 1}} = frac {[ mathrm {C}] ^ c [ mathrm {D}] ^ d} {[ mathrm {A}] ^ a [ mathrm {B }] ^ b} = K_ {eq}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6ea19d7d091bc2086d115756eca8dadca790c6eb)












