Malondialdehyd - Malondialdehyde - Wikipedia
 | |||
| |||
| Jména | |||
|---|---|---|---|
| Název IUPAC propanediální | |||
| Ostatní jména Malonic aldehyd; Malonodialdehyd; Propagační; 1,3-propanedial; Malonaldehyd | |||
| Identifikátory | |||
3D model (JSmol ) |
| ||
| Zkratky | MDA | ||
| ChemSpider | |||
| KEGG | |||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| C3H4Ó2 | |||
| Molární hmotnost | 72.063 g · mol−1 | ||
| Vzhled | Jehlovitá pevná látka[1] | ||
| Hustota | 0,991 g / ml | ||
| Bod tání | 72 ° C (162 ° F; 345 K) | ||
| Bod varu | 108 ° C (226 ° F; 381 K) | ||
| Nebezpečí | |||
| NIOSH (Limity expozice USA pro zdraví): | |||
PEL (Dovolený) | žádný[1] | ||
REL (Doporučeno) | Ca.[1] | ||
IDLH (Okamžité nebezpečí) | Ca [N.D.][1] | ||
| Související sloučeniny | |||
Související alkenals | Kyselina gluková | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
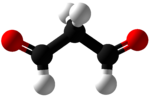
Malondialdehyd (MDA) je organická sloučenina s nominálním vzorec CH2(CHO)2. Bezbarvá kapalina, malondialdehyd, je vysoce reaktivní sloučenina, která se vyskytuje jako enol.[2] Vyskytuje se přirozeně a je markerem oxidační stres.
Struktura a syntéza
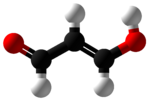
Malondialdehyd existuje hlavně jako enol:[2]
- CH2(CHO)2 → HOC (H) = CH-CHO
V organických rozpouštědlech se cis-izomer je upřednostňován, zatímco ve vodě trans-izomer převládá. Rovnováha je rychlá a je z mnoha důvodů bezvýznamná.
V laboratoři může být generován in situ hydrolýzou jeho acetalu 1,1,3,3-tetramethoxypropan, který je komerčně dostupný a stabilní na skladě, na rozdíl od malondialdehydu.[2] Malondialdehyd se snadno deprotonuje, čímž se získá sodná sůl enolátu (t.t. 245 ° C).
Biosyntéza a reaktivita
Malondialdehyd je výsledkem peroxidace lipidů z polynenasycené mastné kyseliny.[3] Je to prominentní produkt v tromboxan A2 syntéza kde cyklooxygenáza 1 nebo cykloxygenáza 2 metabolizuje kyselina arachidonová na prostaglandin H2 podle krevní destičky a širokou škálu dalších typů buněk a tkání. Tento produkt je dále metabolizován tromboxan syntáza na tromboxan A2, Kyselina 12-hydroxyheptadekatrienová a malonyldialdehyd.[4][5] Alternativně může neenzymaticky přeskupit směs 8-cis a 8-trans isomerů kyseliny 12-hydroxyeikosaheptaenové plus malonyldialdehydu (viz Kyselina 12-hydroxyheptadekatrienová ).[6] Stupeň peroxidace lipidů lze odhadnout podle množství malondialdehydu ve tkáních.[3]
Reaktivní formy kyslíku degradovat polynenasycené lipidy, tvořící malondialdehyd.[7] Tato sloučenina je reaktivní aldehyd a je jedním z mnoha reaktivních elektrofilních druhů, které způsobují toxický stres v buňkách a tvoří kovalentní proteinové adukty označované jako pokročilé lipoxidační konečné produkty (ALE), analogicky k koncové produkty pokročilé glykace (STÁŘÍ).[8] Výroba tohoto aldehydu se používá jako biomarker pro měření hladiny oxidační stres v organismu.[9][10]
Malondialdehyd reaguje s deoxyadenosin a deoxyguanosin v DNA, formování DNA adukty, primární bytostí M1G, který je mutagenní.[11] Guanidinová skupina zbytků argininu kondenzuje s malondialdehydem za vzniku 2-aminopyrimidinů.
Člověk ALDH1A1 aldehyddehydrogenáza je schopna oxidovat malondialdehyd.
Analýza
Malondialdehyd a další thiobarbiturové reaktivní látky (TBARS) kondenzuje se dvěma ekvivalenty kyselina thiobarbiturová čímž se získá fluorescenční červený derivát, který lze analyzovat spektrofotometricky.[2][12] 1-Methyl-2-fenylindol je alternativní selektivnější činidlo.[2]
Nebezpečí a patologie
Malondialdehyd je reaktivní a potenciálně mutagenní.[13] Bylo zjištěno v zahřátých jedlých olejích, jako jsou slunečnicové a palmové oleje.[14]
Rohovky pacientů trpících keratokonus a bulózní keratopatie podle jedné studie mají zvýšené hladiny malondialdehydu.[15] MDA lze také nalézt v tkáňových částech kloubů od pacientů s artróza.[16]
Rovněž lze uvažovat o hladinách malondialdehydu (jako markeru) peroxidace lipidů ) posoudit poškození membrány u spermií; to je zásadní, protože oxidační stres ovlivňuje funkci spermií změnou tekutosti membrány, propustnosti a zhoršení funkční kompetence spermií.[17]
Viz také
Reference
- ^ A b C d NIOSH Kapesní průvodce chemickými nebezpečími. "#0377". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ A b C d E V. Nair, C. L. O'Neil, P. G. Wang „Malondialdehyde“, Encyklopedie činidel pro organickou syntézu, 2008, John Wiley & Sons, New York. doi:10.1002 / 047084289X.rm013.pub2 Článek Datum zveřejnění online: 14. března 2008
- ^ A b Davey MW1, Stals E, Panis B, Keulemans J, Swennen RL (2005). "Vysoce výkonné stanovení malondialdehydu v rostlinných tkáních". Analytická biochemie. 347 (2): 201–207. doi:10.1016 / j.ab.2005.09.041. PMID 16289006.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ J. Biol. Chem. 248: 5673; 1973
- ^ Proc. Natl. Acad. Sci. USA 71: 3 400; 1974
- ^ Prostaglandiny Jiné lipidové léky. 1998 červen; 56 (2-3): 53-76
- ^ Pryor WA, Stanley JP (1975). "Dopis: Navrhovaný mechanismus pro produkci malondialdehydu během autoxidace polynenasycených mastných kyselin. Neenzymatická produkce prostaglandinových endoperoxidů během autoxidace". J. Org. Chem. 40 (24): 3615–7. doi:10.1021 / jo00912a038. PMID 1185332.
- ^ Farmář EE, Davoine C (2007). "Reaktivní elektrofilní druhy". Curr. Opin. Plant Biol. 10 (4): 380–6. doi:10.1016 / j.pbi.2007.04.019. PMID 17646124.
- ^ Moore K, Roberts LJ (1998). "Měření peroxidace lipidů". Free Radic. Res. 28 (6): 659–71. doi:10.3109/10715769809065821. PMID 9736317.
- ^ Del Rio D, Stewart AJ, Pellegrini N (2005). „Přehled nedávných studií o malondialdehydu jako toxické molekule a biologickém markeru oxidačního stresu“. Nutr Metab Cardiovasc Dis. 15 (4): 316–28. doi:10.1016 / j.numecd.2005.05.003. PMID 16054557.
- ^ Marnett LJ (1999). "Peroxidace lipidů - poškození DNA malondialdehydem". Mutat. Res. 424 (1–2): 83–95. doi:10.1016 / S0027-5107 (99) 00010-X. PMID 10064852.
- ^ http://www.amdcc.org/shared/showFile.aspx?doctypeid=3&docid=33 Archivováno 14. Září 2006 v Wayback Machine
- ^ Hartman PE, Předpokládané mutageny a karcinogeny v potravinách. IV. Malonaldehyd (malondialdehyd) Environ Mutagen. 1983; 5 (4): 603-7
- ^ Dourerdjou, P .; Koner, B. C. (2008), Vliv různých nádob na vaření na peroxidaci různých jedlých olejů vyvolanou teplem, „Journal of Food Biochemistry, 32: 740–751. doi:10.1111 / j.1745-4514.2008.00195.x
- ^ Buddi R, Lin B, Atilano SR, Zorapapel NC, Kenney MC, Brown DJ (březen 2002). „Důkazy oxidačního stresu u lidských onemocnění rohovky“. J. Histochem. Cytochem. 50 (3): 341–51. doi:10.1177/002215540205000306. PMID 11850437.[trvalý mrtvý odkaz ]
- ^ Tiku ML, Narla H, Jain M, Yalamanchili P (2007). „Glukosamin zabraňuje in vitro degradaci kolagenu v chondrocytech inhibicí pokročilých lipoxidačních reakcí a oxidace proteinů“. Výzkum a terapie artritidy. 9 (4): R76. doi:10.1186 / ar2274. PMC 2206377. PMID 17686167.
- ^ Collodel, G .; Moretti, E .; Micheli, L .; Menchiari, A .; Moltoni, L .; Cerretani, D. (březen 2015). "Charakteristiky spermatu a hladiny malondialdehydu u mužů s různými reprodukčními problémy". Andrologie. 3 (2): 280–286. doi:10.1111 / ar.297. PMID 25331426. S2CID 28027300.