Spojka Liebeskind – Srogl - Liebeskind–Srogl coupling
tento článek příliš spoléhá na Reference na primární zdroje. (Květen 2019) (Zjistěte, jak a kdy odstranit tuto zprávu šablony) |
| Spojka Liebeskind – Srogl | |
|---|---|
| Pojmenoval podle | Lanny S. Liebeskind Jiří Srogl |
| Typ reakce | Vazební reakce |
| Identifikátory | |
| RSC ontologické ID | RXNO: 0000604 |
The Spojka Liebeskind – Srogl reakce je organická reakce formování nového vazba uhlík-uhlík od a thioester a a kyselina boritá pomocí kovu katalyzátor. Je to křížová vazebná reakce.[1] Tuto reakci vynalezl a pojmenoval Jiří Srogl z Akademie věd České republiky a Lanny S. Liebeskind z Emory University, Atlanta, Georgia, USA. Existují tři generace této reakce, přičemž první generace je uvedena níže. Původní transformace používala jako další ligand katalytický Pd (0), TFP = tris (2-furyl) fosfin a stechiometrický CuTC = měď (I) thiofen-2-karboxylát jako katalyzátor na kov. Celkové reakční schéma je uvedeno níže.
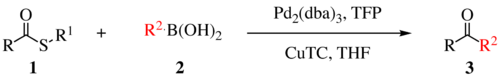
Liebeskind-Sroglova reakce se nejčastěji vyskytuje u thioetherových nebo thioesterových elektrofilů a kyseliny borité nebo stannanových nukleofilů, ale u mnoha dalších spojovací partneři jsou životaschopné. Kromě alkyl a aryl thioesterů; (hetereo) arylthioethery, thioamidy, thioalkyny a thiokyanáty jsou kompetentní elektrofily.[2] Prakticky každá vazba kov-R, která je schopna transmetalace bylo prokázáno.[2] Nukleofily odvozené od india nevyžadují žádnou měď ani bázi. Všimněte si, že tento rozsah je použitelný pro spojení první generace, protože druhá a třetí generace jsou mechanicky odlišné a byly prokázány pouze u thioesterů schopných tvořit šestičlenné metalocyklus, boronové kyseliny, a stannanes.

Přístup první generace ke křížové vazbě probíhá za anaerobních podmínek za použití stechiometrické mědi a katalytického palladia.[1]
Přístup druhé generace činí reakce katalytické v mědi použitím extra ekvivalentu kyseliny borité za aerobních podmínek bez obsahu palladia.[3] Dodatečný ekvivalent uvolňuje měď z přídavku síry a umožňuje její převrácení. Tato chemie je omezena na thioestery a thioethery a mohla by být také omezena náklady a dostupností organoboron činidlo.
Třetí generace činí reakci katalytickou v mědi, přičemž se používá pouze jeden ekvivalent kyseliny borité.[4]
Mechanismus
Generace 1
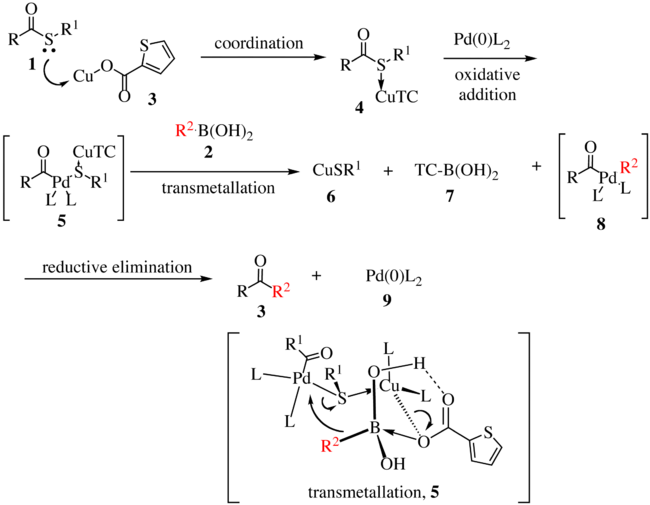
Navrhovaný mechanismus reakce pro první generaci je uveden níže.[5][6] Thioester 1 komplexy s komplexem mědi 3 za vzniku sloučeniny 4. S oxidační inzerce [Pd] do vazba uhlík-síra sloučenina 5 je vytvořen as transmetalace, organopalladium druh 8 je vytvořen. Transmetalace probíhá převodem R.2 do centra kovu palladia se současným přenosem atomu síry do komplexu mědi. Redukční eliminace dává keton 3 s regenerací aktivního katalyzátoru 9.
Generace 2
Mechanismus pro druhou generaci je uveden níže.[3] Mechanismus se neřídí tradiční cestou oxidační adice-transmetelace-reduktivní eliminace jako první generace. Souběžně se studiemi Cu (I) -dioxygenových reakcí se navrhuje vazba s vyšším oxidačním stavem, Cu-templated.[7][8][9][10][11] Koordinace mědi (I) s thioesterem podléhá oxidaci vzduchem za vzniku meziproduktu mědi (II / III). Kovové šablonování Cu (II / III) působí jako Lewisova kyselina, a to jak k aktivaci thiolesteru, tak k dodávání R2 (buď přímo z boru, nebo prostřednictvím meziproduktu Cu-R2 druh), který produkuje keton a Cu-thiolát. K přerušení vazby mědi a síry a uvolnění mědi zpět do katalytického cyklu je zapotřebí druhý ekvivalent kyseliny borité.

Generace 3
Třetí generace činí reakci katalytickou v mědi a používá pouze jeden ekvivalent kyseliny borité napodobováním metalothioneinový (MT) systém že houby hlíny z biologických systémů.[4] Thio-pomocná látka obsahuje motiv N-O, který napodobuje motiv S-S v biosystému MT, který je nezbytný k rozbití vazby mědi a síry a převrácení katalyzátoru. Tato generace neobsahuje palladium a je v mikrovlnných podmínkách. Očekává se, že mechanismus bude následovat mechanismus druhé generace (zobrazený jako aktivní Cu (I) -R2 druh ale R2 může být dodáván přímo z koordinované kyseliny borité), ale obsahuje přídavnou uvolňující měď zpět do katalytického cyklu namísto další kyseliny borité.

Aplikace v syntéze
Spojka Liebeskind – Srogl byla v několika případech použita jako klíčové retrosyntetické odpojení celková syntéza přírodního produktu.
Například při syntéze Goniodominu A použila laboratoř Sasakki tuto chemii pro rychlý přístup k severní polovině přírodního produktu.[12]

Laboratoř Guerrero použila spojku Liebeskind – Srogl ke konstrukci celého uhlíkového skeletu viridin ve vysokém výtěžku ve vícegramovém měřítku.[13]

Laboratoř ve Figadere použila Liebeskind-Sroglovu vazbu v rané fázi syntézy amfidinolidu F[14] využitím této reakce ke konstrukci severovýchodního fragmentu makrocyklu a terpen řetěz.

jiný
Usměrněná diferencializace
Laboratoř Yu prokázala, že v přítomnosti dvou thioetherových vazeb může být jedna selektivně funkcionalizována v přítomnosti jednoho ekvivalentu nukleofilu, pokud je řízena karbonylovým kyslíkem.[15] Tato reakce probíhá prostřednictvím pětičlenného člena palladacycle přičemž na tom probíhá oxidační přidání cis-thioether. Další ekvivalence nukleofilu bude funkcionalizovat trans-pozice.

Reference
- ^ A b Liebeskind, L .; Srogl, Jiří (2000). „Spojení thiol-ester-kyselina boritá. Mechanicky bezprecedentní a obecná syntéza ketonů“. J. Am. Chem. Soc. 122 (45): 11260–11261. doi:10.1021 / ja005613q.
- ^ A b Cheng, Hong-Gang; Chen, Han; Liu, Yue; Zhou, Qianghui (březen 2018). „Křížová vazebná reakce Liebeskind-Srogl a její syntetické aplikace“. Asian Journal of Organic Chemistry. 7 (3): 490–508. doi:10.1002 / ajoc.201700651.
- ^ A b Villalobos, Janette M .; Srogl, Jiří; Liebeskind, Lanny S. (prosinec 2007). „Nové paradigma pro vytváření vazeb uhlík – uhlík: aerobní, měděné templátované křížové vazby“. Journal of the American Chemical Society. 129 (51): 15734–15735. doi:10.1021 / ja074931n. ISSN 0002-7863. PMC 2561227. PMID 18047333.
- ^ A b Zhang, Zhihui; Lindale, Matthew G .; Liebeskind, Lanny S. (27. dubna 2011). „Mobilizace Cu (I) pro katalýzu vytvářející vazby uhlík-uhlík v přítomnosti thiolátu. Chemické napodobování metalothioneinů“. Journal of the American Chemical Society. 133 (16): 6403–6410. doi:10.1021 / ja200792m. ISSN 0002-7863. PMC 3128984. PMID 21449537.
- ^ Yu, Y .; Liebeskind, L. S. (2004). "Měď zprostředkovaná, palladiem katalyzovaná vazba thiolesterů s alifatickými organoboronovými činidly". J. Org. Chem. 69 (10): 3554–3557. doi:10.1021 / jo049964p. PMID 15132570.
- ^ ^ Villalobos, J. M .; Srogl, J .; Liebeskind, L. S. (2007). „Nové paradigma pro vytváření vazeb uhlík-uhlík: aerobní křížová vazba s měděným vzorem“. J. Am. Chem. Soc. 129 (51): 15734–15735. doi:10.1021 / ja074931n. PMC 2561227. PMID 18047333.
- ^ Hatcher, Lanying Q .; Vance, Michael A .; Narducci Sarjeant, Amy A .; Solomon, Edward I .; Karlin, Kenneth D. (duben 2006). „Copper-Dioxygen Adducts and the Side-on Peroxo Dicopper (II) / Bis (μ-oxo) Dicopper (III) Equilibrium: Significant Ligand Electronic Effects“. Anorganická chemie. 45 (7): 3004–3013. doi:10,1021 / ic052185m. ISSN 0020-1669. PMID 16562956.
- ^ Mirica, Liviu M .; Rudd, Deanne Jackson; Vance, Michael A .; Solomon, Edward I .; Hodgson, Keith O .; Hedman, Britt; Stack, T. Daniel P. (březen 2006). „μ-η2: η2-Peroxodicopper (II) Complex with a Secondary Diamine Ligand: A Functional Model of Tyrosinase“. Journal of the American Chemical Society. 128 (8): 2654–2665. doi:10.1021 / ja056740v. ISSN 0002-7863. PMID 16492052.
- ^ Matsumoto, Takahiro; Furutachi, Hideki; Kobino, Masashi; Tomii, Masato; Nagatomo, Shigenori; Tosha, Takehiko; Osako, Takao; Fujinami, Shuhei; Itoh, Shinobu (březen 2006). „Intramolekulární hydrolýza arenu versus intermolekulární epoxidace olefinů komplexem (μ-η2: η2-Peroxo) dicopper (II) podporovaný doinucleatujícím ligandem“. Journal of the American Chemical Society. 128 (12): 3874–3875. doi:10.1021 / ja058117g. ISSN 0002-7863. PMID 16551071.
- ^ Lewis, Elizabeth A .; Tolman, William B. (únor 2004). "Reaktivita systémů s dioxygenem a mědí". Chemické recenze. 104 (2): 1047–1076. doi:10.1021 / cr020633r. ISSN 0009-2665. PMID 14871149.
- ^ Chemické recenze. 104 (8): 6. 11. srpna 2004. doi:10.1021 / cr040141 +. ISSN 0009-2665. Chybějící nebo prázdný
| název =(Pomoc) - ^ Saito, Tomoyuki; Fuwa, Haruhiko; Sasaki, Makoto (19. listopadu 2009). „Směrem k celkové syntéze goniodominu A, mořského polyether-makrolidu zaměřeného na aktiny: konvergentní syntéza segmentu C15-C36“. Organické dopisy. 11 (22): 5274–5277. doi:10.1021 / ol902217q. ISSN 1523-7060. PMID 19905029.
- ^ Del Bel, Matthew; Abela, Alexander R .; Ng, Jeffrey D .; Guerrero, Carlos A. (24. května 2017). "Enantioselektivní chemické syntézy furanosteroidů (-) - Viridin a (-) - Viridiol". Journal of the American Chemical Society. 139 (20): 6819–6822. doi:10.1021 / jacs.7b02829. ISSN 0002-7863. PMID 28463562.
- ^ Ferrié, Laurent; Fenneteau, Johan; Figadère, Bruno (červen 2018). "Celková syntéza mořského makrolidu amfidinolidu F" (PDF). Organické dopisy. 20 (11): 3192–3196. doi:10.1021 / acs.orglett.8b01020. ISSN 1523-7060. PMID 29762038.
- ^ Jin, Weiwei; Du, Wangming; Yang, Qin; Yu, Haifeng; Chen, Jiping; Yu, Zhengkun (19. srpna 2011). „Regio- a stereoselektivní syntéza multisubstituovaných olefinů a konjugovaných dienů pomocí α-oxoketenových dithioacetálů jako stavebních bloků“. Organické dopisy. 13 (16): 4272–4275. doi:10,1021 / ol201620g. ISSN 1523-7060. PMID 21761823.
