Fulvalene - Fulvalene
 | |
 | |
| Jména | |
|---|---|
| Ostatní jména Bicyklopentyliden-2,4,2 ', 4'-tetraen 1,1'-Bi [cylopentadienyliden] Pentafulvalene Bicyklopentadienyliden [5,5 '] Bicyklopentadienyliden | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChemSpider | |
PubChem CID | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C10H8 | |
| Molární hmotnost | 128.174 g · mol−1 |
| Hustota | 1,129 g / ml |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
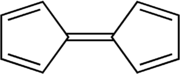
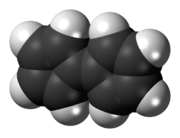
Fulvalene (bicyklopentadienyliden) je členem fulvalene rodina s molekulární vzorec C10H8. Teoreticky je zajímavý jako jeden z nejjednodušších non-benzenoid konjugovaný uhlovodíky. Fulvalene je nestabilní izomer běžnějších benzenoidových aromatických sloučenin naftalen a azulen. Fulvalene se skládá ze dvou pětičlenných kruhů, každý se dvěma dvojné vazby, ke kterému se přidala ještě pátá dvojná vazba. Má D.2h symetrie.
Dějiny
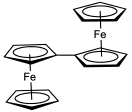
Dřívější pokus o syntézu fulvalenu v roce 1951, který provedli Pauson a Kealy, vedl k náhodnému objevu ferrocen.[1] Jeho syntéza byla poprvé uvedena v roce 1958 E. A. Matznerem, pracujícím pod William von Eggers Doering.[2] V této metodě cyklopentadienylový anion je kondenzován s jodem na dihydrofulvalen. Dvojnásobek deprotonace dihydrofulvalenu s n-butyllithium dává dilithiový derivát, který oxiduje kyslíkem. Fulvalene byl spektroskopicky pozorováno u 77 K. z fotolýza z diazocyklopentadien, který indukuje dimerizace derivátu cyklopentadienu karbeny.[3] Sloučenina byla izolována v roce 1986.[4] Bylo zjištěno, že je nearomatický. Nad -50 ° C dimerizuje o a Diels-Alderova reakce.
Deriváty
Perchlorofulvalen (C.4Cl4C)2 je poměrně stabilní na rozdíl od samotného fulvalenu.[5]
Viz také
- Fulvenes, (CH = CH)2C = CH2 a substituované deriváty
- Tetrathiafulvalene, C.2H2S2C = CS2C2H2
Reference
- ^ T. J. Kealy, P. L. Pauson (1951). „Nový typ sloučeniny organo-železo“. Příroda. 168 (4285): 1039–1040. Bibcode:1951Natur.168.1039K. doi:10.1038 / 1681039b0. S2CID 4181383.
- ^ Disertační abstrakty Int'l 26-06 strana 3270 6411876.
- ^ Demore, William B .; Pritchard, H. O .; Davidson, Norman (1959). „Fotochemické experimenty v tuhých médiích při nízkých teplotách. II. Reakce methylenu, cyklopentadienylenu a difenylmethylenu“. Journal of the American Chemical Society. 81 (22): 5874–5879. doi:10.1021 / ja01531a008.
- ^ Escher, André; Rutsch, Werner; Neuenschwander, Markus (1986). „Synthese von Pentafulvalen durch oxidativní Kupplung von Cyclopentadienid mittels Kupfer (II) -chlorid“. Helvetica Chimica Acta. 69 (7): 1644 - 1654. doi:10,1002 / hlca.19860690719.
- ^ Mark, V. (1966). „Perchlorofulvalene“. Organické syntézy. 46: 93. doi:10.15227 / orgsyn.046.0093.
