Methyltrimethoxysilan - Methyltrimethoxysilane
 | |
| Jména | |
|---|---|
| Název IUPAC Trimethoxy (methyl) silan | |
| Ostatní jména MTM, trimethoxymethylsilan | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
| Informační karta ECHA | 100.013.350 |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C4H12Ó3Si | |
| Molární hmotnost | 136.222 g · mol−1 |
| Vzhled | Bezbarvá kapalina |
| Hustota | 0,955 g / cm3 |
| Bod varu | 102–104 ° C (216–219 ° F; 375–377 K) |
| hydrolýza | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
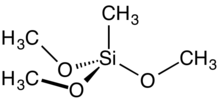
Methyltrimethoxysilan je organokřemičitá sloučenina se vzorcem CH3Si (OCH3)3. Je to bezbarvá, volně tekoucí kapalina. Jedná se o síťovadlo při přípravě polysiloxan polymery.[1][2]
Příprava, struktura a reaktivita
Methyltrimethoxysilan se obvykle připravuje z methyltrichlorsilan a methanolu:
- CH3SiCl3 + 3 CH3OH → CH3Si (OCH3)3 + 3 HCl
Alkoholýza alkylchlorsilanů obvykle probíhá přes SN2 mechanismus. Inverze konfigurace je upřednostňována během nukleofilního útoku při přemisťování dobře odstupujících skupin, jako je chlorid.[3] Naproti tomu vysídlení chudých odcházejících skupin, jako např alkoxid, zachování je upřednostňováno.[4]
Methyltrimethoxysilan je čtyřboký a je často popisován jako sp3 hybridizováno. Má idealizovaný C.3v bodová symetrie.
Hydrolýza MTM probíhá jak za kyselých, tak za zásaditých podmínek. V kyselých podmínkách rychlost postupných hydrolyzací methyltrimethoxysilanu klesá s každým krokem. Za základní podmínky je opak pravdou.[1]
Reference
- ^ A b Brinker, C. J. (1988). „Hydrolýza a kondenzace silikátů: účinky na strukturu“ (PDF). Časopis nekrystalických pevných látek. 100: 31. Bibcode:1988JNCS..100 ... 31B. doi:10.1016/0022-3093(88)90005-1.
- ^ Kuroda, Kazujuki; Shimojima, Atsushi; Kawahara, Kazufumi; Wakabayashi, Ryutaro; Tamura, Yasuhiro; Asakura, Yusuke; Kitahara, Masaki (2014). „Využití alkoxysilylových skupin k vytváření strukturně řízených nanomateriálů na bázi siloxanu“. Chemie materiálů. 26: 211. doi:10,1021 / cm4023387.
- ^ Stephan, Pawlenko (1986). Organosilicon Chemistry. Berlín: Walter de Gruyter. ISBN 9780899252025.
- ^ Colvin, W. Ernest, Křemík v organické syntéze, Butterworth and Co Ltd, 1981.
