Fosfireniový ion - Phosphirenium ion
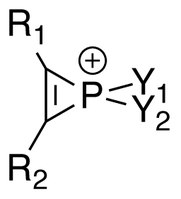
Fosfireniové ionty (R
1R
2C
2PY
1Y+
2) jsou série organofosforové sloučeniny obsahující nenasycený tříčlenný kruhový fosfor (V) heterocykly a σ * -aromaticita Předpokládá se, že je v takových molekulách přítomen. Mnoho solí obsahujících fosfireniové ionty bylo izolováno a charakterizováno NMR spektroskopie a Rentgenová krystalografie.
Syntéza
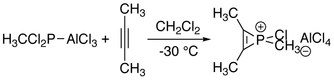
První série fosfireniových iontů byla syntetizována reakcí alkynů s methyl- nebo fenylfosfonovým dichloridem a chloridem hlinitým. Tyto reakce lze považovat za formální přidání „RClP+„na alkyny.[1]
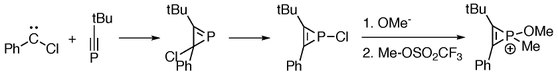
[2 + 1] -cykloadiční reakce mezi fosfaalkyny a chlorkarbeny dávají fosfireny, které slouží jako výchozí materiály pro generování fosfireniových látek.[2]
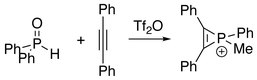
Zpracováním difenylfosfinoxidu difenylacetylenem se získají fosfireniové sloučeniny.[3]
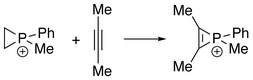
Fosfireniové ionty lze také získat reakcí mezi fosfiry a alkyny, kde „RClP+„je formálně převeden z alkenů na alkyny.[4]
Charakterizace
V literatuře, 31P NMR spektra fosfireniových iontů vykazují posuny směrem nahoru (-57,3 ppm, když R1 = R.2 = Y1 = CH3, Y2 = Cl). Velké spojovací konstanty J se také nacházejí v 11H NMR a jsou srovnatelné s těmi nalezenými v cyklopropeniové ionty.[1]
První fosfireniový ion charakterizovaný rentgenovou krystalografií má následující strukturní vzorec:[5]
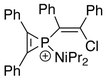
V rafinované krystalové struktuře bylo zjištěno, že průměrná vzdálenost fosforu od cyklického uhlíku je 1,731 (12) Å, což zhruba odpovídá řádu vazeb 1,5. Pro srovnání jsou typické vzdálenosti P – C s jednou a dvojnou vazbou 1,86 Å, respektive 1,68 Å.[5][6]
Reaktivita
Připomíná výměna n-ligandu v koordinační sloučeniny, fosfireniový iont může procházet alkynovou výměnou s jinými alkyny za vzniku směsi fosinireniových sloučenin v rovnováze. Kineticky se navrhuje eliminace alkinu z kationtu krok určující rychlost.[7]
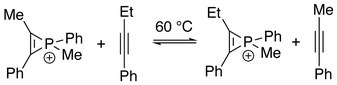
Kromě toho může být porušen tříčlenný kruh fosfireniového iontu. Následné reakce s vhodným nukleofilem jsou schopné pokračovat na elektrofilním atomu fosforu. S přítomností alkinu:[8]

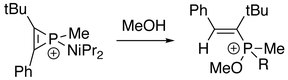
Při přítomnosti vody nebo alkoholu:[2]
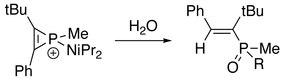
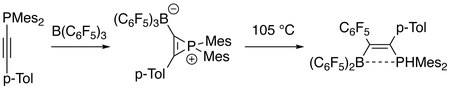
Elektrofilní B (C.6F5)3 snadno reaguje s fosfinylalkyny při teplotě místnosti za vzniku fosfirenium-boritanu zwitterions jako meziprodukty, které pak při vyšší teplotě generují produkty aktivace vazby uhlík-fosfor σ. Výrobky jsou předmětem zájmu vědy o materiálech. Tečkovaná čára v produktu označuje slabou interakci mezi atomy boru a fosforu (viz frustrovaný Lewisův pár ).[9]
σ * - aromatičnost
Kvalitativní molekulární orbitální (MO) diagram phophirenium iontu lze získat lineární kombinací orbitalů z a PY+
2 fragment a ohnutý fragment RC = CR.[10][11] Nízko položený σ * orbitál z prvního s ungerade symetrií interaguje s oběma π a π * orbitaly druhého a vytváří 2π-Hückelův systém, analogický k tomu v cyklopropeniovém iontu. Tento efekt byl pojmenován jako σ * -aromaticita. Je pozoruhodné, že na rozdíl od případu cyklopropeniového iontu, interakce mezi vyplněným σ orbitálem PY+
2 fragment a π orbitaly také vedou k určitému stupni antiaromatického charakteru. Čistý 3-středový konjugační účinek je tedy kombinací stabilizačního příspěvku σ * a destabilizujícího příspěvku σ.[10]
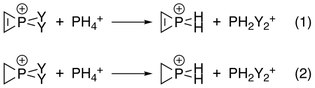
Elektronegativita každého z substituentů na fosforu hraje roli, protože ty, které více darují elektrony, poskytují vyšší stupeň destabilizace antiaromatického sigma. To bylo potvrzeno Analýza přirozené populace (NPA), kde byly energetické změny reakcí níže vypočítány s interakcemi mezi dvojnou vazbou C – C a fosforem jak zapnutím, tak vypnutím manipulací Fockové maticové prvky:
2C
2PF+
2 z analýzy NBO.
Destabilizační energie byly rozdíly mezi odpovídajícími reakcemi:[10]
- Destabilizační energie = energie (1) - energie (2)
- Destabilizační energie s různými Y skupinami: Y = F> OH> Cl> NH2 > Br> I> CH3 > H
Tato řada odpovídá trendu elektronegativity atomů ligandu.
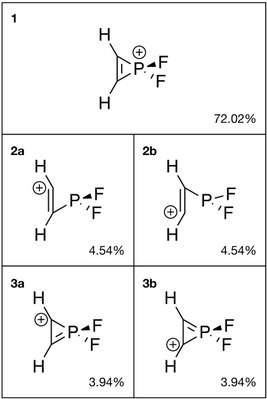
Přírodní vazba orbitální (NBO) analýza poskytuje možné Lewisovy struktury molekuly a bylo provedeno za účelem posouzení struktury H
2C
2PF+
2. Podobně jako aromatický cyklopropeniový iont vykazuje fosforový analog rezonanci mezi strukturou s dvojnou vazbou uhlík-uhlík (1, 72,02%) a ty s dvojnou vazbou uhlík-fosfor (3a a 3b, 7,88% dohromady). Kromě toho se otevírá kruh 2a a 2b kombinovaná také zabírají 9,08% hmotnosti.
Reference
- ^ A b Fongers, K. S .; Hogeveen, H .; Kingma, R. F. (1983). "Syntéza fosfireniových solí". Čtyřstěn dopisy. 24 (6): 643–646. doi:10.1016 / s0040-4039 (00) 81487-2.
- ^ A b Heydt, Heinrich; Hoffmann, Jürgen; Göller, Andreas; Clark, Timothy; Regitz, Manfred (1998). „Organofosforové sloučeniny; 122. Alkylace 1H-Fosfireny s trifláty - syntéza λ5σ4-1H-Fosfireniové kationty “. Syntéza. 1998 (2): 175–180. doi:10.1055 / s-1998-2010. ISSN 0039-7881.
- ^ Hockless, David C.R .; McDonald, Mark A .; Pabel, Michael; Wild, S. Bruce (1997). "Snadná syntéza a interkonverze mezi jednoduchými fosfraniovými a fosfireniovými solemi". Journal of Organometallic Chemistry. 529 (1–2): 189–196. doi:10.1016 / s0022-328x (96) 06641-7.
- ^ Ne, Yuto; Hirano, Koji; Miura, Masahiro (03.05.2017). „Electrofilic Phosphination / Cyclization of Alkynes“. Journal of the American Chemical Society. 139 (17): 6106–6109. doi:10.1021 / jacs.7b02977. ISSN 0002-7863. PMID 28412816.
- ^ A b Vural, J. M .; Weissman, Steven A .; Baxter, S. G .; Cowley, Alan H .; Nunn, Christine M. (01.01.1988). „Rentgenová krystalová struktura fosfireniového iontu“. Journal of the Chemical Society, Chemical Communications. 0 (7): 462. doi:10.1039 / C39880000462. ISSN 0022-4936.
- ^ Pyykkö, Pekka; Atsumi, Michiko (01.01.2009). "Molekulární kovalentní poloměry s jednou vazbou pro prvky 1–118". Chemistry - A European Journal. 15 (1): 186–197. doi:10.1002 / chem.200800987. ISSN 1521-3765. PMID 19058281.
- ^ Brasch, Nicola E .; Hamilton, Ian G .; Krenske, Elizabeth H .; Wild, S. Bruce (01.01.2004). „Výměna π-ligandu na fosfornatých iontech: reverzibilní výměna mezi volnými a koordinovanými alkyny ve fosfireniových solích“. Organometallics. 23 (2): 299–302. doi:10.1021 / om030607z. ISSN 0276-7333.
- ^ Weissman, Steven A .; Baxter, S. G. (1990). "Důkazy o přeskupení P-chlorfosfireniové ionty až P-vinylfosfeniové ionty “. Čtyřstěn dopisy. 31 (6): 819–822. doi:10.1016 / s0040-4039 (00) 94636-7.
- ^ Ekkert, Olga; Kehr, Gerald; Fröhlich, Roland; Erker, Gerhard (06.09.2011). „Zwitterion fosfirenium-boritanu: tvorba při 1,1-karboborační reakci fosfinylalkynů“. Chemická komunikace. 47 (37): 10482. doi:10.1039 / c1cc13008k. ISSN 1364-548X. PMID 21860861.
- ^ A b C Göller, Andreas; Heydt, Heinrich; Clark, Timothy (01.01.1996). „σ * -Aromaticita substituovaných 1H-fosfireniových kationtů a substituovaných siilacyklopropenů“. The Journal of Organic Chemistry. 61 (17): 5840–5846. doi:10.1021 / jo960387h. ISSN 0022-3263.
- ^ Priyakumari, Chakkingal P .; Jemmis, Eluvathingal D. (2013-10-30). "P
3F2–
9: All-Pseudo-π * 2π-Aromatic ". Journal of the American Chemical Society. 135 (43): 16026–16029. doi:10.1021 / ja408308g. ISSN 0002-7863. PMID 24134040.
