PBT2 - PBT2 - Wikipedia
 | |
| Jména | |
|---|---|
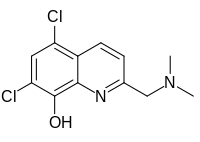
| Název IUPAC 5,7-Dichlor-2 - [(dimethylamino) methyl] chinolin-8-ol | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| UNII | |
| |
| |
| Vlastnosti | |
| C12H12Cl2N2Ó | |
| Molární hmotnost | 271.14 g · mol−1 |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
PBT2 je zinek bezpečný pro lidské použití ionofor[1] a kandidát na experimentální drogu. Je to druhá generace 8-hydroxychinolin analogový[2] zamýšlel být nástupcem cliochinol a potenciální léčba Alzheimerova choroba[3] a Huntingtonova choroba.
Klinické testy
PBT2 byl předmětem tří klinické studie fáze II pro Alzheimerovu chorobu („EURO“),[4] „IMAGINE“ & „IMAGINE EXTENSION“) a jeden pro Huntingtonova choroba („REACH2HD“)[5] soud.
Výsledky kognitivní účinnosti u Alzheimerovy choroby byly smíšené. Studie EURO prokázala některá zlepšení kognitivních funkcí, zejména domén výkonných funkcí, zatímco studie IMAGINE ne.[6][7][8][9] Ačkoli neexistují důkazy o tom, že by PBT2 měl jakýkoli přínos při Alzheimerově demenci,[10] počet subjektů léčených PBT2 na AD ve placebem kontrolovaných studiích fáze II (N ~ 76) je omezený a studie nebyly určeny k detekci kognitivních výsledků. Ve studii fáze II PBT2 s Huntingtonovou chorobou se sice celková měřená kognitivní složka nezlepšila, ale významně se zlepšila doména výkonné funkce v této složce.[6][7]
Fáze II studie AD
PBT2-201 (EURO) byla 12týdenní randomizovaná, dvojitě zaslepená, placebem kontrolovaná paralelní studie se třemi skupinami (fáze II), která hodnotila bezpečnost, snášenlivost a účinnost dvou úrovní dávek PBT2 ke zpomalení progrese onemocnění u pacientů s časnou AD. Bylo zařazeno 78 pacientů (78) a u všech byla hodnocena bezpečnost a účinnost. Léčba PBT2 v dávce 50 a 250 mg denně byla dobře tolerována u pacientů s AD během 12 týdnů léčby, přičemž existují důkazy, že dávka PBT2 250 mg / den může modulovat určité biomarkery spojené s AD, zejména významné snížení hladin CSF Abeta, a zdokonalení aspektů kognitivních funkcí, měřeno složeným skóre Executive Function a individuálním testem Trails Making Test (TMT) část B a testy plynulosti kategorie.[8]
PBT2-204 (IMAGINE) byla 12měsíční studie zobrazování amyloidů v mozku, ve které byly pacientům s mírnou AD (n = 42) podávány PBT2 250 mg nebo placebo. Bylo zařazeno 42 pacientů (42) a u všech byla hodnocena bezpečnost a účinnost. Ukázalo se, že PBT2 je bezpečný a velmi dobře tolerovaný po dobu 52 týdnů, přičemž profil nežádoucích účinků je ekvivalentní mezi skupinami s placebem a léčenými skupinami. Nebyl zjištěn žádný rozdíl v hladinách amyloidu v mozku mezi skupinami léčenými PBT2 a placebem, měřeno pomocí PiB.[11]
PBT2-204-Ext (rozšíření)[12] Třicet tři (n = 33) pacientů pokračovalo v otevřené dávce 250 mg PBT2 a bylo hodnoceno z hlediska bezpečnosti a účinnosti, přičemž studii dokončilo n = 27 pacientů. Zjištění bezpečnosti ukazují, že dlouhodobá léčba (až 104 týdnů) 250 mg PBT2 byla dobře tolerována u pacientů s prodromální nebo mírnou AD. Zjištění bezpečnosti z této studie odpovídají těm, která by se dala očekávat u populace starších dospělých s prodromální nebo mírnou AD.
Fáze II studie v HD
PBT2-203 (Reach2HD)[5] byla 6měsíční studie bezpečnosti, snášenlivosti a účinnosti u HD. Pacienti s HD v raném až středním stádiu (n = 109) dostávali PBT2 100 mg, PBT2 250 mg nebo placebo jednou denně. Primárním cílem studie bylo vyhodnotit bezpečnost a snášenlivost dvou úrovní dávek PBT2 (100 mg a 250 mg jednou denně) ve srovnání s placebem po 26 týdnech u účastníků s HD v raném až středním stadiu. Ukázalo se, že PBT2 je bezpečný a dobře tolerovaný po dobu 26 týdnů, přičemž profil nežádoucích účinků je ekvivalentní mezi skupinami s placebem a PBT2.
Sekundární cíle studie se zaměřily na specifické příznaky nebo projevy HD. Primárním cílem účinnosti studie bylo určit účinek PBT2 na poznávání měřený kognitivní testovací baterií sestávající z testu plynulé kategorie, částí A a B TM, hledání mapy, testu modalit číslicových symbolů, testu čtení slov Stroop, zrychleného klepání Úkol a MoCA. Výsledky těchto hodnocení byly použity k výpočtu tří složených z-skóre poznání - hlavní složené z-skóre, průzkumné složené z-skóre a výkonné funkce z-skóre.
PBT2 ve studii vykazoval známky zlepšení některých aspektů kognitivních funkcí. Dávka 250 mg PBT2 podávaná jednou denně vykázala lepší a statisticky významnou účinnost během 12týdenního léčebného období ve srovnání s placebem pro hlavní kompozitní kognitivní skóre (p = 0,020), průzkumné složené poznávací z-skóre (p = 0,016) , Složené Z skóre výkonné funkce (p = 0,005) a TMT část B (p <0,001), nástroj kognitivního hodnocení. Po 26 týdnech bylo TMT část B statisticky významně zlepšeno (p = 0,042) a výkonné funkční složené skóre z hlediska trendů ke zlepšení. U pacientů s časnou HD (celková funkční kapacita 11-13) se statisticky významně zlepšilo složené skóre Executive Function (p = 0,038).
Výsledky celkově naznačují, že k úplnému posouzení profilu bezpečnosti a účinnosti PBT2 u AD a HD jsou zapotřebí rozsáhlejší studie.[10][5]
Další aplikace
PBT2 se používá k léčbě bakterií rezistentních na více léčiv. V kombinaci se zinkem, zinkem ionofor Bylo prokázáno, že PBT2 zvrací rezistenci na antibiotika u řady klinicky významných bakteriálních patogenů, včetně MRSA, GAS a VRE in vitro a v modelu infekce myší.[1]
Viz také
Reference
- ^ A b Bohlmann, Lisa; De Oliveira, David M. P .; El-Deeb, Ibrahim M .; Brazel, Erin B .; Harbison-Price, Nichaela; Ong, Cheryl-lynn Y .; Rivera-Hernandez, Tania; Ferguson, Scott A .; Cork, Amanda J .; Phan, Minh-Duy; Soderholm, Amelia T .; Davies, Mark R .; Nimmo, Graeme R .; Dougan, Gordon; Schembri, Mark A .; Cook, Gregory M .; McEwan, Alastair G .; von Itzstein, Mark; McDevitt, Christopher A .; Walker, Mark J .; Kline, Kimberly A. (11. prosince 2018). „Chemická synergie mezi ionoforem PBT2 a zinkem zvrací odolnost vůči antibiotikům“. mBio. 9 (6). doi:10,1128 / mBio.02391-18.
- ^ Adlard, Paul A .; Cherny, Robert A .; Finkelstein, David I .; Gautier, Elisabeth; Robb, Elysia; Cortes, Mikhalina; Volitakis, Irene; Liu, Xiang; et al. (2008). „Rychlé obnovení poznání u Alzheimerových transgenních myší s 8-hydroxy chinolinovými analogy je spojeno se sníženou intersticiální Ap“. Neuron. 59 (1): 43–55. doi:10.1016 / j.neuron.2008.06.018. PMID 18614028.
- ^ Duce, James A .; Tsatsanis, Andrew; Cater, Michael A .; James, Simon A .; Robb, Elysia; Wikhe, Krutika; Leong, Su Ling; Perez, Keyla; et al. (2010). „Feroxidázová aktivita exportu železa β-amyloidového prekurzorového proteinu je u Alzheimerovy choroby inhibována zinkem“. Buňka. 142 (6): 857–67. doi:10.1016 / j.cell.2010.08.014. PMC 2943017. PMID 20817278. Shrnutí ležel – ScienceDaily (10. září 2010).
- ^ Lannfelt, L; et al. (2008). ""Zjištění bezpečnosti, účinnosti a biomarkerů PBT2 při cílení na Abetu jako modifikující léčbu Alzheimerovy choroby: fáze IIa, dvojitě zaslepená, randomizovaná, placebem kontrolovaná studie"". Lancet Neurol. 7: 779–786. doi:10.1016 / s1474-4422 (08) 70167-4.
- ^ A b C „Bezpečnost, snášenlivost a účinnost PBT2 u Huntingtonovy choroby: randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie fáze 2“. Lancet Neurol. 14: 39–47. 2015. doi:10.1016 / S1474-4422 (14) 70262-5. PMID 25467848.
- ^ A b „Prana Biotech vrhá 76%; droga selhává ve studii Alzheimerovy choroby“
- ^ A b „PBT2 se ponoří do fáze 2 Alzheimerovy zkoušky“
- ^ A b Lannfelt, L; et al. (2008). „Zjištění bezpečnosti, účinnosti a biomarkerů PBT2 při cílení na Abetu jako modifikující terapii Alzheimerovy choroby: fáze IIa, dvojitě zaslepená, randomizovaná, placebem kontrolovaná studie“. Lancet Neurol. 7: 779–786. doi:10.1016 / s1474-4422 (08) 70167-4.
- ^ Prana Biotechnology oznamuje špičkové výsledky studie fáze 2 IMAGINE s PBT2 u Alzheimerovy choroby 31. března 2014. http://pranabio.com/news/prana-biotechnology-announces-top-line-results-phase-2-imagine-trial -pbt2-alzheimerova choroba # .WNNuE2996Uk
- ^ A b „Neexistují důkazy o tom, že MPAC (PBT1 nebo PBT2) jsou prospěšné pro Alzheimerovu demenci“
- ^ Prana Biotechnology oznamuje špičkové výsledky studie fáze 2 IMAGINE s PBT2 u Alzheimerovy choroby 31. března 2014. http://pranabio.com/news/prana-biotechnology-announces-top-line-results-phase-2-imagine-trial -pbt2-alzheimerova choroba # .WNNuE2996Uk
- ^ Prana oznamuje bezpečnostní výsledky Alzheimerovy studie IMAGINE Extension 30. června 2015. http://pranabio.com/news/prana-announces-safety-outcomes-alzheimers-imagine-extension-trial#.WNNvF2996Uk
