Magnesocen - Magnesocene
 | |
| Jména | |
|---|---|
| Název IUPAC bis (η5-cyklopentadienyl) hořčík | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider |
|
| Informační karta ECHA | 100.110.799 |
| Číslo ES |
|
PubChem CID |
|
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C10H10Mg | |
| Molární hmotnost | 154.495 g · mol−1 |
| Nebezpečí | |
| Bezpečnostní list | Externí BL |
| Piktogramy GHS |    |
| Signální slovo GHS | Nebezpečí |
| H228, H250, H261, H314 | |
| P210, P231 + 232, P280, P303 + 361 + 353, P304 + 340 + 310, P305 + 351 + 338 + 310, P335 + 334, P422 | |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Magnesocen, také známý jako bis (cyklopentadienyl) hořčík (II) a někdy zkráceně jako MgCp2, je organokovová sloučenina vzorce Mg (η5-C5H5)2. Je to příklad s-bloku hlavní skupina sendvičová směs, strukturálně související s prvkem d-bloku metaloceny, a skládá se z centrální hořčík atom sevřený mezi dva cyklopentadienyl prsteny.
Vlastnosti
Magnesocen je bílá pevná látka při pokojové teplotě.[1] Má teplotu tání 176 ° C, i když při atmosférických tlacích sublimuje při 100 ° C.[1] Na rozdíl od ferrocen „magnesocen vykazuje mírnou disociaci a následnou asociaci iontů v polárních rozpouštědlech poskytujících elektrony (jako je ether a THF).[2]
Zatímco ferrocen je stabilní za okolních podmínek, magnesocen se rychle vystavuje působení kyslíku nebo vlhkosti a jako takový musí být syntetizován a skladován za inertních podmínek.[3]
Struktura a lepení
Jak odhalil Rentgenová krystalografická rafinace, magnesocen v pevné fázi vykazuje průměrnou vzdálenost vazby Mg-C a C-C 2,30 Å a 1,39 Å, v tomto pořadí, a Cp kroužky zaujímají střídavou konformaci (bodová skupina D5 d).[4] Plynná fáze elektronová difrakce vykazuje podobné délky vazeb, i když s Cp kroužky v zákrytové konformaci (bodová skupina D5h).[5][6]
Povaha vazby Mg-Cp byla horlivě sporná, pokud jde o to, zda je interakce primárně iontový[7][8] nebo kovalentní[5][6][9] v charakteru. Měření elektronové difrakce v plynné fázi bylo vyvoláno jako argument pro kovalentní model vibrační spektroskopie měření nabídla důkazy pro oba.
Výpočty Hartree-Fock prokázali, že na rozdíl od přechodový kov metaloceny, Mg 3d orbitaly nehrají žádnou roli ve vazbě kovových kruhů; místo toho jsou příznivé vazebné interakce se systémem Cp π dosaženy podporou dvou 3s elektronů na 3px, y orbitaly.[10] Další stabilizace je zajištěna zpětným darováním z Cp prstenů na orbitál Mg 3s. Takové interakce poskytují ve srovnání s ferrocenem nižší stupeň orbitálního překrytí, což vede k poměrně slabé vazbě kov-kruh a poměrně vysokému efektivnímu lokálnímu náboji na Mg. Experimentální důkazy ve prospěch modelu iontové vazby lze tedy vysvětlit velmi slabými, vysoce polárními interakcemi Mg-Cp. Slabá povaha tohoto režimu vazby je zodpovědná za relativní nestabilitu magnesocenu a silnou reaktivitu ve srovnání s ferrocenem.
Syntéza
Vysokoteplotní syntéza
První syntéza magnesocenu, jak uvádí F. A. Bavlna a Geoffrey Wilkinson v roce 1954 zahrnoval tepelný rozklad cyklopentadienylu Grignardovo činidlo.[11] Podobný postup nabídl W. A. Barber, při kterém cyklopentadien přímo reaguje s pevným hořčíkem při 500-600 ° C.[1] Za podmínek bez vody a kyslíku, čerstvě destilováno monomerní cyklopentadien je směrován trubkovou pecí pomocí inertního nosného plynu (jako je např hélium, argon nebo dusík ) a prošel přes hořčíkové třísky nebo prášek. Magnesocen se usazuje na chladnějších površích za výstupním koncem pece. Produktem tohoto procesu je obvykle bílá, načechraná hmota jemných mikrokrystalů, ale velké, bezbarvé monokrystaly lze získat úpravou teploty a průtoku. Pokud není potřebný pevný magnesocen, může být přijímací baňka místo toho naplněna rozpouštědlem a produkt shromážděn v roztoku, což Barber zaznamenal mnohem bezpečněji než čistá pevná látka.
Tento postup je za ideálních podmínek schopen produkovat gram produktu každé dvě minuty a to s vertikálním nastavením (ve kterém cyklopentadien směřuje dolů a produkt se shromažďuje níže) lze získat téměř čistý produkt s> 80% výtěžkem (cyklopentadienem ). Ukázalo se, že je možné horizontální nastavení, ale na úkor čistoty produktu, kvůli omezení toku plynu akumulací produktu.
Metody kapalné fáze
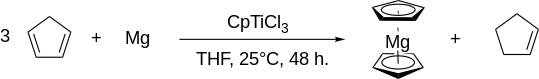
Magnesocen lze vyrobit z hořčíkových třísek v THF za mírných podmínek s cyklopentadienyltitanium trichloridem (CpTiCl3) působící jako katalyzátor.[12] Maslennikov a kol. později vykazoval podobnou katalytickou aktivitu s Cp2TiCl2, TiCl3, TiCl4a VCl3.[13] Mechanismus, jak ukazuje elektronová spinová rezonance, postupuje prostřednictvím Cp2TiH2MgCl meziprodukt.[13] Tvorba magnesocenu z elementárního hořčíku nebyla v THF pozorována bez přítomnosti katalyzátoru.[13] Pokusy nahradit THF diethyletherem, diglymem nebo benzenem vedly pouze k polymeraci cyklopentadienu.[13]
Syntéza magnesocenu a jeho derivátů byla také provedena v uhlovodík rozpouštědla, jako je heptan, z Cp a (nBu) (sBu) Mg.[14][15]
Metalizace cyklopentadienu může být také provedena pomocí komplexů Mg-Al alkyl s konečným výtěžkem magnesocenu 85%.[14]
Reaktivita a potenciální aplikace
Magnesocen slouží jako meziprodukt při přípravě metalocenů přechodných kovů:[16]
Magnesocen také prochází ligandovými výměnnými reakcemi s MgX2 (X = halogenid ) za vzniku polo sendvičových sloučenin CpMgX v THF:[17]
Výsledný napůl sendvič halogenidy mohou sloužit jako výchozí materiály pro syntézu substituovaných cyklopentadienů z organických halogenidů.[14]
Díky své vysoké reaktivitě je magnesocen atraktivním cílem polovodič výzkum jako výchozí materiál pro chemická depozice par a doping aplikace.[18][19]
magnesocen byl také zkoumán z důvodu jeho potenciálního použití jako elektrolytu v hořčíkových iontových bateriích nové generace.[2]
Reference
- ^ A b C Barber, W. A .; Jolly, William L. (1960), "Magnesium Cyclopentadienide", Anorganické syntézy„John Wiley & Sons, Ltd, s. 11–15, doi:10.1002 / 9780470132371.ch5, ISBN 9780470132371
- ^ A b Schwarz, Rainer; Pejic, marijana; Fischer, Philipp; Marinaro, Mario; Jörissen, Ludwig; Wachtler, Mario (21.11.2016). „Elektrolyty na bázi magnesocenu: nová třída elektrolytů pro hořčíkové baterie“. Angewandte Chemie International Edition. 55 (48): 14958–14962. doi:10,1002 / anie.201606448. ISSN 1521-3773. PMID 27791301.
- ^ Barber, W. A. (01.01.1957). "Nový přípravek cyklopentadienidu hořečnatého". Journal of Anorganic and Nuclear Chemistry. 4 (5–6): 373–374. doi:10.1016/0022-1902(57)80026-8. ISSN 0022-1902.
- ^ Bünder, W .; Weiss, E. (10.06.1975). „Verfeinerung der kristallstruktur von dicyclopentadienylmagnesium, (η-C5H5) 2Mg [Upřesnění krystalové struktury dicyklopentadienylmagnesium, (η5-C5H5) 2Mg]“. Journal of Organometallic Chemistry. 92 (1): 1–6. doi:10.1016 / S0022-328X (00) 91094-5. ISSN 0022-328X.
- ^ A b Starowieyski, Kazimir B .; Brunvoll, Jon; Novak, David P .; Lusztyk, Janusz; Haaland, Arne (01.01.1974). „Molekulární struktury dicyklopentadienylmagnesium a dicyklopentadienylchromia elektronovou difrakcí v plynné fázi“. Journal of the Chemical Society, Chemical Communications. 0 (2): 54–55. doi:10.1039 / C39740000054. ISSN 0022-4936.
- ^ A b Haaland, A .; Lusztyk, J .; Brunvoll, J .; Starowieyski, K. B. (11. 2. 1975). "O molekulární struktuře dicyklopentadienylmagnesium". Journal of Organometallic Chemistry. 85 (3): 279–285. doi:10.1016 / S0022-328X (00) 80301-0. ISSN 0022-328X.
- ^ Cotton, F. A .; Reynolds, L. T. (leden 1958). "Struktura a vazba cyklopentadienylthalia a bis-cyklopentadienylmagnesium". Journal of the American Chemical Society. 80 (2): 269–273. doi:10.1021 / ja01535a004. ISSN 0002-7863.
- ^ Aleksanyan, V. T .; Garbuzova, I. A .; Gavrilenko, V. V .; Zakharkin, L. I. (1977-04-12). "Vibrační spektra a struktura bis (cyklopentadienyl) hořčíku". Journal of Organometallic Chemistry. 129 (2): 139–143. doi:10.1016 / S0022-328X (00) 92483-5. ISSN 0022-328X.
- ^ Lippincott, Ellis R .; Xavier, J .; Steele, D. (01.05.1961). "Vibrační spektrum a struktura bis-cyklopentadienylmagnesium". Journal of the American Chemical Society. 83 (10): 2262–2266. doi:10.1021 / ja01471a011. ISSN 0002-7863.
- ^ Faegri Jr., K .; Almlöf, J .; Lüth, H. P. (1983-06-28). „Geometrie a vazba magnesocenu. Vyšetřování AB-initio MO-LCAO“. Journal of Organometallic Chemistry. 249 (2): 303–313. doi:10.1016 / S0022-328X (00) 99429-4. ISSN 0022-328X.
- ^ Wilkinson, G .; Cotton, F. A. (1954). Chemie a průmysl (Londýn). 11: 307.
- ^ Saito, Taro (01.01.1971). "Příprava biscyklopentadienylmagnesium pomocí katalyzátoru na bázi titanového komplexu". Journal of the Chemical Society D: Chemical Communications. 0 (22): 1422. doi:10.1039 / C29710001422. ISSN 0577-6171.
- ^ A b C d Maslennikov, Stanislav V .; Ignatyev, Roman A .; Piskounov, Alexandr V .; Spirina, Irina V. (01.03.2001). „Syntéza hořečnatého dicyklopentadienidu katalyzovaného deriváty titanu a vanadu“. Aplikovaná organokovová chemie. 15 (3): 161–168. doi:10,1002 / aoc.115. ISSN 1099-0739.
- ^ A b C Dzhemilev, USA; Ibragimov, A. G .; Tolstikov, G. A. (1991-03-26). „Syntéza a transformace„ negrignardových “organohořečnatých činidel získaných z 1,3-dienů“. Journal of Organometallic Chemistry. 406 (1–2): 1–47. doi:10.1016 / 0022-328X (91) 83169-5. ISSN 0022-328X.
- ^ Eisch, J. J .; Sanchez, R. (03.12.1985). „Snadná magnezita uhlíkových uhlíkových kyselin elektrofilními sloučeninami hořčíku alkylmagnesium“. Journal of Organometallic Chemistry. 296 (3): c27 – c31. doi:10.1016 / 0022-328X (85) 80378-8. ISSN 0022-328X.
- ^ Hull, H. S .; Reid, Allen Forrest; Turnbull, Alan G. (01.04.1967). "Teplo tvorby a vazebná energie bis (cyklopentadienyl) hořčíku". Anorganická chemie. 6 (4): 805–807. doi:10.1021 / ic50050a032. ISSN 0020-1669.
- ^ Ford, Warren T .; Grutzner, John B. (01.08.1972). "Protonová a uhlíková-13 nukleární magnetická rezonanční spektra cyklopentadienylmagnéziových sloučenin v tetrahydrofuranu". The Journal of Organic Chemistry. 37 (16): 2561–2564. doi:10.1021 / jo00981a009. ISSN 0022-3263.
- ^ Lundberg, Á; Andersson, S. G .; Landgren, G .; Rask, M. (01.07.1988). „Abruptpovy dopingové přechody využívající bis- (cyklopentadienyl) -magnesium v epitaxi kovově-organické parní fáze GaAs“. Journal of Electronic Materials. 17 (4): 311–314. Bibcode:1988JEMat..17..311R. doi:10.1007 / BF02652111. ISSN 1543-186X.
- ^ Kondo, M .; Anayama, C .; Sekiguchi, H .; Tanahashi, T. (01.08.1994). „Přechody dopingu Mg během metalorgické epitaxe plynné fáze GaAs a AlGaInP“. Journal of Crystal Growth. 141 (1–2): 1–10. Bibcode:1994JCrGr.141 .... 1K. doi:10.1016 / 0022-0248 (94) 90085-X. ISSN 0022-0248.




![{ displaystyle { ce {Mg + 2C5H6 -> [500-600 ^ oC] Mg (C5H5) 2 + H2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7670c6b5fe07f9d57ffbc3dae05cf8e8f2ca2e56)