Leuckartova reakce - Leuckart reaction
| Leuckartova reakce | |
|---|---|
| Pojmenoval podle | Rudolf Leuckart |
| Typ reakce | Substituční reakce |
| Identifikátory | |
| RSC ontologické ID | RXNO: 0000101 |
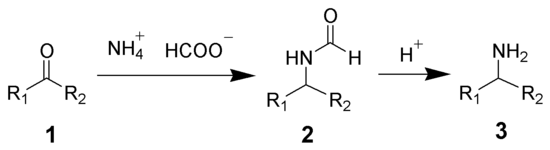
The Leuckartova reakce je chemická reakce který převádí aldehydy nebo ketony na aminy podle redukční aminace v přítomnosti tepla.[1][2] Reakce, pojmenovaná po Rudolf Leuckart, používá buď mravenčan amonný nebo formamid jako dárce dusíku a redukční činidlo.[3] Vyžaduje vysoké teploty, obvykle mezi 120 a 130 ° C; pro formamidovou variantu může být teplota vyšší než 165 ° C.[1]
Dějiny
Reakce společnosti Leuckart je pojmenována na počest jejího vývojáře, německého chemika Rudolf Leuckart (1854–1899). Objevil to topení benzaldehyd s formamidem nevytváří benzylidendiformamid podle očekávání, ale benzylamin.[4] V roce 1891 provedl kolega z Leuckartu na univerzitě v Göttingenu Otto Wallach další reakce s použitím alicyklických a terpenoidních ketonů i aldehydů, což prokázalo obecnou aplikaci.[4] V průběhu minulého století chemici objevili několik způsobů, jak zlepšit výtěžek reakce a provést ji za méně náročných podmínek. Pollard a Young shrnuli různé způsoby, kterými lze aminy tvořit: použitím buď formamidu nebo mravenčanu amonného, nebo obou, nebo přidáním kyseliny mravenčí k formamidu.[3] Nejlepšího výtěžku však dosáhne pouze použití mravenčanu amonného jako činidla.[1][3] Použití formamidu produkuje nízké výtěžky ve srovnání s mravenčanem amonným, ale výtěžky lze zvýšit použitím velkého množství formamidu nebo použitím mravenčanu amonného, síranu amonného a chloridu hořečnatého jako katalyzátory.[5]
Mechanismus
Mravenčan amonný jako činidlo:

Mravenčan amonný nejprve disociuje na kyselina mravenčí a amoniak. Amoniak poté provede a nukleofilní útok na karbonyl uhlík.[3] Kyslík deprotonuje vodík z dusíku za vzniku hydroxylové skupiny. Hydroxylová skupina je protonována vodíkem z kyseliny mravenčí, což umožňuje molekule vody odejít. Tím se vytvoří karbokation, který je rezonančně stabilizovaný. Sloučenina napadá vodík z deprotonované kyseliny mravenčí z předchozího kroku za vzniku oxidu uhličitého a aminu.
Formamid jako činidlo:

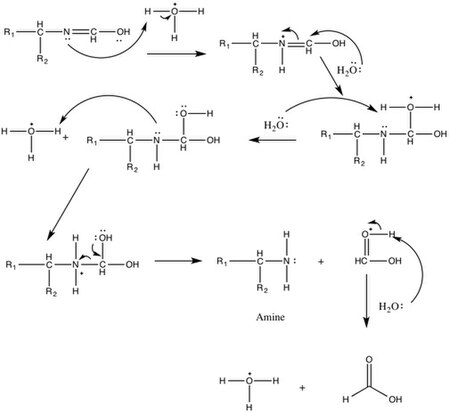
Formamid nejprve nukleofilně napadá karbonylový uhlík.[3] Kyslík je protonován abstrahováním vodíku z atomu dusíku, následným vytvořením molekuly vody, která opouští, za vzniku N-formyl derivátu, který je stabilizovaný rezonancí.[3] Voda hydrolyzuje formamid za vzniku mravenčanu amonného, který působí jako redukční činidlo a přidává se k N-formyl derivátu. Dochází k posunu hydridů, což vede ke ztrátě oxidu uhličitého. Přidá se amonný iont za vzniku iminu a uvolnění amoniaku. Imin prochází hydrolýzou za vzniku aminu, který je znázorněn na následujícím schématu.
Aplikace
Pozoruhodným příkladem Leuckartovy reakce je její použití při syntéze tetrahydro-1,4-benzodiazepin-5-onu, molekuly, která je součástí benzodiazepin rodina.[6] Mnoho sloučenin v této rodině molekul potlačuje centrální nervový systém a je spojeno s terapeutickým použitím a řadou léků, jako jsou antibiotika, látky proti vředům a látky proti HIV.[6] Vědci byli schopni syntetizovat tetrahydro-1,4-benzodiazepin-5-ony s vynikajícími výtěžky a čistotou pomocí Leuckartovy reakce. Vědci provedli reakci prostřednictvím syntéza na pevné fázi a jako redukční činidlo byla použita kyselina mravenčí.[6]
Viz také
Reference
- ^ A b C Alexander, Elliot; Ruth Bowman Wildman (1948). "Studie o mechanismu Leuckartovy reakce". Journal of the American Chemical Society. 70 (3): 1187–1189. doi:10.1021 / ja01183a091. PMID 18909189.
- ^ Ingersoll, A. W. (1937). „a-fenylethylamin“. Organické syntézy. 17: 76. doi:10.15227 / orgsyn.017.0076.
- ^ A b C d E F Pollard, C.B .; David C. Young (1951). „Mechanismus Leuckartovy reakce“. Journal of Organic Chemistry. 16 (5): 661–672. doi:10.1021 / jo01145a001.
- ^ A b Crossley, Frank S .; Maurice L. Moore (1944). "Studie o Leuckartově reakci". Journal of Organic Chemistry. 9 (6): 529–536. doi:10.1021 / jo01188a006.
- ^ Webers, Vincent J .; William F. Bruce (1948). „Leuckartova reakce: Studie mechanismu“. Journal of the American Chemical Society. 70 (4): 1422–1424. doi:10.1021 / ja01184a038. PMID 18915755.
- ^ A b C Lee, Sung-Chan; Seung Bum Park (2007). „Nová aplikace Leuckart – Wallachovy reakce pro syntézu knihovny tetrahydro-1,4-benzodiazepin-5-onů“. Chemická komunikace (36): 3714–3716. doi:10.1039 / B709768A. PMID 17851604.
