Hydrogelové zapouzdření kvantových teček - Hydrogel encapsulation of quantum dots - Wikipedia
Chování kvantové tečky (QD) v roztoku a jejich interakce s jinými povrchy má velký význam pro biologické a průmyslové aplikace, jako jsou optické displeje, značení zvířat, barviva a barvy proti padělání, chemické snímání a fluorescenční značení. Nemodifikované kvantové tečky však mají tendenci být hydrofobní, což vylučuje jejich použití ve stabilních koloidy. Kromě toho, protože poměr povrchu k objemu v kvantové tečce je mnohem vyšší než u větších částic, je termodynamická volná energie spojené s visícími vazbami na povrchu stačí k zabránění kvantové omezení z excitony. Jednou solubilizovaný zapouzdřením buď a hydrofobní interiér micela nebo a hydrofilní vnější micely mohou být QD úspěšně zavedeny do vodného média, ve kterém tvoří prodloužené hydrogel síť. V této formě lze kvantové tečky využít v několika aplikacích, které těží z jejich jedinečných vlastností, jako je lékařské zobrazování a termická destrukce maligních nádorů.[1]
Kvantové tečky
Kvantové tečky (QD) jsou v nanoměřítku polovodič částice o průměru 2-10 nm v průměru. Mají elektrické vlastnosti mezi vlastnostmi objemových polovodičů a jednotlivých molekul a také optické vlastnosti, díky nimž jsou vhodné pro aplikace, kde fluorescence je žádoucí, například lékařské zobrazování. Většina QD syntetizovaných pro lékařské zobrazování je ve formě jádrových (skořepinových) částic CdSe (ZnS). CdSe Ukázalo se, že QD mají lepší optické vlastnosti než organická barviva.[2] Plášť ZnS má dvojí účinek:
- komunikovat s visící dluhopisy které by jinak vedly k agregaci částic, ztrátě vizuálního rozlišení a impedanci kvantové omezení účinky
- k dalšímu zvýšení fluorescence samotných částic.[3]
Problémy s kvantovými tečkami CdSe (ZnS)
Přes jejich potenciál pro použití jako kontrastních látek pro lékařské zobrazovací techniky, jejich použití in vivo brání cytotoxicita z Kadmium. K řešení tohoto problému byly vyvinuty metody „zabalení“ nebo „zapouzdření“ potenciálně toxických QD v biologicky inertních polymerech, aby se usnadnilo použití v živé tkáni. I když jsou QD bez Cd komerčně dostupné, nejsou vhodné pro použití jako náhrada organických kontrastů.[4] Další problém s nanočásticemi CdSe (ZnS) je významný hydrofobicita, což brání jejich schopnosti vstupovat do roztoku s vodnými médii, jako je krev nebo míšní tekutina. Určitý hydrofilní polymery by mohly být použity k tomu, aby byly tečky rozpustné ve vodě.
Syntéza zapouzdřeného polymeru
RF-PEG syntéza
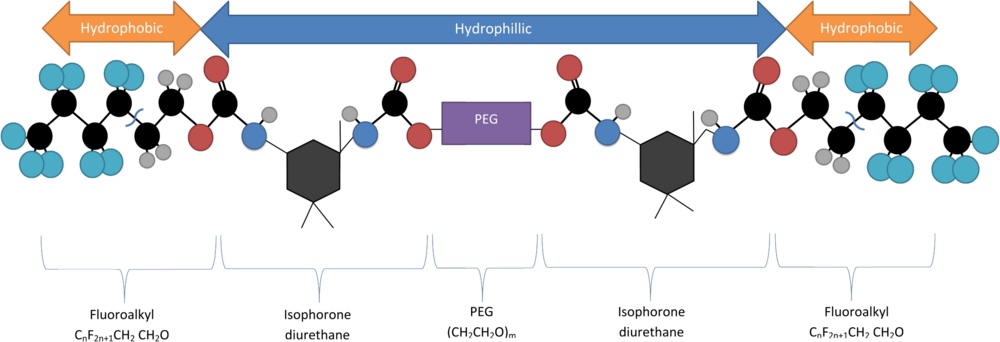
Jedna pozoruhodná technika zapouzdření kvantových teček zahrnuje použití molekuly polyethylenglykolu s dvojitým fluoralkylovým koncem (RF-PEG) jako povrchově aktivní látka, která při své kritické koncentraci micel (CMC) spontánně vytvoří micelární struktury. Kritická micelární koncentrace R.F-PEG závisí na délce PEG části polymeru. Tato molekula se skládá z hydrofilní látky KOLÍK páteř se dvěma hydrofilními koncovými skupinami (C.nF2n + 1-CH2CH2O) připojený přes isoforon diurethan.[5] Syntetizuje se dehydratací roztoku 1,3-dimethyl-5-fluoruracilu a PEG a jejich smícháním v přítomnosti těžké vody (D2O) prostřednictvím a sonikátor pak kombinovat.[6]

Micelizace

V příslušných případech Krafftova teplota a kritická koncentrace micel tyto molekuly budou tvořit jednotlivé smyčky slzných kapek, kde jsou hydrofobní konce přitahovány k sobě navzájem, k dalším molekulám a také k podobně hydrofobním QD. Toto tvoří nabitou micelu s hydrofilním vnějším obalem a hydrofobním jádrem.[6]
Při zapouzdření hydrofobů tímto způsobem je důležité zajistit, aby velikost částic byla vhodná pro použitou základní kostru PEG, protože počet PEG merných jednotek (obvykle s MW 6K nebo 10K Daltony ) určuje maximální velikost částic, které mohou být úspěšně obsaženy v jádře micely.
Pro stanovení průměrného průměru D QD se použije následující empirická rovnice:
Kde
- je průměr CdSe QD v nm
- je vlnová délka prvního absorpčního píku v nm
Role pláště ZnS
Je to během zapouzdření že skořápka ZnS hraje obzvláště důležitou roli v tom, že pomáhá předcházet aglomeraci částic CdSe, které neměly skořápku, obsazením výše zmíněných vazeb na povrchu tečky; ke shlukování však stále může docházet sekundárními silami, které vznikají z běžné hydrofobicity. To může mít za následek více částic v každé micele, což může negativně ovlivnit celkové rozlišení. Z tohoto důvodu je pro dosažení optimálních zobrazovacích vlastností nezbytných několik kombinací délky řetězce PEG a průměru částic.

Hydrogelová síť
Po počátečním zapouzdření zbývající molekuly vytvoří spojení mezi jednotlivými micelami a vytvoří ve vodném médiu síť zvanou a hydrogel, vytvoření difúzní a relativně konstantní koncentrace zapouzdřené částice v gelu. Tvorba hydrogelů je jev pozorovaný u superabsorpční polymery, nebo „kašovité prášky“, ve kterých polymer, často ve formě prášku, absorbuje vodu, stává se až 99% kapalným a 30–60krát větším.[7]
Stokes-Einsteinova rovnice

The difuzivita sférických částic v suspenzi je aproximován Stokes-Einstein rovnice:[6]
- kde
- je plynová konstanta
- je teplota
- je poloměr částic
- je číslo Avogadra
- je hydrogelová viskozita
Typický R.F-PEG hydrogelové difuzivity pro 2 nm kvantové tečky jsou řádově 10−16 m2/ s, takže suspenze kvantových teček bývají velmi stabilní. Viskozitu hydrogelu lze stanovit pomocí reologických technik.
Reologie micel
Při zapouzdření hydrofobních nebo potenciálně toxických materiálů je důležité, aby zapouzdřovací látka zůstala neporušená, když je uvnitř těla. Studium reologických vlastností micel umožňuje identifikaci a výběr polymeru, který je nejvhodnější pro použití v dlouhodobých biologických aplikacích. RF-PEG vykazuje vyšší kvalitu reologické vlastnosti při použití in vivo.
Důležitost délky polymeru
Vlastnosti polymeru jsou ovlivněny délkou řetězce. Správná délka řetězu zajišťuje, že se zapouzdřovač v průběhu času neuvolní. Vyvarování se uvolňování QD a jiných toxických částic je zásadní, aby se zabránilo neúmyslné buňce nekróza u pacientů. Délka polymeru je řízena dvěma faktory:
- Hmotnost páteře PEG v Daltonech, představovaná #K (tisíce Daltonů)
- Délka hydrofobních konců, označená počtem atomů uhlíku v terminální skupině (C #).
Zvětšení délky PEG zvyšuje rozpustnost polymeru. Pokud je však řetězec PEG příliš dlouhý, micela se stane nestabilní. Bylo pozorováno, že stabilní hydrogel lze vytvořit pouze s PEG kostry o hmotnosti mezi šesti a deseti tisíci Daltonů.[8]
Na druhé straně zvětšování délky hydrofobních koncových skupin snižuje rozpustnost ve vodě. Pokud je hydrofob pro danou hmotnost PEG příliš krátký, polymer se jen rozpustí v roztoku a pokud je příliš dlouhý, polymer se vůbec nerozpustí. Obecně platí, že dvě koncové skupiny vedou k nejvyšší konverzi na micely (91%):[8]
Maxwellova tekutina
Při molekulárních hmotnostech mezi 6 000 a 10 000 Daltons R.F-PEG hydrogel působí jako a Materiál Maxwell, což znamená, že tekutina má obojí viskozita a pružnost. To je určeno měřením modulu plató, modul pružnosti pro viskoelastický polymer je konstantní nebo "uvolněný", když je deformován, v rozsahu frekvencí pomocí oscilační reologie.[9][10] Vynesení integrálů hodnot modulu modulu prvního a druhého řádu, a Cole-Coleův graf je získán, který po namontování na model Maxwell poskytuje následující vztah:
Kde
- je modul plató
- je kmitočet oscilace v radiánech za sekundu
Mechanické vlastnosti společného RF-PEG molekuly
Na základě maxwellovského chování hydrogelu a pozorování eroze pomocí povrchová plazmonová rezonance (SPR), vyplývají následující údaje pro 3 běžné RF-PEG typy v jejich specifikovaných koncentracích:[11][12]
| 6.8 | 6.5 | 11.0 | |
| 1.2 | 0.029 | 0.023 | |
| 14.4 | 18.5 | 56.1 | |
| 18 | 0.53 | 1.5 | |
| 94 | 94 | 89 |
XKCY označuje X tisíc Daltony z molekulová hmotnost a Y uhlík atomy.
Tyto hodnoty nám mohou poskytnout informace o stupni zapletení (nebo stupni zesíťování, v závislosti na uvažovaném polymeru). Obecně platí, že vyšší stupně zapletení vedou k vyššímu času potřebnému pro návrat polymeru do nedeformovaného stavu nebo relaxační časy.
Aplikace
Hydrogelové zapouzdření QD otevírá novou řadu aplikací, například:
- Biosenzory
- Enzymy a další bioaktivní molekuly slouží jako jednotky biologického rozpoznávání, zatímco QD slouží jako signalizační jednotky. Přidáním enzymů do hydrogelové sítě QD lze obě jednotky kombinovat za vzniku a biosenzor. Enzymatická reakce, která detekuje konkrétní molekulu, způsobí zhášení fluorescence QD. Tímto způsobem lze pozorovat umístění sledovaných molekul.[13]
- Vliv buněk a zobrazování
- Přidání nanočástic oxidu železa do micel QD jim umožňuje být fluorescenční a magnetické. Tyto micely lze pohybovat v magnetickém poli a vytvářet koncentrační gradienty, které ovlivňují procesy buňky.[14]
- Zlatá hypertermie
- Při excitaci vysokoenergetickým zářením, například laserem, nanočástice zlata emitují tepelné pole. Tento jev lze použít jako formu hypertermická terapie zničit maligní rakoviny bez poškození okolních tkání. V kombinaci s QD v hydrogelu by to mohlo usnadnit monitorování léčby nádoru v reálném čase.[15]
Viz také
- Hydrofob
- Termodynamika micelizace
- Krafftova teplota
- Povrchově aktivní látky
- Čisticí prostředek
- Entropická síla
- Cole – Coleova rovnice
Reference
- ^ Glazer, ES; SA Curley (červenec 2010). „Radiofrekvenční pole indukovaná tepelná cytotoxicita v rakovinných buňkách ošetřených fluorescenčními nanočásticemi“. Rakovina. 116 (13): 3285–93. doi:10.1002 / cncr.25135. PMC 2928886. PMID 20564640.
- ^ Resch-Genger, Ute; Grabolle; Cavaliere-Jaricot; Nitschke; Nann (srpen 2008). "Kvantové tečky versus organická barviva jako fluorescenční štítky". Přírodní metody. 5 (9): 763–775. doi:10.1038 / nmeth.1248. PMID 18756197.
- ^ Angell, Joshuo. "Syntéza a charakterizace kvantových bodů Core-Shell CdSe-ZnS". Citovat deník vyžaduje
| deník =(Pomoc) - ^ Jin, Shan; Yanxi Hu; Zhanjun Gu; Lei Liu; Hai-Chen Wu (červenec 2011). "Aplikace kvantových teček v biologickém zobrazování". Journal of Nanomaterials.
- ^ Lundberg, D.J .; R.G. Hnědý; J.E. Glass; R.R.Eley (1994). "Syntéza, charakterizace a reologie roztoku modelových hydrofobně modifikovaných, ve vodě rozpustných ethoxylovaných uretanů". Langmuir. 10 (9): 3027–3034. doi:10.1021 / la00021a028.
- ^ A b C Mathias, Errol V .; Julia Aponte; Julia A. Kornfield; Yong Ba (říjen 2010). "Vlastnosti plnění a difúze malých molekulárních léčiv ve fluorovaném hydrogelu PEG studované pomocí 1H molekulární difúzní NMR a 19F spinové difúzní NMR". Koloidní a polymerní věda. 288 (18): 1655–1663. doi:10.1007 / s00396-010-2304-9. PMC 2982959. PMID 21170115.
- ^ Horie, K, et. al, 890.
- ^ A b Tae, Giyoong; Julia A. Kornfield; Jeffry A. Hubbell; Diethelm Johannsmann; Thieo E. Hogen-Esch (květen 2001). „Hydrogely s kontrolovanými charakteristikami povrchové eroze při samosestavování poly (ethylenglykolu) s fluorovaným alkylovým zakončením“. Makromolekuly. 34 (18): 6409–6419. Bibcode:2001MaMol..34.6409T. doi:10.1021 / ma0107511.
- ^ Wyss, Hans; Ryan J. Larson; David A. Weitz (2007). „Oscilační reologie: Měření viskoelastického chování měkkých materiálů“ (PDF). G.I.T. Laboratoř. 3 (4): 68–70.
- ^ Rubinstein, M .; A.V. Dobrynin (1997). Trendy ve vědě o polymerech. 5 (6): 181. Chybějící nebo prázdný
| název =(Pomoc) - ^ Aust, E.F .; S. Ito; M. Sawodny; W. Knoll (1994). Trendy ve vědě o polymerech. 2: 313. Chybějící nebo prázdný
| název =(Pomoc) - ^ Tae, G .; J.A. Kornfield; J.A. Hubbell; Diethelm Johannsmann (17. září 2002). „Anomální sorpce v tenkých vrstvách poly (ethylenglykolu) s fluorovaným alkylem“. Langmuir. 18 (21): 8241–8245. doi:10.1021 / la020255l.
- ^ Yuan, Jipei; Dan Wen; Nikolai Gaponik; Alexander Eychmuller (22. listopadu 2012). „Enzymově zapouzdřující hydrogely a xerogely kvantové tečky jako biosenzory: multifunkční platformy jak pro biokatalýzu, tak pro fluorescenční sondování“. Angewandte Chemie International Edition. 52 (3): 976–979. doi:10,1002 / anie.201205791. PMID 23172829.
- ^ Roullier, Victor; Fabien Grasset; Fouzia Boulmedais; Franck Artzner; Olivier Cador; Vale´rie Marchi-Artzner (15. října 2008). „Malé bioaktivované magnetické micely s kvantovou tečkou“ (PDF). Chemie materiálů. 20 (21): 6657–6665. doi:10,1021 / cm801423r. Citováno 8. června 2013.
- ^ Huff, Terry; Ling Tong; Yan Zhao; Matthew Hansen; Jin-Xin Cheng; Alexander Wei (2007). „Hypertermický účinek nanorodů zlata na nádorové buňky“ (PDF). Nanomedicína. 2 (1): 125–132. doi:10.2217/17435889.2.1.125. PMC 2597406. PMID 17716198.












![{G ^ { prime prime} ( omega) = } [G ^ { prime} ( omega) G_0 - {G ^ { prime} ( omega)} ^ 2] ^ {- {1 nad2}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7065af8a404b619803278cc63fc916e7fbb746f2)









