Hexachlorethan - Hexachloroethane
 | |
 | |
| Jména | |
|---|---|
| Název IUPAC Hexachlorethan | |
| Ostatní jména Chlorid uhličitý, hexanchlorid, perchlorethan | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Informační karta ECHA | 100.000.606 |
| Číslo ES |
|
| KEGG | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C2Cl6 | |
| Molární hmotnost | 236,74 g / mol |
| Vzhled | bezbarvé krystaly[1] |
| Zápach | jako kafr[1] |
| Hustota | 2,091 g / ml při 25 ° C |
| Bod tání | vznešené |
| Bod varu | 183 až 185 ° C (361 až 365 ° F; 456 až 458 K) |
| 0,005% (22,2 ° C)[1] | |
| Tlak páry | 0,2 mmHg (20 ° C)[1] |
| -112.7·10−6 cm3/ mol | |
| Nebezpečí | |
| Hlavní nebezpečí | Pravděpodobný karcinogen, nebezpečná deprese CNS |
| NFPA 704 (ohnivý diamant) | |
| Bod vzplanutí | nehořlavý[1] |
| Smrtelná dávka nebo koncentrace (LD, LC): | |
LD50 (střední dávka ) | 4460 mg / kg (potkan, orální) 4970 mg / kg (morče, orální) |
| NIOSH (Limity expozice USA pro zdraví): | |
PEL (Dovolený) | TWA 1 ppm (10 mg / m3) [kůže][1] |
REL (Doporučeno) | Ca TWA 1 ppm (10 mg / m3) [kůže][1] |
IDLH (Okamžité nebezpečí) | Ca [300 ppm][1] |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
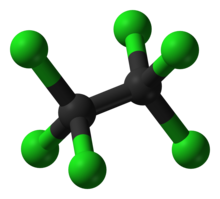
Hexachlorethan, známý také jako perchlorethan (PCA), je organochlorová sloučenina se vzorcem (CCl3)2. Je bílé pevné látky při pokojové teplotě se zápachem podobným kafru.[3] To bylo používáno armádou v kouřové směsi, například vysunutí základny kouřová munice (kouřové granáty ).
Výroba
Hexachlorethan je vedlejším produktem mnoha průmyslových odvětví chlorování procesy:
- C2H6 + 6 Cl2 → C.2Cl6 + 6 HCl
Aplikace
Hexachlorethan se používá při formulaci extrémního tlaku maziva. Používá se také jako agent přenosu řetězce v emulzní polymerace kopolymeru propylen-tetrafluorethylenu. Hexachlorethan byl použit jako anthelmintikum v veterinární medicína, urychlovač kaučuku, složka fungicidních a insekticidních formulací, jakož i repelent můry a změkčovadlo pro estery celulózy.[3]
Hexachlorethan se používá při výrobě odplyňovacích pelet k odstranění bublin plynného vodíku z roztaveného hliníku ve slévárnách hliníku. Toto použití, stejně jako podobné použití v hořčík, je v Evropská unie. To bylo vyřazeno již v roce 1999 v Spojené státy.[4]
Použijte jako kouřový prostředek
Kouřové granáty, nazývané hexachlorethanový (HCE) kouř nebo HC kouř, využívají směs obsahující zhruba stejné části HCE a oxid zinečnatý a přibližně 6% zrnitý hliník. Tyto kouře jsou toxické, což se připisuje výrobě chlorid zinečnatý (ZnCl2).[5]
Použití proti demonstrantům
Federální síly použily hexachlorethan proti demonstrantům v Portland, Oregon Během George Floyd protestuje.[6]
Toxicita
Hexachlorethan není při perorálním podání zvlášť toxický,[7] ale je považován za docela toxický při adsorpci kůží. Primárním účinkem je deprese centrálního nervového systému.[3] IDLH se udává jako 300 ppm a OSHA PEL je 1 ppm (kůže).[7] Dá se rozumně předpokládat, že jde o karcinogen.[4]
Reference
- ^ A b C d E F G h NIOSH Kapesní průvodce chemickými nebezpečími. "#0316". Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ "Hexachlorethan". Koncentrace bezprostředně nebezpečné pro život a zdraví (IDLH). Národní institut pro bezpečnost a ochranu zdraví při práci (NIOSH).
- ^ A b C Snedecor, Gayle (1999). „Hexachlorethan“. V Kroschwitz, Jacqueline I. (ed.). Kirk-Othmer Stručná encyklopedie chemické technologie (4. vydání). New York: John Wiley & Sons, Inc. str. 428. ISBN 978-0471419617.
- ^ A b „Zpráva o karcinogenech, dvanácté vydání, hexachlorethan“ (PDF). NIH. 2011. Citováno 2012-10-04.
- ^ „Příloha E: Prostředky na kouření a maskování“ (PDF). Australské ministerstvo pro záležitosti veteránů. Prosince 2003. str. E-3. Archivovány od originál (PDF) dne 2014-02-13. Citováno 2012-10-04.
- ^ https://theintercept.com/2020/10/10/portland-tear-gas-chemical-grenades-protests/
- ^ A b „Dokumentace pro bezprostředně nebezpečné pro život nebo zdraví (IDLHs) hexachlorethan“. NIOSH. Květen 1994. Citováno 2012-10-04.

