Bromobiman - Bromobimane
 | |
 | |
| Jména | |
|---|---|
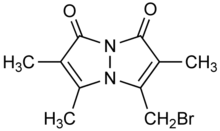
| Název IUPAC 3- (brommethyl) -2,5,6-trimethyl-1H,7H- | |
| Ostatní jména Bromobiman, mBBr | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| UNII | |
Řídicí panel CompTox (EPA) | |
| |
| |
| Vlastnosti | |
| C10H11BrN2Ó2 | |
| Molární hmotnost | 271.114 g · mol−1 |
| Bod tání | 152 až 154 ° C (306 až 309 ° F; 425 až 427 K) |
| v MeOH, DMF, DMSO | |
| Nebezpečí | |
| Hlavní nebezpečí | alkylační činidlo |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Bromobiman nebo monobromobiman je heterocyklická sloučenina a bimanové barvivo který se používá jako činidlo v biochemie. I když samotný brombiman je v podstatě nefluorescenční, je alkyláty thiol skupiny, vytěsnění bromu a přidání fluorescenční značky (λemise = 478 nm) na thiol. Jeho alkylační vlastnosti jsou srovnatelné s jodacetamid.[1]
Syntéza
Bromobiman se připraví z 3,4-dimethyl-2-pyrazolin-5-onu (kondenzační produkt ethyl-2-methylacetoacetátu s hydrazinem) chlorací a následným bazickým zpracováním; s vodným K.2CO3 za heterogenních podmínek požadováno syn-biman, 2,3,5,6-tetramethyl-lH,7H-pyrazolo [1,2-A] pyrazol-1,7-dion, je hlavním produktem. Poté může být selektivně bromován na cílový brombiman (s 1 ekvivalentem Br2; nebo dibromobiman, pokud 2 ekvivalenty Br2 Jsou používány):[2]

Bromobimany jsou sloučeniny citlivé na světlo a měly by být uchovávány v chladu a chráněny před světlem.
Reference
- ^ Paul C. Chinn; Vincent Pigiet a Robert C. Fahey (1986). „Stanovení thiolových proteinů pomocí značení monobromobimanem a vysoce výkonné kapalinové chromatografické analýzy: Aplikace na thioredoxin z Escherichia coli“. Analytická biochemie. 159 (1): 143–149. doi:10.1016/0003-2697(86)90319-2. PMID 3544950.
- ^ Kosower, Edward M .; Pazhenchevsky, Barak (1980). "Bimany. 5. Syntéza a vlastnosti syn- a proti-1,5-Diazabicyklo [3.3.0] oktadienediony (9,10-dioxabimany) ". Journal of the American Chemical Society. 102 (15): 4983–4993. doi:10.1021 / ja00535a028.
