Aspergillus giganteus - Aspergillus giganteus - Wikipedia
| Aspergillus giganteus | |
|---|---|
| Vědecká klasifikace | |
| Království: | Houby |
| Divize: | Ascomycota |
| Třída: | Eurotiomycetes |
| Objednat: | Eurotiales |
| Rodina: | Trichocomaceae |
| Rod: | Aspergillus |
| Druh: | A. giganteus |
| Binomické jméno | |
| Aspergillus giganteus Wehmer (1901)[1] | |
Aspergillus giganteus je druh z houba v rod Aspergillus (z latiny „aspergillum“, což znamená „postřikovač svěcené vody“), který roste jako plíseň.[2] Poprvé to popsal v roce 1901 Wehmer,[1] a je jedním ze šesti Aspergillus druhy z Clavati část podrod Fumigati.[3] Jeho nejbližší taxonomičtí příbuzní jsou Aspergillus rhizopodus (Rai a kol., 1975)[4][3] a Aspergillus longivescia (Huang a Raper, 1971).[5][3]
Morfologie

Jako většina Aspergillus druh,[6] A. giganteus reprodukuje nepohlavně a nebyl pozorován v sexuálním stavu.[3] Podobně jako u jiných druhů v Clavati, A. giganteus produkuje řadu konidioforů, které se vyznačují sklovitými a průsvitnými stonkovitými strukturami nazývanými stipes a klubkovitá aspergilla, které se zužují směrem ke špičkám.[3] Volaly modrozelené asexuální výtrusy konidie formulář na těchto tipech.[3]
Na makroskopické úrovni A. giganteus kolonie se vyznačují sametovou strukturou.[3] Kolonie jsou zpočátku často bílé a po vystavení světlu získávají bledě modrozelenou barvu.[3]

Na mikroskopické úrovni A. giganteus produkuje dva hroty konidioforů, které mají zřetelné stipky a vezikuly. První z těchto konidioforů jsou obvykle 2-3 mm vysoké, včetně délky třeně.[3] Tyto kratší konidiofory produkují klavátové váčky, které jsou 100-250 μm dlouhé a 30-50 μm široké.[3] Druhý typ konidioforů je mnohem větší, přibližně 1–5 cm dlouhý.[3] Většina z této délky je způsobena podlouhlými čepy.[3] Tyto podlouhlejší konidiofory jsou fototropní, což znamená, že jsou schopni se vyvíjet a růst pouze za přítomnosti světla.[3] Vezikuly produkované dlouhými konidiofory jsou dlouhé 400-600 μm a široké 120-180 μm, což je více než dvojnásobek velikosti vezikul produkovaných jejich kratšími protějšky.[3]
Společně vezikul a phialides tvoří konidiální hlavu. v A. giganteus, tyto hlavy jsou modrozelené barvy a s dozráváním formy se dělí na dva nebo více sloupců.[3] Z těchto konidiálních hlav se tvoří konidie. Konidie z A. giganteus jsou relativně silnostěnné a lze je odlišit hladkým eliptickým vzhledem a velikostí (3,5–4,5 × 2,4–3,0 μm). Tyto vlastnosti jsou charakteristické pro oba typy konidioforů.[3]A. giganteus lze odlišit od jiných Aspergillus druhy umístěné v rámci Clavati mikroskopickou morfologií a jedinečnou kombinací extrolitů, což jsou sloučeniny syntetizované buňkami a následně vylučované buňkami na obranu proti bakteriím a jiným houbám.[3][8] Morfologicky, A. giganteus postrádá rhizoidní buňky nohou přítomné v A. rhizopodus, a má váčkové váčky, které stojí na rozdíl od podlouhlých váčků A. longivesica.[3] Pokud jde o syntézu extrolitu, ačkoli A. giganteus vyrábí mykotoxiny a antibiotika které jsou charakteristické pro všechny Clavati druhy druhů (např patulin,[8] tryptoquivalines and tryptoquivalones,[3] a alfa-sarciny),[9] také produkuje extrolity, které nejsou syntetizovány jeho nejbližšími příbuznými. Patří mezi ně několik různých karotinoidy[10] a penicilin - jako klavinformin.[11]
Ekologie
A. giganteus se vyskytuje po celém světě a byl oficiálně dokumentován v Nigérii, Spojených státech, Egyptě, Mexiku, Panamě, Německu, Surinamu, Nizozemsku a Polsku.[3] Je to nejčastěji hnůj, ale bude růst v alkalické půdě a dřevěných podkladech.[3] Jako saprotrofická forma[2] A. giganteus získává svoji energii vstřebáváním živin ze substrátů, ve kterých roste. Ačkoli mnoho dalších Aspergillus a Clavati části druhů jsou známé patogeny lidí, A. giganteus nemá žádné hlášené patogenní účinky.[3]
V laboratoři A. giganteus byl kultivován na obou Czapek kvasnicový extrakt agar (CYA) desky a desky Malt Extract Agar Oxoid® (MEAOX),[3] Jak je ukázáno níže.
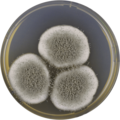
Aspergillus giganteus rostoucí na desce CYA
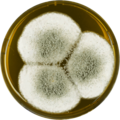
Aspergillus giganteus rostoucí na desce MEAOX
Ekonomický význam
Antifungální protein (AFP)
A. giganteus produkuje antifungální protein (AFP), který má potenciální aplikace pro prevenci plísňových infekcí ve farmaceutickém i zemědělském prostředí. Bylo prokázáno, že AFP omezuje růst mnoha ekonomicky důležitých vláknitých hub.[12] Tyto zahrnují Aspergillus fumigatus, hlavní příčina aspergilóza u lidí[12] a další Aspergillus druh;[13] Fusarium oxysporum a související Fusarium druh,[12] běžné patogeny rostlin rajčete, fazolí, banánů, melounů, bavlny a cizrny;[14] Magnaporthe grisea patogen rýže a obilnin;[2] a Botrytis cinearapatogenní pro pelargónie a jiné ekonomicky významné okrasné rostliny.[15] AFP může navíc omezit růst oomycete Phytopthera infestans,[2] patogen neslavný pro způsobení pozdní plíseň v bramborách (hlavní příčina Velký hladomor Irska ) a rajčata.[16]
Kromě vysokého potenciálu pro úspěch v boji proti výše uvedeným infekcím AFP neinhibuje životaschopnost droždí, bakterie, savčí,[17] nebo rostlinné buňky.[18] Protože existuje mnoho vláknitých druhů hub, které nereagují na AFP, je pravděpodobné, že škodlivé účinky proteinu jsou druhově specifické.[13][19] AFP jako takový by mohl být použit k léčbě a prevenci infekce velmi specifickými patogeny bez poškození pacientů nebo hostitelských rostlin. Dále může být protein snadno syntetizován fermentací A. giganteus a je odolný vůči sluchu. Ve srovnání s jinými antifungálními léčbami je zapotřebí malého množství proteinu, aby se zabránilo růstu škodlivých patogenů.[20] V kombinaci se skutečností, že AFP téměř úplně blokuje růst citlivých, patogenních hub (na rozdíl od antifungálních ošetření ozónem, peroxidem vodíku a chlordioxidem, které se v současné době používají v zemědělských systémech)[18] tyto faktory zdůrazňují potenciál AFP jako levného, hromadně vyrobitelného a extrémně účinného řešení patogenní infekce.
Režim činnosti AFP
Na cysteiny bohatý,[20] amfipatický[13] Protein inhibuje růst patogenů AFP-senstivie více cestami. Za prvé, AFP může inhibovat růst buněk inhibicí chitin syntéza.[12] U citlivých hub AFP aktivuje cestu integrity buněčné stěny, čímž zvyšuje expresi genu α-1,3-glukan syntázy A odpovědného za remodelaci buněčných stěn a inhibici tvorby chitinu.[21] AFP může také změnit propustnost buněčné membrány citlivých hub,[19] zejména z Aspergillus niger,[13] nebo způsobit okamžité, trvalé zvýšení klidového potenciálu buněk kationu vápníku, které často vede k programované buněčné smrti.[21] Každá z těchto cest nakonec vede ke smrti patogenu citlivého na AFP. Ačkoli je zapotřebí více výzkumu k identifikaci toho, jak tyto cesty fungují v choti, široká škála způsobů působení AFP zdůrazňuje, že protein může interagovat s citlivými patogeny různými způsoby, že se tyto patogeny liší svou citlivostí na AFP.[13]
Předběžné studie o aplikacích AFP
V předběžných studiích o farmaceutických a zemědělských aplikacích AFP vědci použili AFP k zastavení růstu Phytopthera infestans[2] a Aspergillus druh[12][13][19] v kultuře. Při aplikaci řešení AFP na listy a kořeny rostlin se infekce Botrytis cineara v pelargónie[15] a Magnaporthe grisea u rostlin rýže byly odstraněny.[2] V každém z těchto případů způsobil AFP deformace v hyfách citlivých hub, což mělo za následek snížené prodloužení hyf a neschopnost patogenu růst.[2][15] Kromě přímé aplikace na rostlinné struktury může být gen kódující AFP upraven do genomů rostlin ovlivněných houbami citlivými na AFP, takže rostliny jsou schopné syntetizovat protein samy.[22][23][24] Tato technika byla úspěšně použita ke snížení infekce pomocí Puccinia substriata, hlavní příčina nemoci rzi, a Sclerospora graminicola, původce plísní, v rostlinách perlového prosa,[22] stejně jako infekce Magnaporthe grisea v rostlinách rýže.[23][24] Ačkoli genetické vylepšení zastavilo infekci v laboratorních a skleníkových podmínkách, vědci pokračují v debatách o škálovatelnosti úpravy rostlinných genomů a schopnosti samotných rostlin syntetizovat dostatek AFP k boji proti patogenní infekci v terénu.[23][24]
Reference
- ^ A b Wehmer 1901, Mem. Soc. Phys. Genève 33 (2): 85
- ^ A b C d E F G Vila L, Lacadena V, Fontanet P, Martinez del Pozo A, San Segundo B (listopad 2001). „Protein z plísně Aspergillus giganteus je silným inhibitorem plísňových rostlinných patogenů“. Molekulární interakce rostlin a mikrobů. 14 (11): 1327–31. doi:10.1094 / MPMI.2001.14.11.1327. PMID 11763131.
- ^ A b C d E F G h i j k l m n Ó str q r s t u proti w X Varga J, Due M, Frisvad JC, Samson RA (2007). „Taxonomická revize sekce Aspergillus Clavati na základě molekulárních, morfologických a fyziologických údajů“. Studie v mykologii. 59: 89–106. doi:10.3114 / sim.2007.59.11. PMC 2275193. PMID 18490946.
- ^ Rai JN, Wadhwani K, Agarwal SC (červen 1975). "Aspergillus rhizopodus sp.nov. Z indických alkalických půd". Transakce Britské mykologické společnosti. 64 (3): 515–517. doi:10.1016 / s0007-1536 (75) 80153-7. ISSN 0007-1536.
- ^ Huang LH, Raper KB (leden 1971). "Aspergillus Longivesica, nový druh z nigerijské půdy". Mykologie. 63 (1): 50–57. doi:10.1080/00275514.1971.12019081. ISSN 0027-5514.
- ^ Dyer PS, Paoletti M (květen 2005). „Reprodukce v Aspergillus fumigatus: sexualita u údajně nepohlavního druhu?“. Lékařská mykologie. 43 Suppl 1 (s1): S7-14. doi:10.1080/13693780400029015. PMID 16110786.
- ^ "Aspergillus". Mykologie online. University of Adelaide. Citováno 2019-05-17.
- ^ A b Varga J, Rigó K, Molnár J, Tóth B, Szencz S, Téren J, Kozakiewicz Z (2003). "Produkce mykotoxinů a evoluční vztahy mezi druhy Aspergillus sekce Clavati". Antonie van Leeuwenhoek. 83 (2): 191–200. doi:10.1023 / A: 1023355707646. PMID 12785313.
- ^ Lin A, Huang KC, Hwu L, Tzean SS (leden 1995). „Produkce ribotoxinů typu II druhy Aspergillus a příbuznými houbami na Tchaj-wanu“. Toxicon. 33 (1): 105–10. doi:10.1016/0041-0101(94)00140-4. PMID 7778122.
- ^ van Eijk GW, Mummery RS, Roeymans HJ, Valadon LR (01.09.1979). "Srovnávací studie karotenoidů Aschersonia aleyroides a Aspergillus giganteus". Antonie van Leeuwenhoek. 45 (3): 417–422. doi:10.1007 / BF00443280. ISSN 1572-9699. PMID 554534.
- ^ Florey HW, Jennings MA, Philpot FJ (leden 1944). „Claviformin z Aspergillus giganteus Wehm“. Příroda. 153 (3874): 139. Bibcode:1944Natur.153..139F. doi:10.1038 / 153139a0.
- ^ A b C d E Hagen S, Marx F, Ram AF, Meyer V (duben 2007). „Antifungální protein AFP z Aspergillus giganteus inhibuje syntézu chitinu u citlivých hub“. Aplikovaná a environmentální mikrobiologie. 73 (7): 2128–34. doi:10.1128 / AEM.02497-06. PMC 1855660. PMID 17277210.
- ^ A b C d E F Meyer V (únor 2008). „Malý protein, který bojuje proti houbám: AFP jako nové slibné antifungální činidlo biotechnologické hodnoty“. Aplikovaná mikrobiologie a biotechnologie. 78 (1): 17–28. doi:10.1007 / s00253-007-1291-3. PMID 18066545.
- ^ Michielse CB, Rep M (květen 2009). „Aktualizace profilu patogenu: Fusarium oxysporum“. Molekulární rostlinná patologie. 10 (3): 311–24. doi:10.1111 / j.1364-3703.2009.00538.x. PMC 6640313. PMID 19400835.
- ^ A b C Moreno AB, Del Pozo AM, Borja M, Segundo BS (listopad 2003). „Aktivita protiplísňového proteinu z Aspergillus giganteus proti Botrytis cinerea“. Fytopatologie. 93 (11): 1344–53. doi:10.1094 / PHYTO.2003.93.11.1344. PMID 18944061.
- ^ Barkai-Golan R (červen 2001). Nemoci ovoce a zeleniny po sklizni (1. vyd.). Elsevier. ISBN 978-0-444-50584-2.
- ^ Szappanos H, Szigeti GP, Pál B, Rusznák Z, Szucs G, Rajnavölgyi E, Balla J, Balla G, Nagy E, Leiter E, Pócsi I, Hagen S, Meyer V, Csernoch L (červenec 2006). „Antifungální protein AFP vylučovaný Aspergillus giganteus nezpůsobuje škodlivé účinky na některé savčí buňky“. Peptidy. 27 (7): 1717–25. doi:10.1016 / j.peptides.2006.01.009. PMID 16500727.
- ^ A b Barakat H, Spielvogel A, Hassan M, El-Desouky A, El-Mansy H, Rath F, Meyer V, Stahl U (červen 2010). „Antifungální protein AFP z Aspergillus giganteus zabraňuje sekundárnímu růstu různých druhů Fusarium na ječmeni“. Aplikovaná mikrobiologie a biotechnologie. 87 (2): 617–24. doi:10.1007 / s00253-010-2508-4. PMID 20217075.
- ^ A b C Theis T, Wedde M, Meyer V, Stahl U (únor 2003). „Antifungální protein z Aspergillus giganteus způsobuje permeabilizaci membrány“. Antimikrobiální látky a chemoterapie. 47 (2): 588–93. doi:10.1128 / aac.47.2.588-593.2003. PMC 151754. PMID 12543664.
- ^ A b Lacadena J, del Pozo AM, Gasset M, Patino B, Campos-Olivas R, Vazquez C a kol. (Prosinec 1995). „Charakterizace antifungálního proteinu vylučovaného MouldAspergillus giganteus“. Archivy biochemie a biofyziky. 324 (2): 273–81. doi:10.1006 / abbi.1995.0040. PMID 8554319.
- ^ A b Binder U, Bencina M, Eigentler A, Meyer V, Marx F (září 2011). „Antifungální protein Aspergillus giganteus AFPNN5353 aktivuje cestu integrity buněčné stěny a narušuje homeostázu vápníku“. Mikrobiologie BMC. 11 (1): 209. doi:10.1186/1471-2180-11-209. PMC 3197501. PMID 21943024.
- ^ A b Girgi M, Breese WA, Lörz H, Oldach KH (červen 2006). „Rezistence vůči rzi a plísni perly proso (Pennisetum glaucum) zprostředkovaná heterologní expresí genu afp z Aspergillus giganteus“. Transgenní výzkum. 15 (3): 313–24. doi:10.1007 / s11248-006-0001-8. PMID 16779647.
- ^ A b C Coca M, Bortolotti C, Rufat M, Peñas G, Eritja R, Tharreau D, del Pozo AM, Messeguer J, San Segundo B (leden 2004). „Transgenní rostliny rýže exprimující antifungální AFP protein z Aspergillus giganteus vykazují zvýšenou odolnost vůči houbě Magnaporthe grisea“. Molekulární biologie rostlin. 54 (2): 245–59. doi:10.1023 / B: PLAN.0000028791.34706,80. PMID 15159626.
- ^ A b C Moreno AB, Peñas G, Rufat M, Bravo JM, Estopà M, Messeguer J, San Segundo B (září 2005). „Produkce antifungálního proteinu AFP z Aspergillus giganteus vyvolaná patogenem propůjčuje transgenní rýži rezistenci vůči vysoké houbě Magnaporthe grisea“. Molekulární interakce rostlin a mikrobů. 18 (9): 960–72. doi:10.1094 / MPMI-18-0960. PMID 16167766.


