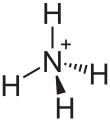
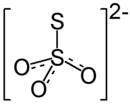
Thiosíran amonný - Ammonium thiosulfate
| |||
| Jména | |||
|---|---|---|---|
| Název IUPAC Thiosíran diamonný | |||
| Ostatní jména Thiosíran amonný, ATS | |||
| Identifikátory | |||
3D model (JSmol ) | |||
| ChEBI | |||
| ChemSpider | |||
| Informační karta ECHA | 100.029.074 | ||
PubChem CID | |||
| UNII | |||
Řídicí panel CompTox (EPA) | |||
| |||
| |||
| Vlastnosti | |||
| H8N2Ó3S2 | |||
| Molární hmotnost | 148.20 g · mol−1 | ||
| Vzhled | bezbarvá nebo bílá pevná látka | ||
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |||
| Reference Infoboxu | |||
Thiosíran amonný (thiosíran amonný v Britská angličtina ) je anorganická sloučenina se vzorcem (NH4)2S2Ó3. Je to bílé krystalický pevné s amoniak vůně, snadno rozpustný v voda, málo rozpustný v aceton a nerozpustný v ethanol a diethylether.[1]
Výroba
Vyrábí se zpracováním siřičitan amonný se sírou:[2]
- (NH4)2TAK3 + S → (NH4)2S2Ó3
Aplikace
Thiosíran amonný se používá v fotografický ustalovač. Jedná se o takzvaný rychlý ustalovač, který působí rychleji než thiosíran sodný ustalovače.[3] Fixace zahrnuje tyto chemické reakce (ilustrováno pro bromid stříbrný ):[4]
- AgBr + 2 (NH4)2S2Ó3 → (NH4)3[Ag (S2Ó3)2] + NH4Br
- AgBr + 3 (NH4)2S2Ó3 → (NH4)5[Ag (S2Ó3)3] + NH4Br
Thiosíran amonný se také používá pro loužení z zlato a stříbrný. Funguje s přítomností měď jako katalyzátor tady. Tento proces je netoxickou alternativou kyanidace zlata.[5] Výhodou thiosíranu amonného je, že pyrolýza jeho komplexů stříbra zanechává zbytek pouze ze sulfidu stříbrného, na rozdíl od komplexů odvozených od thiosíranu sodného.[2]
jiný
Thiosíran amonný lze použít jako a hnojivo.[6] Jak naznačují některé výzkumné studie, lze jej použít jako přísadu do uhlí -odpad směsi ke snížení tvorby velmi nebezpečných látek dioxiny a furany.[7]
Bezpečnost
LD50 (orálně, potkan) je 2890 mg / kg.[2]
Viz také
Reference
- ^ BL - Thiosíran amonný
- ^ A b C J. J. Barbera; A. Metzger; M. Wolf (2012). "Siřičitany, thiosírany a dithionity". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a25_477.
- ^ Praní černobílých filmů a papírů
- ^ Keller, Karlheinz (2005). "Fotografování". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002 / 14356007.a20_001.
- ^ Aylmore, M.G .; Muir, D.M (2001). „Vyluhování thiosíranu zlata - recenze“. Inženýrství minerálů. 14 (2): 135–174. doi:10.1016 / S0892-6875 (00) 00172-2.
- ^ McCarty, G. W .; Bremner 1, J. M .; Krogmeier 1, M. J. (1990). "Hodnocení thiosíranu amonného jako inhibitoru ureázy v půdě". Výzkum hnojiv. 24 (3): 135–139. doi:10.1007 / BF01073581. S2CID 28574791.
- ^ Wielgosiński, Grzegorz (2011). „Snížení emisí dioxinů z procesů výroby tepla a energie“. Journal of the Air & Waste Management Association. 61 (5): 511–526. doi:10.3155/1047-3289.61.5.511. PMID 21608491. S2CID 44546628.