Taxodon - Taxodone
 | |
 | |
| Jména | |
|---|---|
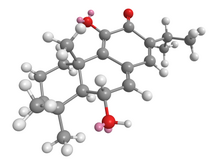
| Název IUPAC (4b.)S, 8aS,9S) -4,9-dihydroxy-4b, 8,8-trimethyl-2-propan-2-yl-6,7,8a, 9-tetrahydro-5H-fenanthren-3-on | |
| Ostatní jména 6,11-dihydroxyabieta-7,9 (11), 13-trien-12-on, NSC122420, AC1L9XIL, CID457961 | |
| Identifikátory | |
3D model (JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Vlastnosti | |
| C20H28Ó3 | |
| Molární hmotnost | 316.441 g · mol−1 |
| Vzhled | Zlatá krystalická pevná látka |
| Bod tání | 176 až 177 ° C (349 až 351 ° F; 449 až 450 K) |
| Nerozpustný | |
| Rozpustnost v chloroformu, alkoholu, hexanu, etheru | Rozpustný |
| Související sloučeniny | |
Související sloučeniny | Taxodion |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Taxodon je přirozeně se vyskytující diterpenoid nalezen v Taxodium distichum (Plešatý cypřiš), Rosmarinus officinalis (Rosemary), několik Salvia druhů a dalších rostlin, spolu s jeho oxidovaným produktem přesmyku, taxodionem. Vystavují taxodon a taxodion protinádorový,[1][2][3] antibakteriální,[4][5][6] antioxidant,[7] protiplísňový,[8] insekticid,[9] a antifeedant[10] činnosti.
Objev
Taxodon byl poprvé izolován v roce 1968 ze semen Taxodium distichum (Bald Cypress) od S. Morris Kupchana a spolupracovníků.[1] Uváděli stanovení struktury a základní chemii taxodonu a jeho oxidovaného přesmyku, taxodionu.[11][12] Taxodon se přirozeně vyskytuje ve formě (+) - taxodonu.
Výskyt
Taxodon a / nebo taxodion byly kromě toho identifikovány v několika rostlinách Taxodium distichum počítaje v to: Rosmarinus officinalis (Rosemary),[13] Salvia barrelieri,[7] Metasequoia glyptostroboides (Dawn Redwood),[4] Salvia munzii (San Diego Sage),[14] Salvia moorcroftiana,[15] Salvia staminea,[16] Salvia clevelandii (Cleveland Sage),[17] Salvia hypargeia,[3] Salvia broussonetii,[18] Salvia montbretii,[19][20] Salvia nipponica,[21][22] Salvia verbenaca (Divoká Clary),[23] Salvia lanigera,[24][25]Salvia prionitida,[26] Salvia deserta,[27] Salvia phlomoides,[28][29] a Plectranthus hereroensis[30]
Taxodon, taxodion a jejich reakční produkty byly použity jako archeologické a geologické biomarkery.[31][32][33][34][35][36][37]
Byly také izolovány analogy taxodonu a taxodionu. 2-hydroxy taxodon a 2-hydroxy-taxodion byly nalezeny v Salvia texana (Texas Sage).[38] 5,6-Didehydro-7-hydroxy-taxodon byl nalezen v Salvia munzii.[14] 7-Hydroxytaxodion, 7,7’-bistaxodion a 11,11’-didehydroxy-7,7’-dihydroxytaxodion byly nalezeny v Salvia montbretti.[19][20]
Aktivita
Taxodon a taxodion mají in vivo aktivita proti Walkerovi intramuskulárně karcinosarkom 256 u potkanů (25, respektive 40 mg / kg) a in vitro aktivita proti buňkám odvozeným od člověka karcinom z nosohltanu (KB) (ED50 = 0,6, respektive 3 ug / ml).[1] Vystavují taxodon a taxodion protiplísňový aktivita proti dřevokazným houbám, přičemž taxodion je zvláště účinný proti Trametes versicolor a Fomitopsis palustris.[8] Taxodione vystavoval nejvyšší antioxidant aktivita mezi testovanými diterpenoidy z kořenů Salvia barrelieri.[7] Taxodon vykazoval silný účinek antibakteriální účinky proti jídlu patogenní bakterie, jako Listeria monocytogenes ATCC 19166, Salmonella typhimurium KCTC 2515, Salmonella enteritidis KCTC 2021, Escherichia coli ATCC 8739, Escherichia coli O157: H7 ATCC 43888, Enterobacter aerogenes KCTC 2190, Staphylococcus aureus ATCC 6538 a Staphylococcus aureus.KCTC 1916[4] Taxodon vykazoval silnou termicidní aktivitu proti podzemí termit, Reticulitermes speratus Kolbe.[9] Taxodion potlačuje neruonální Cl-proud ovládaný receptorem GABAA (IGABA).[39] Taxodion může mít potenciál v léčbě kardiovaskulárních onemocnění.[40]
Patentováno je použití taxodonu a taxodionu k inhibici růstu vlasů.[41][42][43] Patentována je také léčba benigního zvětšení prostaty taxodonem.[44]
Chemie
Taxodon byl prvním izolovaným příkladem a chinon methide[45][46][47][48][49][50] s labilní vodík sousedící s touto reaktivní chromofor.[1] Kupchan prokázal, že taxodon aromatizuje na a katechol keton při vystavení mírnému kyselina. Vzduch oxidace z toho katechol keton poskytuje taxodion.

Syntéza
Taxodon se snadno přeuspořádává v přítomnosti mírného stavu kyseliny a snadno reaguje s nukleofily. I když taxodon vykazuje vyšší hodnoty protinádorový a antibakteriální aktivitou než taxodionem unikal tvorbě v laboratoři více než 25 let kvůli své inherentní nestabilitě. Během této doby několik různých skupin uvedlo syntézu stabilnějšího taxodionu.[51][52][53][54][55][56][57][58][59][60][61][62][63][64][65][66][67][68][69]
V roce 1993 byl taxodon poprvé syntetizován v 16krokové sekvenci s využitím jedinečné elektronové reorganizace fenolbenzyl-epoxidu v posledním kroku.[70][71] Protože se taxodon snadno rozkládá na taxodion, tato syntéza taxodonu také představuje formální syntézu taxodionu.

Od syntézy taxodonu existují další syntézy taxodionu a analogů.[6][72][73]
Poznámky a odkazy
- ^ A b C d Kupchan, S. M .; Karim, A; Marcks, C. (1968). "Inhibitory nádoru. XXXIV. Taxodion a taxodon, dva nové inhibitory nádoru diterpenoid chinon methidu z Taxodium distichum". J. Am. Chem. Soc. 90 (21): 5923–5924. doi:10.1021 / ja01023a061. PMID 5679178.
- ^ Zaghloul A. M .; Gohar A. A .; Naiem Z. A .; Abdel Bar F. M. (2008). „Taxodione, sloučenina vázající DNA z Taxodium distichum L. (Rich.)“. Z. Naturforsch. C. 63 (5–6): 355–360. doi:10.1515 / znc-2008-5-608. PMID 18669020.
- ^ A b Ayhan Ulubelen, Gülaçti Topçu, Hee-Byung Chai a John M. Pezzuto (1999). "Cytotoxická aktivita diterpenoidů izolovaných ze Salvia hypargeia". Farmaceutická biologie. 37 (2): 148–151. doi:10.1076 / phbi.37.2.148.6082.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ A b C Vivek K. Bajpai & Sun Chul Kan (2010). „Antibakteriální diterpenoid abietanového typu, taxodon z Metasequoia glyptostroboides Miki ex Hu ". Journal of Biosciences. 35 (4): 533–538. doi:10.1007 / s12038-010-0061-z. PMID 21289435.
- ^ Vivek K. Bajpai; Minkyun Na; Sun Chul Kang (2010). "Úloha bioaktivních látek při kontrole potravinových patogenů odvozených z Metasequoia glyptostroboides Miki ex Hu ". Potravinová a chemická toxikologie. 48 (7): 1945–1949. doi:10.1016 / j.fct.2010.04.041. PMID 20435080.
- ^ A b Tada M .; Kurabe J .; Yoshida T .; Ohkanda T .; Matsumoto Y. (2010). „Syntézy a antibakteriální aktivity derivátů katecholu diterpenu s kostry abietanu, totaranu a podokarpanu proti Staphylococcus aureus rezistentnímu na meticilin a Propionibacterium acnes“. Chem Pharm Bull. 58 (6): 818–824. doi:10,1248 / cpb.58.818. PMID 20522992.
- ^ A b C Ufuk Kolak; Ahmed Kabouche; Mehmet Öztürk; Zahia Kabouche; Gülaçtl Topçu; Ayhan Ulubelen (2009). "Antioxidační diterpenoidy z kořenů Salvia barrelieri". Fytochemická analýza. 20 (4): 320–327. doi:10,1002 / pca.1130. PMID 19402189.
- ^ A b Norihisa Kusumoto, Tatsuya Ashitani, Tetsuya Murayama, Koichi Ogiyama a Koetsu Takahashi (2010). „Antifungální diterpeny abietanového typu z kuželů Taxodium distichum Bohatý". Journal of Chemical Ecology. 36 (12): 1381–1386. doi:10.1007 / s10886-010-9875-2. PMID 21072573.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ A b Norihisa Kusumoto, Tatsuya Ashitani, Yuichi Hayasaka, Tetsuya Murayama, Koichi Ogiyama a Koetsu Takahashi (2009). „Antitermitické aktivity Diterpenů abietanového typu z Taxodium distichum Šišky “. Journal of Chemical Ecology. 35 (6): 635–642. doi:10.1007 / s10886-009-9646-0. PMID 19475449.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ M. C. Ballesta-Acosta1, M. J. Pascual-Villalobos a B. Rodríguez (2008). „Krátká komunikace. Antifeedantní aktivita přírodních rostlinných produktů vůči larvám Spodoptera littoralis“. Španělský žurnál zemědělského výzkumu. 6 (1): 85–91. doi:10,5424 / sjar / 2008061-304.
- ^ Kupchan, S. M .; Karim, A; Marcks, C. (1969). "Inhibitory nádoru. XLVIII. Taxodion a taxodon, dva nové inhibitory nádoru diterpenoid chinon methidu z Taxodium distichum". J. Org. Chem. 34 (12): 3912–3918. doi:10.1021 / jo01264a036. PMID 5357534.
- ^ Hanson, R. C .; Lardy, H. A .; Kupchan, S. M. (1970). „Inhibice fosfofruktokinázy chinonmethidem a alfa-methylenlaktonovými inhibitory tumoru“. Věda. 168 (3929): 378–380. Bibcode:1970Sci ... 168..378H. doi:10.1126 / science.168.3929.378. PMID 4244949.
- ^ El-Lakany, Abdalla M. (2004). „Chlorosmaridione; Novel Chlorinated Diterpene Quinone Methide from Rosemarinus officinalis L“. Vědy o přírodních výrobcích. 10 (2): 59–62.
- ^ A b Luis, J. G .; Grillo, T. A. (1993). "Nové diterpeny ze Salvia munzii: chemické a biogenetické aspekty". Čtyřstěn. 49 (28): 6277–6284. doi:10.1016 / S0040-4020 (01) 87965-5.
- ^ Simoes, F .; Michavila, A .; Rodriguez, B .; García Alvarez, M. C .; Mashooda, H. (1986). „Diterpenoid chinonmethidu z kořene Salvia moorciuftiana“. Fytochemie. 25 (3): 755–756. doi:10.1016/0031-9422(86)88043-8.
- ^ Gulacti Topcu1, Esra N. Altiner, Seyda Gozcu, Belkis Halfon, Zeynep Aydogmus, J. M. Pezzuto, Bing-Nan Zhou, David G. I. Kingston (2003). "Studie na di- a tritrepenoidech ze Salvia staminea s cytotoxickou aktivitou". Planta Med. 69 (5): 464–467. doi:10.1055 / s-2003-39705. PMID 12802732.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Iván C. Guerrero; Lucía S. Andrés; Leticia G. León; Rubén P. Machín; José M. Padrón; Javier G. Luis & José Delgadillo (2006). „Abietane Diterpenoidy z Salvia pachyphylla a S. clevelandii s cytotoxickou aktivitou proti buněčným liniím lidské rakoviny ". J. Nat. Prod. 69 (12): 1803–1805. doi:10.1021 / np060279i. PMID 17190465.
- ^ M. Fraga; Carmen E. Díaz; Ana Guadaño a Azucena González-Coloma (2005). „Diterpeny z Salvia broussonetii Transformované kořeny a jejich insekticidní aktivita ". J. Agric. Food Chem. 53 (13): 5200–5206. doi:10.1021 / jf058045c. PMID 15969497.
- ^ A b Ayhan Ulubelen; Gülaçti Topcu (1996). „Nové abietanové diterpenoidy ze Salvia montbretii“. J. Nat. Prod. 55 (4): 441–444. doi:10.1021 / np50082a006.
- ^ A b Ayhan Ulubelen; Gülaçti Topcu (1996). „Abietane and Rearranged Abietane Diterpenes from Salvia montbretii“. J. Nat. Prod. 59 (8): 734–737. doi:10.1021 / np9602224.
- ^ Ikeshiro Y .; Mase I .; Tomita Y. (1991). „Diterpenové chinony abietanového typu ze Salvia nipponica“. Planta Med. 57 (6): 588. doi:10.1055 / s-2006-960219. PMID 17226213.
- ^ Hsiu-Hui Chana, Tsong-Long Hwangb, Chung-Ren Sua, Mopur Vijaya Bhaskar Reddya a Tian-Shung Wu (2011). „Protizánětlivé, anticholinesterázové a antioxidační složky z kořenů a listů Salvia nipponica Miq. Var. Formosana“. Fytomedicin. 18 (2–3): 148–150. doi:10.1016 / j.phymed.2010.06.017. PMID 21115331.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ A. Kabouche, Z. Kabouche, R. Touzani a C. Bruneau (2008). „Diterpeny a steroly z kořenů Salvia verbenaca subsp. Clandestina“. Chemie přírodních sloučenin. 44 (6): 824–825. doi:10.1007 / s10600-009-9204-6.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Ik-Soo Lee; Norito Kaneda; Rutt Suttisri; Abdalla M. El-Lakany; Nawal Sabri a A. Douglas Kinghorn (1998). "Nové orthochinony z kořenů Salvia lanigera". Planta Med. 64 (7): 632–634. doi:10.1055 / s-2006-957536. PMID 17253304.
- ^ Sabri, N. N., Abou-Donia, A. A., Assad, A. M., Ghazy, N. M., El-lakany, A. M., Tempesta, M. S. a Sanson D. R. (1989). "Abietane diterpene chinony z kořenů Salvia verbenaca a S. lanigera". Planta Medica. 55 (6): 582. doi:10.1055 / s-2006-962111. PMID 17262492.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Li M .; Zhang J. S .; Ye Y. M .; Fang J. N. (2000). "Složky kořenů Salvia prionitis". J Nat Prod. 63 (1): 139–141. doi:10.1021 / np990357k. PMID 10650097.
- ^ Y. Tezuka; R. Kasimu; J. X. Li; P. Basnet; K. Tanaka; T. Namba; S. Kadot (1998). „Složky kořenů Salvia deserta SCHANG. (Xinjiang-Danshen)“. Chem Pharm Bull. 46 (1): 107–112. doi:10,1248 / cpb.46.107.
- ^ Benjamın Rodrıguez (2003). "Methoxyabietan Diterpenoid z kořene Salvia phlomoides a strukturní korekce jiného Diterpene z Cryptomeria japonica". Z. Naturforsch. 58b: 324–327.
- ^ J. A. Hueso-Rodríguez; M. L. Jimeno; B. Rodrıguez; G. Savona; M. Bruno (1983). "Abietane diterpenoidy z kořene Salvia phlomoides". Fytochemie. 22 (9): 2005–2009. doi:10.1016/0031-9422(83)80033-8.
- ^ Olga Batista, M. Fátima Simões, José Nascimento, Sofia Riberio, Aida Duartea, Benjamín Rodríguez a Maria C. de la Torreb (1996). „Přeskupený abietanový diterpenoid z Plectranthus hereroensis“. Fytochemie. 41 (2): 571–573. doi:10.1016 / 0031-9422 (95) 00646-X. PMID 8821435.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ A. Otto; H. Walther; W. Püttmann (1997). „Sesqui- a diterpenoidní biomarkery konzervované v jílovitých jílovitých jelech bohatých na taxodium, v povodí Weisselster, Německo“. Organická geochemie. 26 (1–2): 105–115. doi:10.1016 / S0146-6380 (96) 00133-7.
- ^ A. Otto; H. Walther; W. Püttmann (1994). „Molekulární složení listnatého a kořenového Oligocene Oxbow Lake Clay v Weisselster Basin, Německo“. Organická geochemie. 22 (2): 275–286. doi:10.1016/0146-6380(94)90174-0.
- ^ Angelika Otto; Bernd R. T. Simoneit; William C. Rember (2003). „Pryskyřičné sloučeniny ze semenných šišek tří druhů fosilních jehličnanů z miocénní flóry Clarkia, Emerald Creek, Idaho, USA a ze souvisejících existujících druhů“. Recenze paleobotaniky a palynologie. 126 (3–4): 225–241. doi:10.1016 / S0034-6667 (03) 00088-5.
- ^ Maya Stefanova; Bernd R.T. Simoneit (2008). „Polární aromatické biomarkery chukurovského pryskyřice miocénního věku a korelace s progenitorovou makrofosílií“. International Journal of Coal Geology. 75 (3): 166–174. doi:10.1016 / j.coal.2008.05.003.
- ^ A. Zdravkov; A. Bechtel; R. F. Sachsenhofer; J. Kortenski; R. Gratzer (2011). „Vegetační rozdíly a diagenetické změny mezi dvěma bulharskými ložisky hnědého uhlí - poznatky z petrologie uhlí a složení biomarkerů“. Organická geochemie. 42 (3): 237–254. doi:10.1016 / j.orggeochem.2010.12.006.
- ^ Yann Hautevelle; Raymond Michels; Fabrice Malartre; Alain Trouiller (2006). „Cévnaté rostlinné biomarkery jako proxy pro paleofloru a paleoklimatické změny při přechodu Dogger / Malm v pařížské pánvi (Francie)“. Organická geochemie. 37 (5): 610–625. doi:10.1016 / j.orggeochem.2005.12.010.
- ^ Kenneth E. Peters; Clifford C. Walters; J. Michael Moldowan (2005). „Průvodce biomarkery: biomarkery a izotopy v ropných systémech a historie Země“. 2: 546. Citovat deník vyžaduje
| deník =(Pomoc) - ^ Gonzalez, A. G .; Aguilar, Z. E .; Luis, J. G; Ravelo, A. G .; Dominguez, X. (1988). "Quinon methide diterpenoidy z kořenů Salvia texana". Fytochemie. 27 (6): 1777–1781. doi:10.1016/0031-9422(88)80442-4.
- ^ D. Rutherford; M. Nielsen; N. Tokutomi; N. Akaike (1994). "Účinky rostlinných diterpenů na neuronový GABAA receptorem ovládaný chloridový proud". NeuroReport. 5 (18): 2569–2572. doi:10.1097/00001756-199412000-00041. PMID 7696606.
- ^ C. R. Tirapelli; S.R. Ambrosio; F. B. da Costa; A. M. de Oliveira (2008). „Diterpenes: terapeutický příslib pro kardiovaskulární onemocnění“. Nedávné patenty na kardiovaskulární objevy drog. 3 (1): 1–8. doi:10.2174/157489008783331689. PMID 18221123.
- ^ US patent 5824665
- ^ US patent 6218435
- ^ Americký patent 20070203240
- ^ Světový patent 2004064736
- ^ Karantsios, D .; Scarpa, J. S .; Eugster, C. H. (1966). "Struktur von Fuerstion". Helv. Chim. Acta. 49 (3): 1151–1172. doi:10,1002 / hlca.19660490313.
- ^ Gonzalez, A. G .; Fraga, B. M .; Gonzalez, C. M. (1983). „Rentgenová analýza netzahualcoyonu, methide triterpenového chinonu orthosphenia mexicana". Čtyřstěn. 84 (29): 3033–3036. doi:10.1016 / s0040-4039 (00) 88088-0.
- ^ Simoes, F .; Miehavila, A; Rodríguez. B .; García Alvarez, M. C .; Mashooda, H. (1986). „Diterpenoid chinonmethidu z kořene Salvia moorciuftiana“. Fytochemie. 25 (3): 755–756. doi:10.1016/0031-9422(86)88043-8.CS1 maint: více jmen: seznam autorů (odkaz)
- ^ Sankaram, A. V. B .; Murthi, M. M .; Bhaskaraiah, K .; Narasimha Rao, G. L .; Suhrahmanyam, M .; Shoolery, J. N. (1988). „Bharangin, nový diterpenoid chinonemethid z pygmacopremna herbacea (Roxb.) Moldenke“. Tetrahedron Lett. 29 (2): 245–248. doi:10.1016 / S0040-4039 (00) 80066-0.
- ^ Fernando, H. C .; Gunatilaka, A. A. L .; Kumar, V .; Weexatunga, G. (1988). "Dva nové chinon-methidy z cassine balae: revidovaná struktura balaenonolu". Tetrahedron Lett. 29 (3): 387–390. doi:10.1016 / S0040-4039 (00) 80104-5.
- ^ Sankaram, A. V. B .; Bhaskaraiah, K .; Marthandamurthi. M .; Subrahmanyam, M. (1989). „Isobharangin, nový biogeneticky významný diterpenoid chinonemethid z pygmacopremna herbacea (Roxb.) Moldenke“. Tetrahedron Lett. 30 (7): 867–868. doi:10.1016 / S0040-4039 (01) 80638-9.
- ^ Mori, K .; Matsui, M. (1970). "Celková syntéza diterpenoidů. XIII Taxodion, inhibitor nádoru chinonmethidu". Čtyřstěn. 26 (14): 3467–3473. doi:10.1016 / S0040-4020 (01) 92926-6. PMID 5449327.
- ^ Matsumoto, T .; Tachibana, Y .; Uchida, J .; Fukui, K. (1971). „Celková syntéza (±) -axodionu, inhibitoru nádoru“. Býk. Chem. Soc. Jpn. 44 (10): 2766–2770. doi:10,1246 / bcsj.44.2766.
- ^ Matsumoto, T .; Ohsuga, Y .; Fukui, K. (1974). "Syntéza taxodionu a methyl-11-hydroxy-12-methoxy-7-oxobieta-8,11,13-trien-18-oátu". Chem. Lett. 3 (3): 297–300. doi:10.1246 / cl.1974.297.
- ^ Matsumoto, T .; Osbuga, Y .; Harada, S .; Fukui, K. (1977). „Syntéza taxodionu, royleanonu, kryptojaponolu a methylu 11-hydroxy-12-methoxy-7-oxoabieta-8,11) 13-trien-18-oátu“. Býk. Chem. Soc. Jpn. 50: 266–272. doi:10,1246 / bcsj.50.266.
- ^ Matsumoto. T .; Usui, S .; Morimoto. T. (1977). „Pohodlná syntéza (±) -Taxodionu, (±) -Ferruginolu a (±) -Sugiolu“. Býk. Chem. Soc. Jpn. 50 (6): 1575–1579. doi:10,1246 / bcsj.50.1575.
- ^ Ohtsuka, Y .; Tahara, A. (1978). "Diterpenoidy. XLVI. Syntézy taxodionu, royleanonu a jejich analogů". Chem. Pharm. Býk. 26 (7): 2007–2013. doi:10.1248 / cpb.26.2007.
- ^ Snitman, D.L .; Himmelsbach, R. J .; Haltiwanger, R. C .; Watt, D. S. (1979). "Syntéza (±)-kryptojaponolu a (±) -taxodionu". Tetrahedron Lett. 20 (27): 2477–2480. doi:10.1016 / S0040-4039 (01) 86325-5.
- ^ Johnson, W. S .; Shenvi, A. B .; Boots, S. G. (1982). "Přístup k taxodionu zahrnující biomimetickou metodiku cyklizace polyenu". Čtyřstěn. 38 (10): 1397–1404. doi:10.1016/0040-4020(82)80219-6.
- ^ Stevens, R. V .; Bisaochi, G. G. (1982). "Benzocyklobutenony jako synthony pro syntézu C-11 okysličených diterpenoidů. Aplikace na celkovou syntézu (. + -.) - taxodionu". J. Org. Chem. 47 (12): 2396–2399. doi:10.1021 / jo00133a032.
- ^ Poirier, D .; Jean, M .; Burnell, R. H. (1983). "Alternativní syntézy Taxodionu". Synth. Commun. 13 (3): 201–205. doi:10.1080/00397918308065989.
- ^ Banerjee, AK; Carrasco, M. C. (1988). "Syntetické přístupy k (±) -axodionu". Synth. Commun. 13 (4): 281–287. doi:10.1080/00397918308066977.
- ^ Banerjee, A. K; Carrasco, M. C. (1986). „Celková syntéza (±) -12-methoxyabieta-8,11,13-trien-6-onu, univerzálního meziproduktu pro syntézu diterpenu“. J. Chem. Soc., Perkin Trans. 1: 25–31. doi:10.1039 / p19860000025.
- ^ Burnell, P. H .; Jean, M .; Poirer, D. (1987). "Syntéza taxodionu". Umět. J. Chem. 65 (4): 775–781. doi:10.1139 / v87-132.
- ^ Engler, T. A .; Sampath. U .; N aganathan, S .; Van Der Velde, D .; Takusagawa, F. (1989). "Nový obecný syntetický přístup k diterpenům: Aplikace na syntézy (. + -.) - taxodionu a (. + -.) - royleanonu". J. Org. Chem. 54 (24): 5712–5727. doi:10.1021 / jo00285a018.
- ^ Haslinger, E .; Michl, G. (1988). "Syntéza (+) - taxodionu z (-) - abietové kyseliny". Tetrahedron Lett. 29 (45): 5751–5754. doi:10.1016 / S0040-4039 (00) 82181-4.
- ^ Haslinger, E .; Michl, G. (1989). "chybějící". Justus Liebigs Ann. Chem. 1989 (7): 677–686. doi:10.1002 / jlac.198919890212.
- ^ Harring, S. R; Livinghouse, T. (1992). „Stručná biomimetická celková syntéza (±) -taxodionu prostřednictvím BF3·Já ne2 podporovaná kationtová kaskádová anulace ". J. Chem. Soc., Chem. Commun. (6): 502–503. doi:10.1039 / C39920000502.
- ^ Ruedi, P .; Eugster, C. H. (1981). „14-Hydroxytaxodion: Partialsynthese und Reaktionen“. Helv. Chim. Acta. 64 (7): 2219–2226. doi:10,1002 / hlca.19810640728.
- ^ Matsumoto, T .; Kawashima, H .; Iyo, K. (1982). "Syntéza 3.BETA.-hydroxytaxodionu a coleonů S a T". Býk. Chem. Soc. Jpn. 55 (4): 1168–1173. doi:10,1246 / bcsj.55.1168.
- ^ Sanchez, Anthony J .; Konopelski, Joseph P. (1994). "První celková syntéza (±) -Taxodonu". Synlett. 1994 (5): 335–336. doi:10.1055 / s-1994-22844.
- ^ Sanchez, Anthony J .; Konopelski, Joseph P. (1994). "Fenolbenzylpoxid na chinonmethidovou elektronovou reorganizaci: Syntéza (±) -axodonu". J. Org. Chem. 59 (18): 5445–5452. doi:10.1021 / jo00097a057.
- ^ Scott R. Harring & Tom Livinghouse (1994). „Polyenové kaskádové cyklizace zprostředkované BF3· CH3NE2. neobvykle efektivní metoda pro přímou stereospecifickou syntézu polycyklických meziproduktů prostřednictvím kationtové iniciace na nefunkčních 3 ° alkénech. Aplikace na celkovou syntézu (±) -taxodionu “. Čtyřstěn. 50 (31): 9229–9254. doi:10.1016 / S0040-4020 (01) 85502-2.
- ^ E. Alvarez-Manzaneda, R. Chahboun, E. Cabrera, E. Alvarez, R. Alvarez-Manzaneda, M. Lachkar a I. Messouri (2007). „První syntéza picealaktonu C. Nová cesta k terpenoidům souvisejícím s taxodionem z kyseliny abietové“. Tetrahedron Lett. 48 (6): 989–992. doi:10.1016 / j.tetlet.2006.12.009.CS1 maint: více jmen: seznam autorů (odkaz)
Viz také
externí odkazy
- První celková syntéza (±) -axodonu
- Sanchez, Anthony J .; Konopelski, Joseph P. (1994). „Fenolbenzylpoxid na chinonmethidovou elektronovou reorganizaci: Syntéza (±) -axodonu“. J. Org. Chem. 59 (18): 5445–5452. doi:10.1021 / jo00097a057.
- Taxodon, vstup Pubchem
- Quinone methides, Steven Edward Rokit
- Biologické a toxikologické důsledky tvorby chinonmethidu
- Nedávné pokroky v chemii inhibitorů terpenoidních nádorů
