Prodigiosin - Prodigiosin
 | |
| Jména | |
|---|---|
| Název IUPAC 4-methoxy-5 - [(Z) - (5-methyl-4-pentyl-2H-pyrrol-2-yliden) methyl] -1H,1′H-2,2'-bipyrrol | |
| Identifikátory | |
3D model (JSmol ) | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Pletivo | Prodigiosin |
PubChem CID | |
| UNII | |
| |
| |
| Vlastnosti | |
| C20H25N3Ó | |
| Molární hmotnost | 323.440 g · mol−1 |
Pokud není uvedeno jinak, jsou uvedeny údaje o materiálech v nich standardní stav (při 25 ° C [77 ° F], 100 kPa). | |
| Reference Infoboxu | |
Prodigiosin je červený pigment produkovaný mnoha kmeny bakterie Serratia marcescens,[1] stejně jako další gramnegativní, gama proteobakterie, jako je Vibrio psychroerythrus a Hahella chejuensis.[2] Je zodpovědný za růžový odstín, který se občas vyskytuje ve špíně, která se hromadí na porcelánových površích, jako jsou vany, umyvadla a toaletní mísy. Je to v prodigininy skupina sloučenin, které se produkují v některých gramnegativních gama proteobakteriích, stejně jako vybrané grampozitivní aktinobakterie (např. Streptomyces coelicolor).[2] Název prodigiosin je odvozen z podivuhodný (tj. něco úžasného).
Sekundární metabolit
Prodigiosin je sekundární metabolit Serratia marcescens. Protože je snadno detekovatelný, byl použit jako modelový systém ke studiu sekundárního metabolismu. Již dlouho je známo, že produkce prodigiosinu je zvýšena omezením fosfátů. V podmínkách s nízkým obsahem fosfátů bylo prokázáno, že pigmentované kmeny rostou na vyšší hustotu než nepigmentované kmeny.[3]
Náboženská funkce
Schopnost pigmentovaných kmenů Serratia marcescens růst chléb vedlo k možnému vysvětlení Středověký transsubstanciační zázraky, ve kterých Eucharistická chléb se převádí na Tělo Kristovo. Takový zázraky vedl k Papež Urban IV zavádění Svátek Božího těla v roce 1264. Následovala oslava a Hmotnost na Bolsena v roce 1263 vedená a Český kněz, který měl pochybnosti o tom transsubstanciace. Během mše se zdálo, že eucharistie krvácí a pokaždé, když kněz otřel krev, objevily se další. Tato událost se slaví v freska v Papežském paláci v Vatikán, maloval Raphael.[4]
Biologická aktivita
Prodigiosinu byla věnována obnovená pozornost[2][5] pro svou širokou škálu biologických aktivit, včetně aktivit proti malárii,[6] protiplísňový,[7] imunosupresivum,[8] a antibiotická činidla.[9] Možná je nejlépe známý svou schopností spouštět apoptózu maligních rakovinných buněk. Přesný mechanismus této inhibice je velmi složitý a není zcela objasněn, ale může zahrnovat více procesů, včetně inhibice fosfatázy, štěpení dvouřetězcové DNA zprostředkované mědí nebo narušení gradientu pH transmembránovým transportem iontů H + a Cl-.[10] Výsledkem je, že prodigiosin je vysoce slibným léčivem a je v současné době v preklinické fázi studie léčby rakoviny pankreatu.[11]Nedávno bylo zjištěno, že prodigiosin má vynikající aktivitu proti stacionární fáze Borrelia burgdorferi, původce Lyme nemoc.[12]
Biosyntéza
Tato sekce chybí informace o konkrétních enzymech / operonu (zkuste Williamson). (Dubna 2019) |

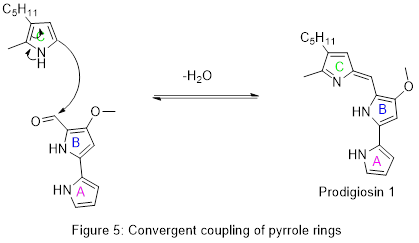
Biosyntéza prodigiosinu[13][14] zahrnuje konvergentní kopulaci tří kruhů pyrrolového typu (na obrázku 1 označených A, B a C) z L-prolinu, L-Serinu, L-methioninu, pyruvátu a 2-oktenalu.
Kruh A je syntetizován z L-prolinu cestou nerribozomální peptidové syntázy (NRPS) (obrázek 2), přičemž pyrrolidinový kruh prolin je dvakrát oxidován prostřednictvím FAD + za vzniku pyrolového kruhu A.

Kruh A je poté expandován polyketidovou syntázovou cestou k začlenění L-serinu do kruhu B (obrázek 3). Kruhový fragment je přenesen z peptidylového nosného proteinu (PCP) do acylového nosného proteinu (ACP) doménou KS, následovaný přenosem na malonyl-ACP dekarboxylační Claisenovou kondenzací. Tento fragment je poté schopen reagovat s maskovaným karbaniontem vytvořeným z PLP zprostředkované dekarboxylace L-serinu, který cyklizuje v dehydratační reakci za vzniku druhého pyrrolového kruhu. Tento meziprodukt je poté modifikován methylací (která obsahuje methylovou skupinu z L-methioninu na alkohol v poloze 6) a oxidací primárního alkoholu na aldehyd za vzniku kruhové struktury jádra A-B.

Kruh C je vytvořen z TPP zprostředkované dekarboxylativní adicí pyruvátu na 2-oktenal, následovanou reakcí s PLP za vzniku aminu pro intramolekulární kondenzaci. Oxidací vzniklého kruhu se získá konečný pyrolový kruh C.

Nakonec jsou tyto dva kousky sešity dohromady při dehydratační reakci poháněné vpřed vytvořením konjugovaného systému napříč všemi třemi kruhy. Tím je dokončena konvergentní syntéza přírodního produktu.
Viz také
- Obatoclax, experimentální lék se související chemickou strukturou
Reference
- ^ Bennett JW, Bentley R (2000). „Vidět červenou: Příběh prodigiosinu“. Adv Appl Microbiol. Pokroky v aplikované mikrobiologii. 47: 1–32. doi:10.1016 / S0065-2164 (00) 47000-0. ISBN 9780120026470. PMID 12876793.
- ^ A b C Williamson NR, Fineran PC, Gristwood T, Leeper FJ, Salmond GP (2006). „Biosyntéza a regulace bakteriálních prodigininů“. Příroda Recenze Mikrobiologie. 4 (12): 887–899. doi:10.1038 / nrmicro1531. PMID 17109029. S2CID 11649828.
- ^ M. Todd-Guay a P.H. Demchick. 1995. Role prodigiosinu ve fosfátu hladovějící Serratia marcescens. Abstrakt výročního zasedání, Americká společnost pro mikrobiologii.
- ^ „Mše v Bolseně od Raphaela“. Vatikánská muzea. Citováno 2017-08-18.
- ^ Williamson NR, Fineran PC, Gristwood T, Chawrai SR, Leeper FJ, Salmond GP (2007). "Protirakovinné a imunosupresivní vlastnosti bakteriálních prodigininů". Budoucí mikrobiol. 2 (6): 605–618. doi:10.2217/17460913.2.6.605. PMID 18041902.
- ^ Castro, A. J. (1967). "Antimalarická aktivita prodigiosinu". Příroda. 213 (5079): 903–904. Bibcode:1967 Natur.213..903C. doi:10.1038 / 213903a0. PMID 6030049. S2CID 4221849.
- ^ Berg, G. Rozmanitost antifungálních a rostlinných kmenů Serratia plymuthica. J. Appl. Microbiol. 88, 952–960 (2000).
- ^ Magae, J., Miller, M. W., Nagai, K. & Shearer, G. M. Účinek metacykloprodigiosinu, inhibitoru zabijáckých T buněk na transplantaci myší kůže a srdce. J. Antibiot. (Tokio) 49, 86–90 (1996).
- ^ Kataoka, T .; et al. (1995). „Prodigiosin 25-C odpojuje vakuolární H + -ATPázu, inhibuje vakuolární okyselování a ovlivňuje zpracování glykoproteinů“. FEBS Lett. 359 (1): 53–59. doi:10.1016/0014-5793(94)01446-8. PMID 7851530. S2CID 30504320.
- ^ Rastogi, S .; et al. (2013). "Syntetické prodigioseny a vliv substituce C-kruhu na štěpení DNA, transmembránový transport chloridů a zásaditost". Org. Biomol. Chem. 11 (23): 3834–3845. doi:10.1039 / c3ob40477c. PMID 23640568.
- ^ Perez-Tomas, R .; Vinas, M. (2010). „Nové poznatky o protinádorových vlastnostech prodigininů“. Curr. Med. Chem. 17 (21): 2222–2231. doi:10.2174/092986710791331103. PMID 20459382.
- ^ Feng, Jie; Shi, Wanliang; Zhang, Shuo; Zhang, Ying (3. června 2015). „Identifikace nových sloučenin s vysokou aktivitou proti stacionární fázi Borrelia burgdorferi ze sbírky sloučenin NCI“. Vznikající mikroby a infekce. 4 (5): e31–. doi:10.1038 / emi.2015.31. PMC 5176177. PMID 26954881.
- ^ Walsh, C. T., Garneau-Tsodikova, S. & Howard-Jones, A. R. Biologická tvorba pyrrolů: Nature's logic and enzymatic machinery. Nat. Prod. Rep. 23, 517–531 (2006).
- ^ Hu, Dennis X .; Withall, David M .; Challis, Gregory L .; Thomson, Regan J. (2016). „Struktura, chemická syntéza a biosyntéza přírodních produktů prodigininu“. Chemické recenze. 116 (14): 7818–7853. doi:10.1021 / acs.chemrev.6b00024. PMC 5555159. PMID 27314508.
