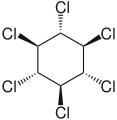
Hexachlorcyklohexan - Hexachlorocyclohexane
Hexachlorcyklohexan (HCH), C
6H
6Cl
6, je některý z několika polyhalogenované organické sloučeniny skládající se z a šestikarbonový kruh s jedním chlór a jeden vodík připojené ke každému uhlíku. Tato struktura má devět stereoizomery (osm diastereomery, z nichž jeden má dva enantiomery ), které se liší podle stereochemie jednotlivých substituentů chloru na cyklohexan. Někdy se to mylně nazývá „benzen hexachlorid „(BHC). Byly použity jako modely pro analýzu účinků různých geometrických poloh velkých atomů s dipolárními vazbami na stabilitu cyklohexanová konformace.[1] Izomery jsou jedovaté, pesticidní a perzistentní organické znečišťující látky, v různé míře.
Hexachlorcyklohexan byl dimerizován pro výrobu mirex, zakázaný pesticid.
Běžné formy jsou:
- alfa-hexachlorcyklohexan, α-HCH nebo α-BHC (CAS RN: 319-84-6 ), opticky aktivní izomer
- beta-hexachlorcyklohexan, β-HCH nebo β-BHC (CAS RN: 319-85-7 )
- gama-hexachlorcyklohexan, γ-HCH, γ-BHC nebo lindan (CAS RN: 58-89-9 ), nejvíce insekticidní izomer
- delta-hexachlorcyklohexan, δ-HCH nebo δ-BHC (CAS RN: 319-86-8 )
- technický hexachlorcyklohexan, t-HCH nebo t-BHC (CAS RN: 608-73-1 ), směs izomerů
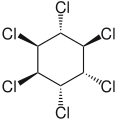
α-Hexachlorcyklohexan, levotočivý enantiomer
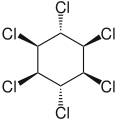
γ-hexachlorcyklohexan, lindan
Chlorace benzen pod elektrofilní aromatická substituce podmínky (Cl2/ FeCl3 nebo Cl2/ AlCl3) vyrábí chlorbenzen. Jelikož mono-chloro-de-hydrogenace deaktivuje molekulu proti dalším elektrofilním reakcím, může být reakce zastavena při substituci jednoho atomu chloru.
- Elektrofilní chlorace: C6H6 + Cl2 → C.6H5Cl + HCl
Naproti tomu chlorace benzenu pod radikální sčítání podmínky (tř2, hν (fotochlorace ) nebo Cl2, Δ, vysoká P) poskytuje hexachlorcyklohexanové izomery po třech po sobě jdoucích krocích radikální dichlorace. Přidání spíše než substituce dochází díky velmi vysoké disociační energii vazby C – H (112 kcal / mol), která znevýhodňuje abstrakci atomu vodíku. Přidání Cl2 ničí aromatičnost benzenového kruhu a přidání dalších dvou Cl2 molekuly jsou ve srovnání s prvními rychlé. Z této reakce lze tedy izolovat pouze třikrát dichlorovaný produkt.
- Radikální přidání: C6H6 + 3Cl2 → C.6H6Cl6
Hexachlorcyklohexanové izomery s více než jedním atomem chloru na uhlík jsou:
- 1,1,2,3,4,5-hexachlorcyklohexan
- 1,1,2,3,4,6-hexachlorcyklohexan
- 1,1,2,3,5,6-hexachlorcyklohexan
- 1,1,2,2,3,4-hexachlorcyklohexan
- 1,1,2,2,3,5-hexachlorcyklohexan
- 1,1,2,2,3,6-hexachlorcyklohexan
- 1,1,2,2,4,5-hexachlorcyklohexan
- 1,1,2,3,3,4-hexachlorcyklohexan
- 1,1,2,3,3,5-hexachlorcyklohexan
- 1,1,2,3,4,4-hexachlorcyklohexan
- 1,1,3,3,5,5-hexachlorcyklohexan
- 1,1,2,4,4,5-hexachlorcyklohexan
- 1,1,2,4,4,6-hexachlorcyklohexan
- 1,1,2,4,5,5-hexachlorcyklohexan
- 1,1,2,5,6,6-hexachlorcyklohexan
- 1,1,2,2,3,3-hexachlorcyklohexan
- 1,1,2,2,4,4-hexachlorcyklohexan
- 1,1,3,3,5,5-hexachlorcyklohexan
Reference
- ^ Zdravkovski, Zoran (2004). "Teoretická studie stability hexachlor- a hexafluorocyklohexanových izomerů" (PDF). Bulletin of the Chemists and Technologists of Macedonia. 23 (2): 131–137. Archivovány od originál (PDF) dne 28. 12. 2005. Citováno 2016-04-17.
externí odkazy
| Tento článek o organický halogenid je pahýl. Wikipedii můžete pomoci pomocí rozšiřovat to. |