Vlnová délka disperzní rentgenová spektroskopie - Wavelength-dispersive X-ray spectroscopy
Tato stránka byla odstraněna z indexů vyhledávačů.
| Akronym | WDXS WDS |
|---|---|
| Klasifikace | Spektroskopie |
| Analyty | Prvky v pevných látkách, kapalinách, prášcích a tenkých vrstvách |
| Výrobci | Anton Paar, Bruker AXS, Hecus, Malvern Panalytical, Rigaku Corporation, Xenocs |
| Další techniky | |
| Příbuzný | Energeticky disperzní rentgenová spektroskopie |
Vlnová délka disperzní rentgenová spektroskopie (WDXS nebo WDS) je nedestruktivní analytická technika používaná k získání elementárních informací o řadě materiálů měřením charakteristických rentgenových paprsků v malém rozsahu vlnových délek. Tato technika generuje a spektrum ve kterých vrcholy odpovídají konkrétním rentgenovým čarám a prvkům lze snadno identifikovat. WDS se primárně používá v chemické analýze, disperzní vlnové délky Rentgenová fluorescence (WDXRF) spektrometrie , elektronové mikro sondy, rastrovací elektronové mikroskopy a vysoce přesné experimenty pro testování atomové a plazmové fyziky.
Teorie
Vlnová délka disperzní rentgenová spektroskopie je založena na známých principech toho, jak jsou charakteristické rentgenové paprsky generovány vzorkem a jak jsou rentgenové paprsky měřeny.
Generování rentgenových paprsků
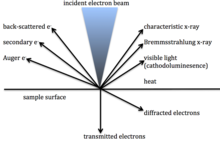
Rentgenové záření se generuje, když elektronový paprsek s dostatečně vysokou energií uvolní elektron z vnitřku orbitální uvnitř atomu nebo iontu a vytváří prázdnotu. Tato prázdnota je vyplněna, když elektron z vyšší orbity uvolní energii a klesne dolů, aby nahradil uvolněný elektron. Energetický rozdíl mezi dvěma orbitaly je charakteristický pro elektronová konfigurace atomu nebo iontu a lze je použít k identifikaci atomu nebo iontu.[1]
Nejlehčí prvky, vodík, hélium , lithium, Berýlium až do atomového čísla 5, nemají elektrony na vnějších orbitálech, aby nahradily elektron vytlačený elektronovým paprskem, a proto je nelze pomocí této techniky detekovat.[2]
Rentgenové měření
Podle Braggův zákon, když rentgenový paprsek vlnové délky „λ“ narazí na povrch krystalu pod úhlem „Θ“ a krystal má roviny atomové mřížky ve vzdálenosti „d“ od sebe, pak konstruktivní interference bude mít za následek paprsek difrakčních rentgenových paprsků, které budou emitovány z krystalu pod úhlem „Θ“, pokud
- nλ = 2d sinΘ, kde n je an celé číslo.[1]
To znamená, že krystal se známou velikostí mřížky odkloní paprsek rentgenových paprsků od konkrétního typu vzorku v předem stanoveném úhlu. Rentgenový paprsek lze měřit umístěním detektoru (obvykle a scintilační čítač nebo a proporcionální počítadlo ) v cestě vychýleného paprsku a protože každý prvek má výraznou vlnovou délku rentgenového záření, lze více prvků určit pomocí více krystalů a více detektorů.[1]
Pro zlepšení přesnosti jsou rentgenové paprsky obvykle kolimoval paralelními měděnými čepelemi zvanými a Söllerův kolimátor. Monokrystal, vzorek a detektor jsou namontovány přesně na a goniometr přičemž vzdálenost mezi vzorkem a krystalem se rovná vzdálenosti mezi krystalem a detektorem. Obvykle se provozuje ve vakuu, aby se snížila absorpce měkkého záření (nízkoenergetické fotony) vzduchem a tím se zvýšila citlivost pro detekci a kvantifikaci světelných prvků (mezi bór a kyslík ). Tato technika generuje spektrum s vrcholy odpovídajícími rentgenovým čarám. To se porovnává s referenčními spektry, aby se určilo elementární složení vzorku.[3]
Jak se zvyšuje atomové číslo prvku, existuje více možných elektronů na různých energetických úrovních, které lze vysunout, což vede k rentgenovým paprskům s různými vlnovými délkami. To vytváří spektra s více řádky, jednou pro každou energetickou hladinu. Největší vrchol ve spektru je označen K.α, další K.β, a tak dále.
Aplikace
Mezi aplikace patří analýza katalyzátorů, cementu, potravin, kovů, těžebních a minerálních vzorků, ropy, plastů, polovodičů a dřeva.[4]
omezení
- Analýza je obecně omezena na velmi malou oblast vzorku, ačkoli moderní automatizované zařízení často používá vzory mřížky pro větší oblasti analýzy.[4]
- Tato technika nemůže rozlišovat mezi izotopy prvků jako elektronová konfigurace izotopů prvku jsou identické.[2]
- Nemůže měřit valenční stav prvku, například Fe2+ vs Fe3+.[2]
- V určitých prvcích je K.α čára může překrývat K.β jiného prvku, a tedy pokud je přítomen první prvek, nelze druhý prvek spolehlivě detekovat (například PROTI K.α překrývá Ti K.β)[2]
Reference
- ^ A b C „BraggsLaw“. Geochemické vybavení a analýza. 10. listopadu 2016. Citováno 14. září 2020.
- ^ A b C d „Vlnová délka - disperzní spektroskopie (WDS)“. Geochemické vybavení a analýza. 10. listopadu 2016.
- ^ „Úvod do rentgenové mikroanalýzy disperzní na energii a na vlnové délce“. Wiley Analytical Science. 14. září 2020. Citováno 14. září 2020.
- ^ A b "EDXRF - XRF - elementární analýza". Applied Rigaku Technologies Inc.. Citováno 14. září 2020.
